КЛАССИФИКАЦИЯ СИСТЕМНЫХ ВАСКУЛИТОВ
Любая клиническая и клинико-морфологическая классификация полиэтиологического процесса воспаления сосудов с единой фенотипической картиной обречена на постоянный пересмотр в связи с достижениями в области молекулярной генетики и клеточной биологии. В научных целях нужны договорные рамки или критерии, позволяющие группировать больных для эпидемиологических и клинических исследований. На последней согласительной конференции в Чапел-Хилле (США), состоявшейся в 2012 г., были выделены шесть групп васкулитов: васкулиты крупных, средних и мелких сосудов, иммунокомплексные васкулиты, а также васкулиты, связанные с системными заболеваниями и ассоциированные с инфекциями (табл.) [29].
Таблица
Определения васкулитов с классификационными критериями для детей [4]
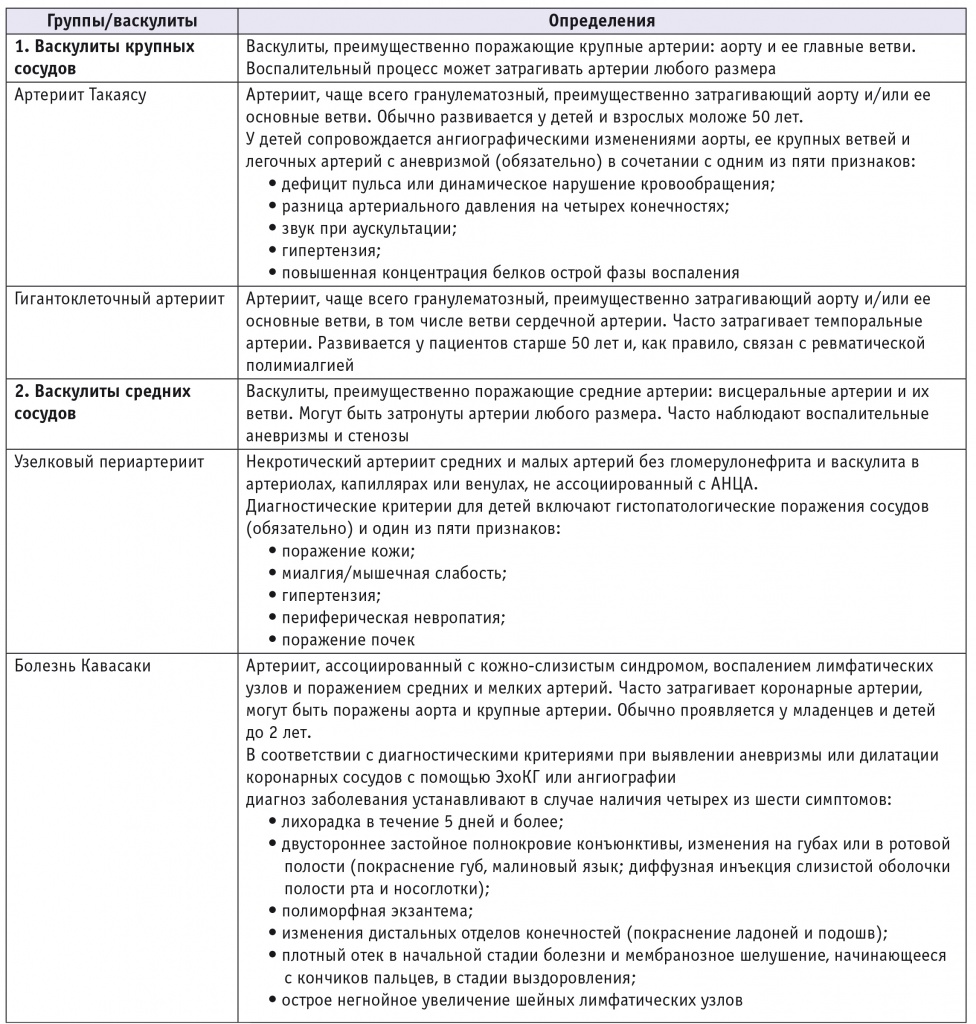
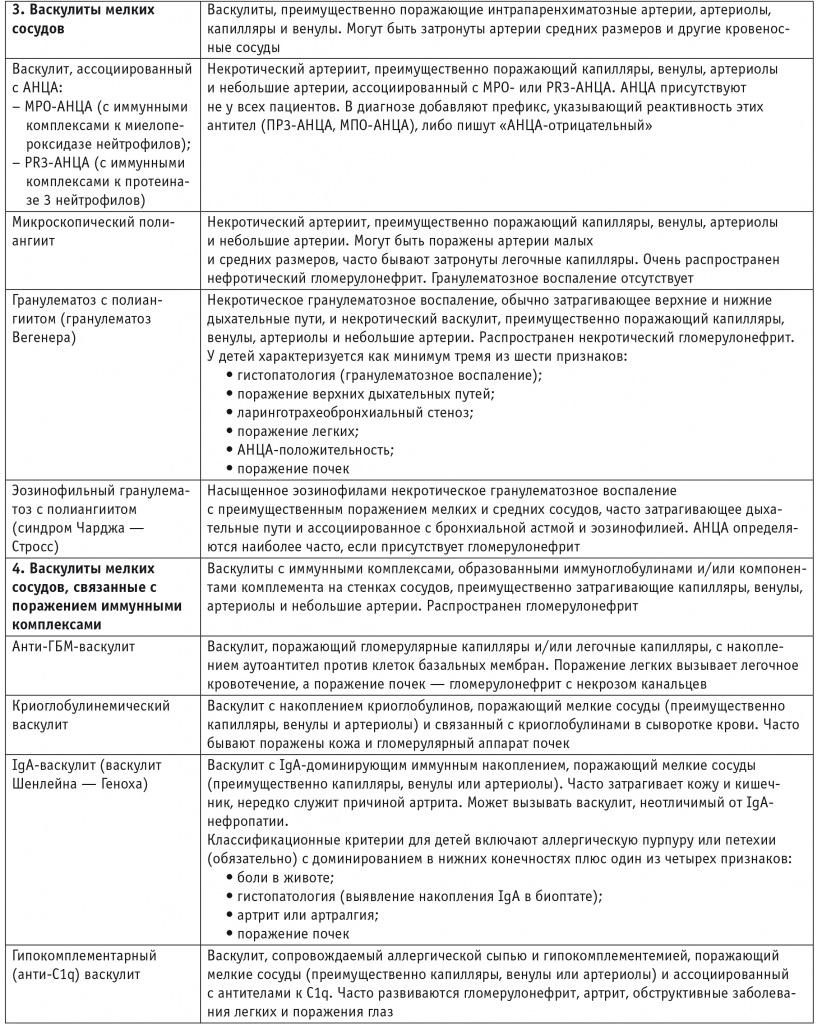
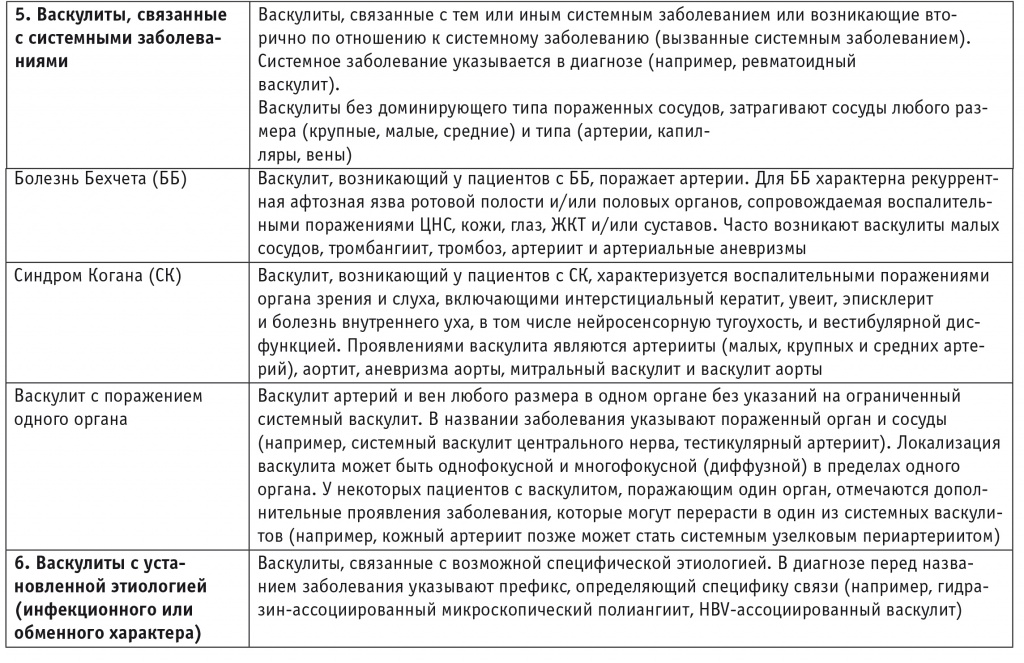
Примечание. АНЦА — антинейтрофильные цитоплазматические антитела; ГБМ — гломерулярная базальная мембрана; ЖКТ — желудочно-кишечный тракт; ЦНС — центральная нервная система; HBV — вирус гепатита B.
IgA-васкулит (пурпура Шенлейна — Геноха)
IgA-васкулит/пурпура Шенлейна — Геноха (IgAВ/ПШГ) — наиболее распространенный СВ у детей с ежегодной частотой 13–20 : 100 000 детей младше 17 лет, причем 90% пациентов с IgAВ/ПШГ младше 10 лет [21]. Взрослые болеют реже (примерно 1,3 : 100 000 взрослых в год) [3]. Среди детей заболеванию IgAВ/ПШГ больше подвержены мальчики, у взрослых гендерная разница отсутствует [20, 47]. Как у детей, так и у взрослых к развитию IgAВ/ПШГ часто предрасполагают инфекции верхних дыхательных путей. Применение лекарственных средств и наличие злокачественных опухолей являются предрасполагающими факторами только у взрослых [31].
IgAВ/ПШГ рассматривают как васкулит, не требующий лечения, но у 20–30% больных детей развивается поражение почек. У взрослых IgAВ/ПШГ протекает намного тяжелее по причине более частого и тяжелого поражения почек. Пурпуру, преимущественно затрагивающую нижние конечности, диагностируют как у детей, так и у взрослых. У детей с IgAВ/ПШГ чаще проявляется суставная боль, хотя суставы одинаково задействованы у детей и взрослых в форме олигоартрита крупных суставов. Согласно большинству исследований, влияние на ЖКТ у детей и взрослых не различается, однако имеются сообщения о более высокой вероятности диареи у взрослых с IgAВ/ПШГ [50]. Для детей более характерны боли в животе как первичный симптом, что вызывает необходимость дифференциальной диагностики с инвагинацией кишечника с участием детских хирургов [27]. Поражение почек при IgAВ/ПШГ, определяющее долгосрочный прогноз, выявлено у 20–55% детей с IgAВ/ПШГ и у 49–83% взрослых, у последних с неблагоприятным исходом [47]. Более легкие поражения почек, включающие изолированную микрогематурию, более распространены у детей, в то время как тяжелые состояния, такие как нефротический синдром и почечная недостаточность, чаще встречаются у взрослых [20]. Хроническая почечная недостаточность при IgAВ/ПШГ зафиксирована у 8–68% взрослых пациентов [20], а у детей — только в 1,8–15% случаев [22].
Специфические лабораторные тесты для IgAВ/ПШГ отсутствуют; сравнение результатов лабораторных анализов детей и взрослых с IgAВ/ПШГ не выявило явных различий [20, 22].
Раннее проявление заболевания связано с поражением ЖКТ, позднее проявление и самая главная причина неблагоприятного исхода заключаются в поражении почек. У детей лечение IgAВ/ПШГ главным образом консервативное, поскольку проявления поражения почек у них обычно не требуют лечения. Артрит хорошо поддается терапии НПВП. При тяжелых поражениях кожи и ЖКТ назначают короткий курс кортикостероидов для приема внутрь. Как показали контролируемые исследования, кортикостероиды не предотвращают заболеваний почек [11].
Четкие рекомендации, касающиеся показаний к биопсии почек, отсутствуют; как правило, ее делают пациентам с острым нефротическим синдромом и/или с протеинурией нефротического генеза. Поскольку лечение пациентов с нефритом при IgAB/ПШГ не регламентировано, при тяжелом поражении почек применяют кортикостероиды в сочетании с такими иммуносупрессивными препаратами, как циклоспорин, азатиоприн или циклофосфамид [55].
Таким образом, IgAВ/ПШГ у детей является доброкачественным заболеванием, не требующим лечения. У взрослых IgAВ/ПШГ протекает в более тяжелой форме и представляет опасность в связи с частым поражением почек. Женщин особенно беспокоит ухудшение функции почек во время беременности [45].
Васкулит, ассоциированный с антинейтрофильными цитоплазматическими антителами
Васкулиты, ассоциированные с антинейтрофильными цитоплазматическими антителами (АНЦА), включают гранулематоз с полиангиитом (ГП, ранее — болезнь Вегенера), микроскопический полиангиит (МП), эозинофильный гранулематоз с полиангиитом (ЭГП, ранее — синдром Чарджа — Стросс) и заболевания отдельных органов, такие как почечный васкулит [7]. Дети редко болеют АНЦА-ассоциированным васкулитом, но он сопровождается тяжелыми проявлениями и характеризуется высокой смертностью, особенно при выявлении заболевания на поздней стадии [2]. Классификационные критерии ГП перечислены в таблице. Для детей с МП и ЭГП классификационные критерии отсутствуют — в этих случаях применяют общие определения (Чапел-Хилл, 2012).
С клинической точки зрения полезно рассматривать две формы ГП: преимущественно гранулематозную форму с главным образом локализованным заболеванием и хроническим течением и прогрессирующую, «истинную» острую форму васкулита мелких сосудов, характеризующуюся тяжелыми легочными кровотечениями и/или другими тяжелыми клиническими проявлениями [7]. Как у детей, так и у взрослых эти два крупных патогенных процесса могут протекать одновременно или последовательно. В исследовании Belostotsky и соавт. у 17 детей с ГП выявлена следующая частота системных нарушений: 87% — респираторные; 53% — почечные; 35% — оториноларингологические; 53% — костно-мышечные; 53% — глазные; 12% — неврологические; 53% — кожные [4]. По результатам исследования Cabral и соавт., проведенного с участием 65 детей с ГП, поражение почек развивалось в 75,4% случаев, диализ был необходим 7 пациентам из 65 (10,8%) и у одного ребенка присутствовало поражение почек последней стадии [9]. Приблизительно у 73,5% взрослых пациентов с ГП обнаруживают гистологические признаки гломерулонефрита [49].
При сравнении детской и взрослой когорт пациентов выделены различия в частоте некоторых клинических проявлений заболевания: у взрослых реже наблюдаются системные симптомы (повышенная температура тела, потеря массы тела), поражения лор-органов (ротовые/носовые язвы, хронический или рецидивирующий средний отит/нарушения слуха), поражения дыхательной системы (стеноз трахеи/эндобронхиальная обструкция, кровохарканье/альвеолярное кровотечение) и почек (гематурия или эритроцитарные цилиндры), а также выше вероятность возникновения кондуктивной тугоухости [6].
Для клинических проявлений МП типичны стремительно прогрессирующий гломерулонефрит и альвеолярное кровотечение, хотя фактически может быть затронута сосудистая система любых органов. У 75–80% взрослых выявляют антитела к миелопероксидазе нейтрофилов (pAНЦA/MПO-AНЦA). Патогенность MПO-AНЦA установлена на экспериментальных моделях, описана трансплацентарная передача антител к новорожденному [6]. Почечные формы МП описаны как для детей, так и для взрослых. Кроме миелопероксидазы, к антигенам АНЦА относят протеиназу 3, лактоферрин, эластазу, белок BPI и катепсин G. Диагностическим тестом служит метод непрямой иммунофлуоресценции с использованием нейтрофильных лейкоцитов. Хотя имеются классические описания поражения почек и легких при МП, клиницистам не следует забывать о возможных патологических изменениях других органов.
В недавнем обзоре 33 случаев ЭГП у детей у всех пациентов отмечены значительная степень эозинофилии периферической крови и бронхиальная астма. Более того, практически у всех пациентов представлены гистологические признаки эозинофилии и/или васкулита [55]. АНЦА при ЭГП обнаружены только у 25% детей и у 38% взрослых пациентов. В отличие от взрослых, у детей чаще наблюдают сердечно-легочные нарушения, в том числе кардиомиопатию (42% детей и 24% взрослых) и легочные инфильтраты (88% детей и 59% взрослых). У больных детского возраста выявлены более редкие поражения периферических нервов (39% детей и 69% взрослых) и более высокая летальность (19% детей и 5% взрослых). Следует отметить сложность дифференциальной диагностики у детей между ЭГП, первичными гиперэозинофильными синдромами и эозинофильной лейкемией; чрезвычайно важно установить точный диагноз, определяющий соответствующий терапевтический подход и результаты лечения.
Поскольку при АНЦА-ассоциированных васкулитах наиболее опасно поражение почек, то последовательная терапия у этих больных направлена на сохранение почечной функции. Лечение АНЦА-ассоциированных васкулитов у детей в широком смысле аналогично таковому у взрослых и включает кортикостероиды, циклофосфамид и плазмаферез по показаниям (особенно при воспалении легочных капилляров и/или быстро прогрессирующем легочно-почечном синдроме).
У взрослых и детей внутривенное введение циклофосфамида более предпочтительно, чем непрерывный прием циклофосфамида внутрь в связи с пониженной суммарной дозой и меньшей частотой нейтропенического синдрома у взрослых пациентов, хотя и без хорошей доказательной базы у детей [7]. Ацетилсалициловую кислоту в антиагрегантных дозах (по 1–5 мг/кг/сут, обычно по 37,5–75,0 мг/сут) применяют для уменьшения риска тромбозов, связанных с заболеванием [36]. Для достижения ремиссии пациентам с ограниченным ГП назначают метотрексат, но у детей с АНЦА-ассоциированным васкулитом его используют редко. При лечении гранулематоза Вегенера, особенно при поражении верхних дыхательных путей, часто применяют Ко-тримоксазол для профилактики оппортунистической инфекции и снижения частоты рецидивов инфекций верхних дыхательных путей. Рекомендации по длительности поддерживающей терапии основаны на клинических исследованиях у взрослых и предположении о высоком риске рецидива при прекращении терапии, поэтому последовательная поддерживающая терапия обычно длится несколько лет [39].
Для детей и взрослых разрабатывают новые иммуносупрессивные препараты и биологические иммуномодуляторы, так как применение циклофосфамида может способствовать присоединению инфекции к основному заболеванию, а также по причине того, что у 50% пациентов АНЦА-ассоциированный васкулит рецидивирует при снижении дозы или отмене препарата. В настоящее время проходят клинические испытания у детей лечения, включающего применение микофенолата мофетила и ритуксимаба [6]. Опубликованы данные об эффективности ритуксимаба при достижении ремиссии у взрослых с АНЦА-ассоциированным васкулитом [30], получены оптимистичные результаты предварительных исследований биологической терапии у детей [15].
Несмотря на неоспоримые терапевтические успехи, достигнутые за последние 10 лет, АНЦА-ассоциированный васкулит по-прежнему связан с высокой заболеваемостью и смертностью как среди детей, так и среди взрослых. Особую озабоченность вызывают необратимые повреждения органов, включающие почечную недостаточность, тяжелое поражение дыхательных путей и осложнения, связанные с терапией, например сепсис. К сожалению, распространены повреждения органов на предиагностической фазе заболевания, так как АНЦА-ассоциированный васкулит нетипичен для детей, врачи плохо о нем информированы и последовательная ранняя диагностика сильно запаздывает. В исследовании Belostotsky и соавт. летальность детей с ГП составила 12% за 17-летний период [4]. Среди детей с МП летальность во время долгосрочного наблюдения педиатрами варьировала от 0% до 14% [30]. Пятилетняя выживаемость взрослых без нарушений функции почек составляет 95%, пациентов с болезнями почек — 70% [38]. Летальность у детей с ЭГП достигает 19%, у взрослых — 5% [56].
Узелковый периартериит
Узелковый периартериит (УП) — первичный системный некротизирующий васкулит, преимущественно поражающий средние сосуды [14]. Частота заболеваемости у взрослых составляет 2–9 : 1 000 000 в год; вероятно, дети болеют реже, хотя эпидемиологических данных о частоте заболевания в детской популяции недостаточно. В некоторых частях света УП занимает третье место по распространенности среди СВ после IgAВ/ПШГ и болезни Кавасаки [41]. У взрослых большинство случаев заболевания приходится на возраст 25–50 лет; пик заболеваемости у детей — 9–10 лет [17]. Среди детей мальчики и девочки в равной степени подвержены заболеванию, тогда как среди взрослых УП чаще встречается у мужчин.
Существуют генетические факторы, предрасполагающие к развитию УП. В Турции изучена взаимосвязь УП у детей с мутациями в гене MEFV, связанном с семейной средиземноморской лихорадкой. Согласно исследованию, по крайней мере в некоторых группах, где обнаружены частые MEFV-мутации, восприимчивость к УП повышена. Недавно у пациентов с симптомами УП были описаны мутации в гене CECR1, кодирующем аденозиндезаминазу 2 (ADA2). Заболевание соответствует всем классификационным критериям УП, что свидетельствует о возможности моногенных УП [55]. Несмотря на ограниченное количество данных, дефицит ADA2 почти наверняка служит причиной заболевания некоторых пациентов с УП [40]. Другая недавно описанная аутовоспалительная болезнь с отчетливыми сосудистыми и легочными нарушениями, напоминающая УП, вызывается мутациями в гене, кодирующем белок-стимулятор интерферона (STING), и обозначается как STING-ассоциированная васкулопатия с проявлением заболевания в младенчестве [33].
Классификационные критерии для УП у детей представлены в таблице. Неспецифические системные проявления, такие как недомогание, лихорадка, потеря массы тела и нарушение функций опорно-двигательного аппарата (боли в суставах и мышцах), а также кожные проявления являются характерными чертами заболевания [17, 41]. У детей УП затрагивает различные системы, наиболее сильно поражая кожный покров, опорно-двигательный аппарат, почки и ЖКТ; сердечные, неврологические и респираторные симптомы встречаются реже. В многоцентровом исследовании, в котором участвовали 110 детей с УП (63 пациента — с системным УП), кожные поражения зарегистрированы у 92 человек, у 71,4% имелись миалгии [41]. В том же исследовании гипертензия описана в 43 случаях, у 11,1% пациентов возникли нарушения функции почек во время заболевания и у 1/3 пациентов наблюдали поражения ЦНС; нарушения сердечной и легочной функций проявились в 14% и 11% случаев соответственно. В многоцентровом ретроспективном исследовании с участием 348 взрослых пациентов с УП наиболее часто отмечали общие симптомы (93,1%): лихорадку (63,8%) и потерю массы тела (69,5%), а также миалгию (58,6%) и боли в суставах (48,9%), неврологические нарушения (79,0%), урологические и почечные проявления (50,6%), поражение кожи (49,7%) и желудочно-кишечные нарушения (37,9%) [14].
Как правило, результаты лабораторных анализов демонстрируют лейкоцитоз и тромбоцитоз наряду с повышенной концентрацией белков острой фазы воспаления. АНЦА обычно отсутствуют. Положительный результат серологического исследования на гепатит B для детей с УП нетипичен. Кроме того, если считать васкулит одним из проявлений инфекции гепатита В, то, в соответствии с номенклатурой 2012 г., его следует отнести к васкулитам с установленной этиологией.
Данные исследований почек указывают на поражение средних артерий до гломерулярных капилляров, в частности долевых и дуговых артерий. Соответственно, в клинической картине наблюдаются протеинурия различной степени и небольшая гематурия. Некротический васкулит этих артерий может привести к распространенным артериальным изменениям, наблюдаемым с помощью артериографии. Классическими выводами ангиографии являются аневризматические расширения, однако возможны и другие изменения артериального просвета, указывающие на васкулит: извитость, резкое прерывание, сужающийся стеноз сосудов меньшего порядка и отсечение периферического почечного артериального дерева. Такие изменения наблюдают и у детей, и у взрослых. Поскольку при УП обычно бывают затронуты артерии меньшего калибра, то «золотым стандартом» радиологической диагностики более признана цифровая субтракционная артериография с обычным катетером, чем недавно введенный метод неинвазивной ангиографии.
Терапия для достижения ремиссии при УП обычно включает применение высоких доз кортикостероидов и циклофосфамида; по достижении ремиссии часто проводят поддерживающую терапию с низкими дозами кортикостероидов и азатиоприна. Недавно описано успешное лечение в рефрактерных случаях биологическими агентами, такими как инфликсимаб или ритуксимаб [10]. Тем не менее лечение УП у детей основано главным образом на данных клинических исследований с участием взрослых пациентов. Рандомизированных контролируемых исследований эффективности терапии УП у детей не проводили. В тяжелых случаях может применяться плазмаферез.
Результаты лечения УП у детей лучше, чем у взрослых пациентов: у них возможно достижение постоянной ремиссии и уровень смертности не превышает 1–4% [17, 40]. Показатель смертности у 349 взрослых пациентов с УП, зарегистрированных в базе Французской группы по изучению васкулитов, составил 24,6% [23]. В недавнем рандомизированном контролируемом исследовании, включавшем 118 взрослых пациентов с МП и УП без неблагоприятных прогностических факторов, 5- и 8-летняя общая выживаемость составила 93% и 86% соответственно без различий между больными МП и УП [45].
Неблагоприятные прогностические факторы, связанные с повышенным риском 5-летней смертности, у взрослых с УП включают возраст старше 65 лет, кардиологические симптомы, почечную недостаточность и поражение ЖКТ. Наихудший результат в когорте из 52 детей с УП ассоциировался с поражениями почек и нервной системы [19]; в другом недавнем педиатрическом исследовании тяжелые желудочно-кишечные заболевания были связаны с повышенным риском рецидива системного УП [17].
У детей встречается особая форма заболевания — так называемый кожный УП, для которого характерны кожный васкулит и минимальные системные поражения. Большинству таких пациентов достаточно приема НПВП, некоторым показано лечение кортикостероидами. Однако этим больным необходимо постоянное наблюдение врача для контроля возникновения системных симптомов [14].
Болезнь Кавасаки
Болезнь Кавасаки (БК) — васкулитный синдром, преимущественно поражающий средние и мелкие артерии. Специальной терапии не требует. БК распространена во всем мире, характеризуется сезонностью и случайными эпидемиями. Заболеванию более подвержены пациенты мужского пола, а также дети стран Азии. Так, в настоящее время частота возникновения БК в Великобритании составляет 8 : 100 000 детей, а заболеваемость среди японских детей намного выше — 360 : 100 000 детей младше 5 лет. Описано несколько случаев заболевания БК взрослых, но эта болезнь признана преимущественно детским СВ [18]. Этиология БК неизвестна. Выраженная сезонность и кластеризация случаев БК ведут к попыткам обнаружения инфекционных агентов как основной причины ее возникновения, однако пока ни один агент последовательно не определен [18].
Для установления диагноза БК необходимо присутствие четырех из шести клинических проявлений, перечисленных в таблице. Другие симптомы включают артрит, асептический менингит, пневмонию, увеит, гастроэнтерит, меатит, дизурию, отит и реактивацию рубца БЦЖ [23]. У младенцев нередко наблюдают меньше классических признаков БК. Результаты лабораторных исследований неспецифичны. При поражении коронарных сосудов на ЭКГ выявляют признаки ишемии миокарда, при допплерографическом исследовании — аневризмы.
Терапия включает внутривенное введение иммуноглобулинов в курсовой дозе 2 г/кг за 12 часов, а в случаях высокого риска — дополнительное введение кортикостероидов и ацетилсалициловой кислоты для первичной терапии [18]. После разрешения лихорадки поражение сердца маловероятно, частота рецидивов составляет 1–3%.
АРТЕРИИТ ТАКАЯСУ
Артериит Такаясу (АТ) — единственный васкулит крупных сосудов, указанный в текущей педиатрической классификации, затрагивающий аорту и ее основные ветви. АТ распространен по всему миру; по опубликованным данным, частота заболевания у европейцев составляет 1,2–2,6 : 1 000 000 в год и в 100 раз выше в Восточной Азии [53]. Дети редко страдают АТ, но заболеть могут даже младенцы [48].
Клиническая диагностика АТ представляет проблему для клиницистов. Считается, что у 1/3 детей представлена фиброзная/стенозирующая фаза заболевания. Ошибочно полагать, что эта фаза является «неактивной» стадией заболевания, так как прогрессирующая стенозирующая болезнь может быть следствием активного воспаления при отсутствии таких лабораторных маркеров системного воспаления, как повышенная концентрация C-реактивного белка или повышенная СОЭ. К сожалению, задержка диагностики у детей случается очень часто и способствует ухудшению результатов лечения [8]. Наиболее характерные признаки болезни у детей и взрослых сходны и включают артериальную гипертензию и/или ее последствия, но полный клинический спектр симптомов АТ у детей может отличаться от симптоматики взрослых. Самым частым проявлением у детей является артериальная гипертензия (82%), за которой следуют головные боли (31%), лихорадка (29%), одышка (23%) и потеря массы тела (22%). Нарушения опорно-двигательного аппарата возникают примерно у 14–65% детей с АТ. В отличие от детей, у взрослых редко проявляется артрит или артралгия. Звук при аускультации (48%) и хромота (27%) чаще бывают у взрослых пациентов с АТ [45]. Поражения глаз у детей также редки.
При подозрении на АТ у детей или у взрослых МРТ и магнитно-резонансная ангиография (МРА), а также КТ-ангиография или комбинация этих методов помогают точно диагностировать АТ, контролировать активность заболевания; МРА и КТ-ангиография дают возможность также получить изображение поперечного сечения артериальной стенки, позволяющее определить ее толщину и выявить интрамуральное воспаление. Кроме того, МРТ сердца все чаще применяют для поиска пораженных клапанов и/или миокардита. Наконец, позитронно-эмиссионная томография с 18F-фтордезоксиглюкозой (18F-ФДГ-ПЭТ) в сочетании с КТ-ангиографией или МРА информативна для определения метаболической активности артериальной стенки с подробной люминографией и, таким образом, предоставляет информацию о течении болезни и ее анатомических особенностях [35]. Однако чувствительность и специфичность этих методов для оценки активности АТ не определены.
У детей гистологическое исследование обычно выявляет умеренное лимфоцитарное воспаление с некоторой неоваскуляризацией, но без гранулематоза, в отличие от взрослых, у которых в начале АТ доминирует гранулематоз. Возможно, отсутствие гранулематоза у детей объясняется небольшой длительностью заболевания к моменту забора материала [25].
Оценка активности АТ затруднена, особенно у детей. Результаты определения концентрации белков острой фазы недостаточно чувствительны, большинство клинических проявлений неспецифичны, и поражения сосудов коварно прогрессируют. Для взрослых больных разработаны две шкалы оценки активности и степени тяжести АТ: ITAS-2010 и DEI.Тak [1, 37]. Эти шкалы созданы на основе шкалы активности васкулитов Бирмингема, но с особым акцентом на сердечно-сосудистых проявлениях, преобладающих при АТ. В настоящее время продолжается работа по адаптации указанных шкал оценки тяжести и активности АТ для детей, так как некоторые показатели зависят от возраста пациента.
Кортикостероиды являются основой лечения АТ. Метотрексат, азатиоприн и циклофосфамид применяют и у детей. Опыт применения кортикостероидов и циклофосфамида в лечении 6 детей с АТ подтвердил их эффективность и безопасность при терапии АТ у больных детского возраста [43]. Полезна и анти-ФНО терапия [41]. Обнадеживают результаты анти-IL-6 терапии (применения тоцилизумаба) у взрослых с АТ, а в некоторых случаях — и у детей [34]. Для облегчения ишемии органов и артериальной гипертензии в результате сосудистого стеноза применяют хирургическое вмешательство. Однако перед выполнением процедуры реваскуляризации или другой сосудистой операции предпочтительно по возможности контролировать васкулит, поскольку вмешательство на фоне активного заболевания менее эффективно.
Пятилетняя смертность детей при АТ составляет 35%. Прогноз зависит от степени артериального поражения, возраста пациента и тяжести артериальной гипертензии. У взрослых с АТ 5-летняя выживаемость достигает 94% [44].
ЗАКЛЮЧЕНИЕ
Данные контролируемых клинических исследований, необходимые для формирования руководства по принятию терапевтических решений по системным васкулитам (СВ), у детей отсутствуют, за исключением болезни Кавасаки [18]. Клинические исследования васкулитов у больных детского возраста сложны по многим причинам, включающим небольшое число пациентов, отсутствие адекватных мер для контроля исхода заболевания и определения результатов лечения. До недавнего времени четкие критерии классификации васкулитов у детей отсутствовали. Несколько успешных клинических исследований, проведенных среди взрослых пациентов с васкулитами, особенно с заболеваниями, ассоциированными с антинейтрофильными цитоплазматическими антителами (АНЦА), легли в основу разработки программ лечения детей [6, 28]. Внедрение закона «О лучших фармацевтических препаратах для детей» в США и законодательства по использованию лекарств для детей (Педиатрических правил) в Европейском Союзе позволяет исправить ситуацию, так же как и недавняя валидизация шкалы активности васкулитов у детей для оценки результатов терапии [15].
Серьезной проблемой при рассмотрении возможности клинических исследований при СВ у детей является достижение достаточного объема материала для переноса данных в клиническую практику, когда ожидаемые размеры выборки малы. Исторически это служило основным препятствием для изучения редких аутоиммунных заболеваний у детей и почти наверняка объясняет причину отсутствия клинических исследований узелкового периартериита (УП) и артериита Такаясу. В настоящее время дизайн клинических исследований редких заболеваний, включающий байесовскую методологию, стали использовать в клинических исследованиях у детей, где недоступны размеры выборки, необходимые для традиционных исследований. Байесовский подход начинается с формальной характеристики предварительного мнения, которое затем обновляется с помощью собранных данных с использованием теоремы Байеса для формирования апостериорного (эмпирического) мнения и его переноса в клиническую практику [32]. Открытое рандомизированное клиническое исследование MYPAN по сравнению эффективности мофетила микофенолата и циклофосфамида при лечении УП у детей — первое клиническое исследование васкулитов у детей, которое адаптирует дизайн клинических испытаний Байеса для преодоления барьера малых размеров выборки при таких редких заболеваниях [24]. Свою лепту в процесс изучения васкулитов вносит постоянное клиническое субтипирование. Традиционное разделение AНЦA-ассоциированных васкулитов на эозинофильный гранулематоз с полиангиитом, гранулематоз с полиангиитом (ГП) и микроскопический полиангиит (МП), основанное на клиническом фенотипе, недавно оспорено на основании клинических наблюдений, данных эпидемиологии и генетики. Кластерный анализ клинических характеристик новых пациентов с ГП и МП выявил пять разных фенотипов с различными исходами: ренальный AНЦA-ассоциированный васкулит с иммунными комплексами к протеиназе 3 нейтрофилов (ПР3-AНЦA); ренальный AНЦA-ассоциированный васкулит без ПР3-AНЦA; неренальный AНЦA-ассоциированный васкулит; сердечно-сосудистый AНЦA-ассоциированный васкулит; желудочно-кишечный AНЦA-ассоциированный васкулит. Особенности проявления заболевания варьируют от популяции к популяции, и для ГП более характерна цикличность, не наблюдаемая при МП. Заметна значительная разница между исходами ГП и МП. В присутствии ПР3-AНЦA риск рецидива васкулита выше. Как показало Европейское молекулярно-генетическое исследование AНЦA-ассоциированных васкулитов, заболевание, ассоциированное с ПР3-AНЦA, связано с генами HLA-DP, SERPINA1 и PRTN3, в то время как васкулит, ассоциированный с АНЦА к миелопероксидазе нейтрофилов, связан с HLA-DQ-фенотипом. SERPINA1 кодирует α1-антитрипсин — сериновую протеазу, которая имеет ПР3 в качестве одной из мишеней. PRTN3 кодирует протеиназу 3. Таким образом, иммунный ответ против аутоантигена ПР3 является главной этиологической особенностью ПР3-AНЦA-ассоциированного васкулита. С учетом этих данных, возможно, необходима новая классификация, учитывающая ранее неизвестные характеристики АНЦА [54].
Таким образом, исследования васкулитов у детей быстро продвигаются вперед, но есть еще много насущных проблем. Для лучшего понимания этиопатогенеза васкулитов и разработки таргетной терапии необходимо многоцентровое сотрудничество.








