ВВЕДЕНИЕ
Эндометриоз — это патологический процесс, при котором определяется наличие ткани, по морфологическим и функциональным свойствам подобной эндометрию, вне полости матки[1]. Эндометриоз встречается у 10–15% женщин репродуктивного возраста и является ведущей причиной дисменореи, хронической тазовой боли, диспареунии и бесплодия[1].
Достижение благоприятных гестационных и перинатальных исходов у женщин с эндометриозом является крайне важной задачей. За последние десятилетия проведено множество исследований по изучению связи между эндометриозом и неблагоприятными исходами беременности для матери и плода: выкидышем, преждевременными родами (ПР), преэклампсией (ПЭ), аномалиями расположения плаценты, фетоплацентарной недостаточностью, задержкой роста плода, низкой массой тела при рождении и др.[2]. Результаты этих работ противоречивы: в одних из них показано негативное влияние эндометриоза на исход беременности, в других нет. Получение разных данных, скорее всего, связано с тем, что авторы включали в исследования пациенток с различным анамнезом: забеременевших с помощью ВРТ и самопроизвольно; с наличием хирургического лечения и гормональной терапии и их отсутствием.
Отдельные авторы изучали биологические механизмы, которые, вероятно, способствуют нарушению физиологического течения беременности у женщин с эндометриозом (табл. 1, рис.). По полученным данным, выкидыши, ПР, плацентарные нарушения, ПЭ могут развиваться у пациенток с эндометриозом из-за иммуноэндокринных нарушений в эндометрии, а также в микросреде малого таза вследствие увеличения образования цитокинов, сосудистого эндотелиального фактора роста, простагландинов, ведущего к нарушению рецептивности эндометрия и сократимости миометрия, эндотелиальной дисфункции, нарушению ремоделирования спиральных артерий, аномальной плацентации. Однако точные механизмы возникновения акушерских осложнений у пациенток с эндометриозом до сих пор неясны.
Таблица 1
Предполагаемые патофизиологические механизмы развития акушерских осложнений у пациенток с эндометриозом
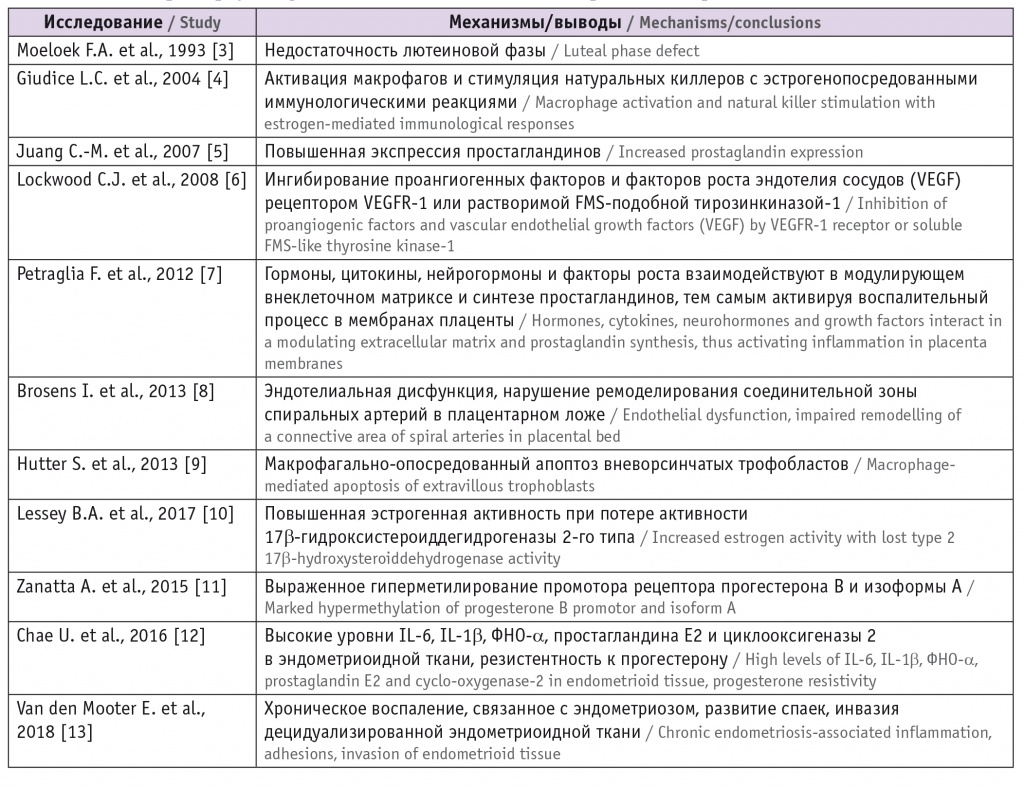
Рис. Эндометриоз, нарушение фертильности и акушерские осложнения: патофизиологические механизмы
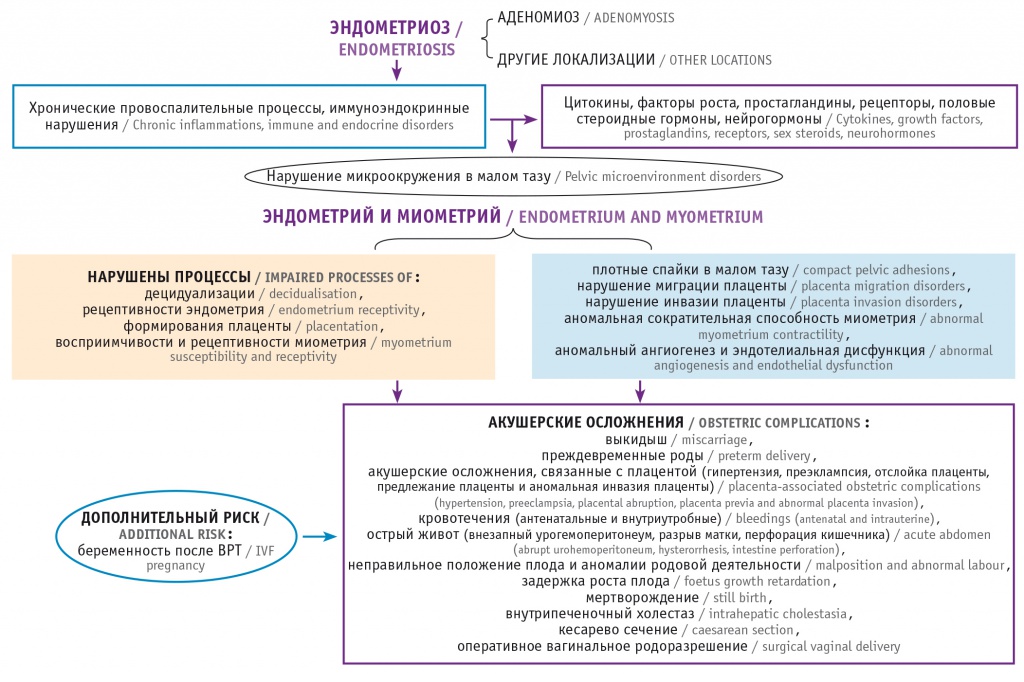
В свете вышеизложенного целью обзора явилось изучение влияния эндометриоза на исходы беременности (с учетом стадии и локализации процесса, методов лечения, способа наступления беременности — спонтанного или в результате применения ВРТ), а также предложение методов профилактики акушерских осложнений у беременных с эндометриозом.
ВЛИЯНИЕ ЭНДОМЕТРИОЗА НА ВЫКИДЫШ И ПРЕЖДЕВРЕМЕННЫЕ РОДЫ
Выкидышем, или спонтанным абортом, называют самопроизвольное прерывание беременности в период до 22-й недели гестации, а ПР — роды, наступившие в сроки от 22 недель до 36 недель и 6 дней.
Основными причинами выкидыша являются генетические факторы, инфекции, эндокринные нарушения (например, недостаточность лютеиновой фазы), анатомические дефекты матки (например, мюллеровские аномалии) и тромбофилии (в частности, антифосфолипидный синдром). У пациенток с эндометриозом частота выкидышей в различных исследованиях варьируется от 30 до 50% и они чаще наблюдаются в I триместре беременности[14].
Ретроспективные исследования не показывают четкой связи между эндометриозом и выкидышем[15–17]. Противоречивость результатов можно объяснить исследованием групп, неоднородных по стадии и локализации патологического процесса, с наличием или отсутствием хирургического лечения до проведения программ ВРТ и др.[18, 19].
Так, согласно P. Yang и соавт., наличие эндометриомы не увеличивает риск выкидыша независимо от ее размера (≥ 3 или < 3 см)[16]. L. Benaglia и соавт. пришли к аналогичным выводам: в их работе частота живорождений у женщин с эндометриомами и без них после проведения ЭКО статистически значимо не различалась (78% против 83%; p = 0,39)[17].
Напротив, A.S. Kohl Schwartz и соавт. продемонстрировали, что эндометриоз легкой степени (поверхностные очаги) в значительной мере связан с воспалительным процессом, который ведет к нарушению фолликулогенеза, оплодотворения и имплантации, повышающему риск выкидыша[19]. По данным P. Santulli и соавт., частота выкидышей при поверхностном эндометриозе также была статистически значимо выше, чем при глубоком инфильтративном эндометриозе и у пациенток без эндометриоза: 37,9% (95%-й ДИ: 25,4–50,5) против 27,2% (95%-й ДИ: 20,4–34,0) и 19,4% (95%-й ДИ: 16,1–22,7) соответственно (p < 0,01)[14]. Авторы полагают, что это можно объяснить как более активным воспалительным процессом при поверхностном эндометриозе по сравнению с фиброзными включениями при глубоком инфильтративном эндометриозе, так и низким процентом наступления беременности у пациенток с тяжелой формой эндометриоза[14].
Показано, что на молекулярном уровне эндометриоз вызывает гормональные, клеточные и иммунологические нарушения в эндометрии, негативно воздействуя на децидуализацию, плацентацию и развитие эмбриона[10]. Опубликованы данные, согласно которым высокая частота выкидышей при эндометриозе связана в основном с тремя факторами: 1) повышением сократительной активности миометрия вследствие увеличения образования простагландинов F2-альфа в очагах эндометриоза[7]; 2) недостаточностью лютеиновой фазы цикла[3]; 3) изменением гуморального и клеточно-опосредованного иммунного ответа, что может повлиять на восприимчивость эндометрия к имплантации эмбриона[10].
Многие авторы демонстрируют высокий риск развития ПР при эндометриозе (табл. 2)[2, 5, 20–24].
Таблица 2
Исследования по изучению риска выкидышей и преждевременных родов у пациенток с эндометриозом
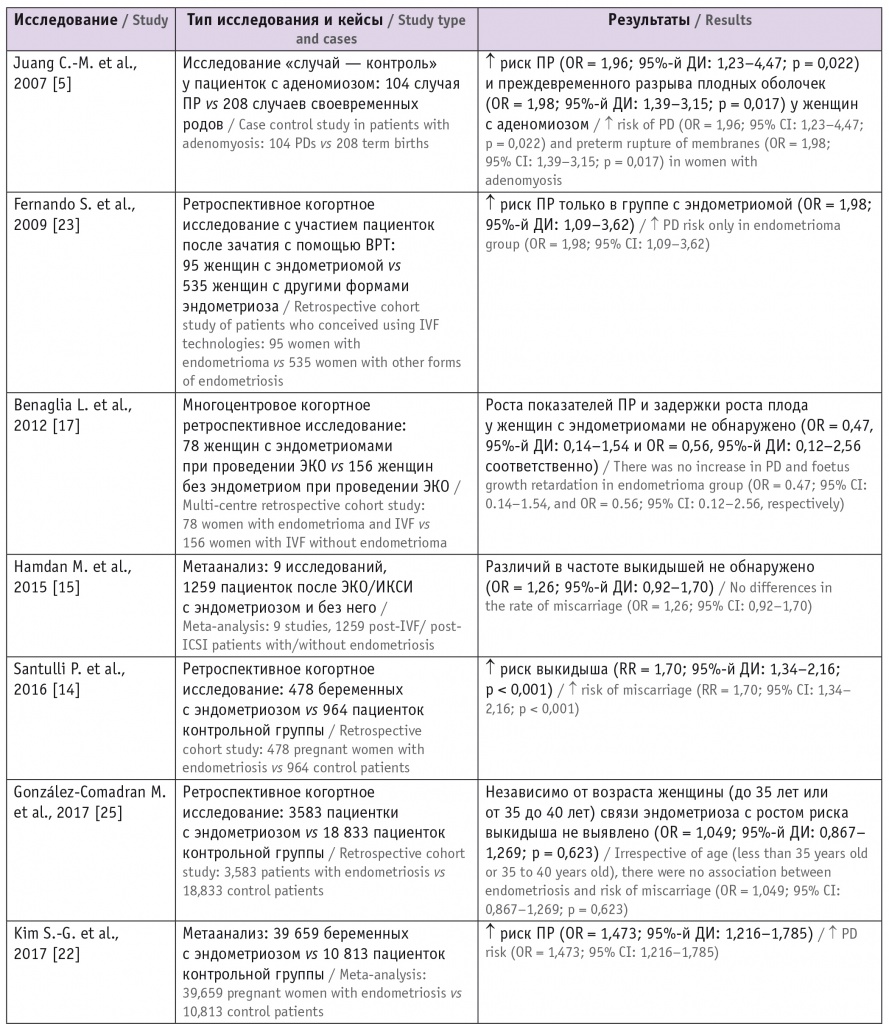

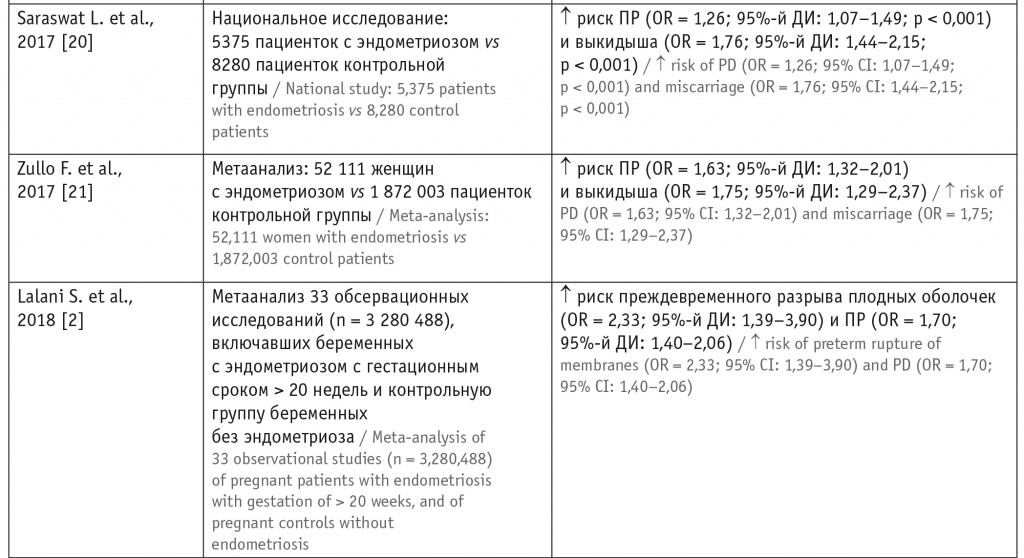

Примечание. ДИ — доверительный интервал; ПР — преждевременные роды; OR — отношение шансов; RR — относительный риск.
Согласно некоторым исследованиям, женщины с эндометриозом подвержены риску развития ПР при первой беременности примерно в 1,5 раза чаще, чем при повторных[22, 27], что свидетельствует об иммунологических и гормональных изменениях у пациенток с эндометриозом во время беременности и их защитной роли в отношении повторных беременностей[22].
К числу факторов риска ПР у пациенток с эндометриозом большинство авторов относит применение ВРТ с целью повышения вероятности наступления беременности. Результаты ретроспективного исследования S. Fernando и соавт. показали, что у женщин с эндометриомой после проведения ЭКО частота ПР и задержки роста плода в 2 раза выше, чем в контрольной группе случайным образом отобранных женщин, хотя в отношении других локализаций эндометриоза подобной связи не выявлено[23]. Причины таких исходов беременности авторы видят в патологии эндометрия, наблюдаемой у женщин с эндометриомами, его децидуализированной строме и патологической плацентации.
Однако, по данным некоторых исследователей, ЭКО само по себе является фактором риска развития ПР. Так, A.J. Fechner и соавт. продемонстрировали, что показатели лютеина и релаксина в сыворотке крови матери прямо коррелируют с вероятностью возникновения ПР при одноплодной беременности[28]. Это свидетельствует о том, что риск ПР может быть также связан со стимуляцией овуляции и избытком стероидов при проведении ЭКО.
С другой стороны, существуют исследования, в которых эндометриоз не оказал негативного влияния на исходы беременности и сроки родов после проведения ЭКО. Так, L. Benaglia и соавт. пришли к выводу, что после ЭКО частота возникновения ПР и рождения недоношенных детей у женщин с эндометриозом и без него сходна[17]. Аналогичные результаты получены в ходе общенационального исследования в Швеции: риск ПР у пациенток с эндометриозом после ВРТ составил 1,24, а у женщин без ВРТ — 1,37[29].
Некоторые авторы изучали риск ПР у женщин с аденомиозом. Y.J. Shin и соавт. в ретроспективном исследовании показали, что пациентки с аденомиозом имеют более высокие проценты ПР и рождения детей с низкой массой тела при рождении, чем женщины без аденомиоза[24]. Кроме того, авторы выявили, что у беременных женщин с аденомиозом риск ПР после ВРТ значительно выше, чем у таковых при самопроизвольно наступившей беременности. Результаты этого исследования согласуются с данными более ранней работы, которые показали, что у женщин с аденомиозом не только в 1,84 раза выше риск ПР, но и в 1,98 раза выше риск преждевременного разрыва плодных оболочек[5].
Высказано предположение, что связь между аденомиозом и ПР может быть объяснена хориоамнионитом или системным воспалением, наблюдаемым у таких пациенток[5]. В другом исследовании сообщается об увеличении внутриматочного давления у пациенток с аденомиозом, что также может приводить к возникновению ПР[30]. Действительно, увеличение сокращения миометрия и повышение внутриматочного давления часто предшествуют ПР.
C.-M. Juang и соавт. считают, что повышенная экспрессия простагландинов, обнаруженная у пациенток с аденомиозом, связана с преждевременным разрывом плодных оболочек, поскольку эти гормоноподобные вещества вызывают маточные сокращения и деградацию коллагена плодных оболочек[5].
Однако для подтверждения всего вышеизложенного необходимы дальнейшие исследования патофизиологических механизмов.
Точный механизм возникновения ПР при наружном генитальном эндометриозе до сих пор неизвестен. F. Petraglia и соавт. предположили, что ПР могут быть связаны с половыми стероидными гормонами, нейрогормонами, цитокинами и факторами роста[7]. По мнению этих исследователей, иммуноэндокринные нарушения способствуют процессу ремоделирования эндометрия и вызывают изменения в базальной мембране, а также запускают ангиогенез и воспалительные процессы. В свою очередь, воспалительные процессы могут влиять на взаимодействие децидуальной оболочки с трофобластом и способствовать развитию ПР. Кроме того, высказано предположение, что подавление синтеза прогестеронового рецептора B связано с клинически наблюдаемой резистентностью к прогестерону у пациенток с эндометриозом, что также может являться причиной развития у них выкидыша и ПР[11]. К тому же показано, что аномальная экспрессия интегринов и генов HOX, которая отмечается у пациенток с эндометриозом, может влиять на восприимчивость эндометрия и последующую плацентацию[10]. Однако на сегодняшний день исследований, которые могли бы подтвердить или опровергнуть эти предположения, не существует.
Некоторые авторы отмечают, что хирургическое лечение эндометриоза с последующей гормональной терапией может улучшить исходы беременности[31]. Это объясняется тем, что лапароскопическое лечение не только дает преимущество в принятии решения о дальнейшей тактике ведения пациенток с эндометриозом, но и создает благоприятную среду в малом тазу, что значительно улучшает фертильность и исходы беременности у них[31]. Хотя в руководстве Европейского общества репродукции человека и эмбриологии (англ. European Society of Human Reproduction and Embryology, ESHRE) нет доказательств в пользу хирургического удаления глубокого инфильтративного эндометриоза до проведения процедур ВРT с целью улучшения репродуктивных исходов[32], натяжение плотных спаек из-за роста беременной матки в области малого таза и брюшной полости может стать триггером возникновения маточных сокращений, что может спровоцировать ПР[33]. Поэтому, на наш взгляд, в случае наличия плотных фиброзных спаек хирургическое лечение должно быть обязательной составляющей прегравидарной подготовки у пациенток с эндометриозом.
Другим популярным подходом к оптимизации результатов ВРТ у бесплодных женщин с эндометриозом является продолжительная (на протяжении 3–6 месяцев) супрессивная гормональная терапия агонистами ГнРГ. Показано, что это увеличивает вероятность наступления спонтанной беременности в 4 раза[34]. Есть также сведения, что сверхдлинный протокол с агонистами ГнРГ (в течение 3 месяцев до ЭКО) помогает уменьшить вредное воздействие цитотоксических цитокинов и окислительного стресса у бесплодных женщин с эндометриозом, тем самым улучшая репродуктивные исходы[35].
ВЛИЯНИЕ ЭНДОМЕТРИОЗА НА ГИПЕРТЕНЗИВНЫЕ РАССТРОЙСТВА ВО ВРЕМЯ БЕРЕМЕННОСТИ, ПРЕЭКЛАМПСИЮ И ПЛАЦЕНТАРНЫЕ НАРУШЕНИЯ
Современные данные о влиянии эндометриоза на ПЭ противоречивы. Многие авторы сходятся во мнении, что женщины с эндометриозом подвержены более высокому риску развития гипертензивных расстройств во время беременности (ГРВБ) и ПЭ (табл. 3)[36–38]. Это подтверждено результатами метаанализа (n = 3 280 488), проведенного в 2018 г. S. Lalani и соавт., где продемонстрировано, что женщины с эндометриозом по сравнению с женщинами без эндометриоза имеют более высокий риск развития как ПЭ, так и ГРВБ[2]. Кроме того, авторы данного метаанализа не выявили повышения риска развития ГРВБ и ПЭ под влиянием ВРТ: для женщин, которые забеременели спонтанно, отношение шансов ГРВБ и ПЭ составило 1,12 и 1,21, в то время как для женщин, забеременевших после ВРТ, — 0,79 и 0,89 соответственно.
Таблица 3
Исследования плацентарных нарушений у беременных с эндометриозом
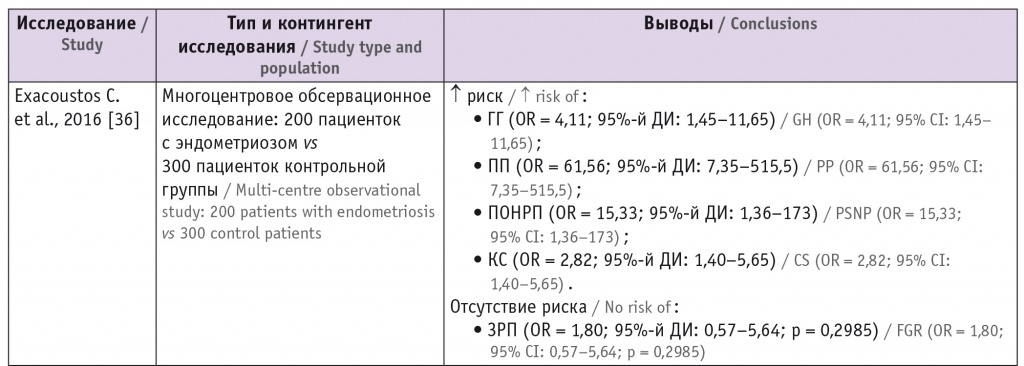
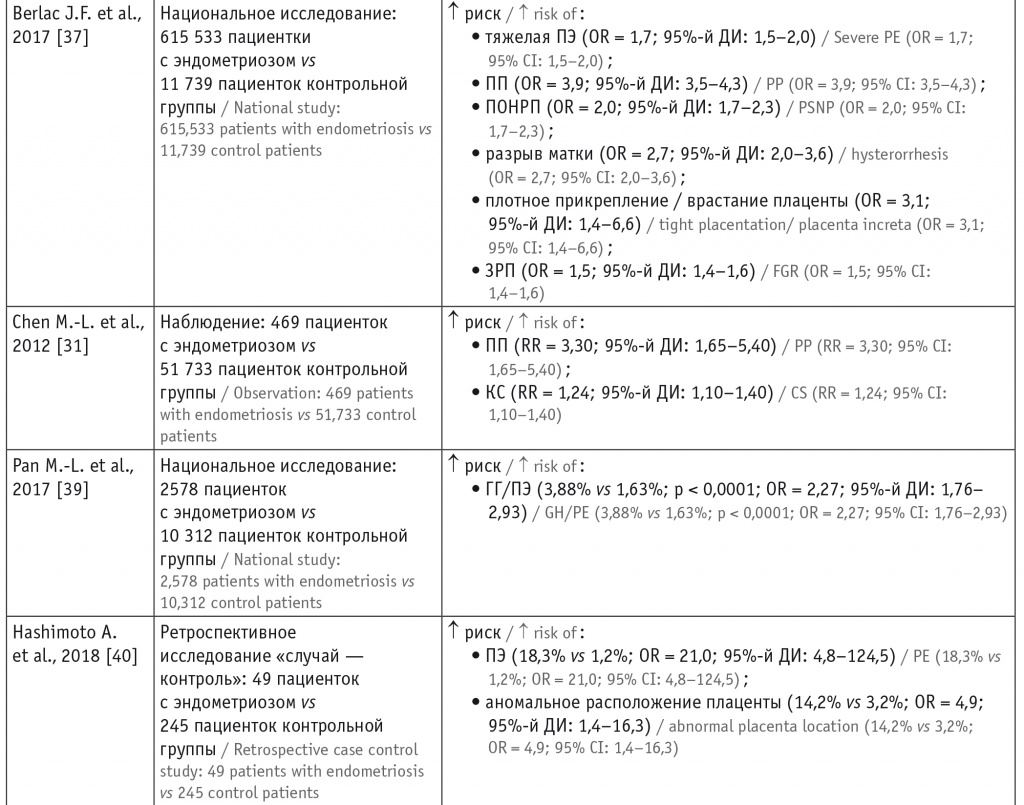
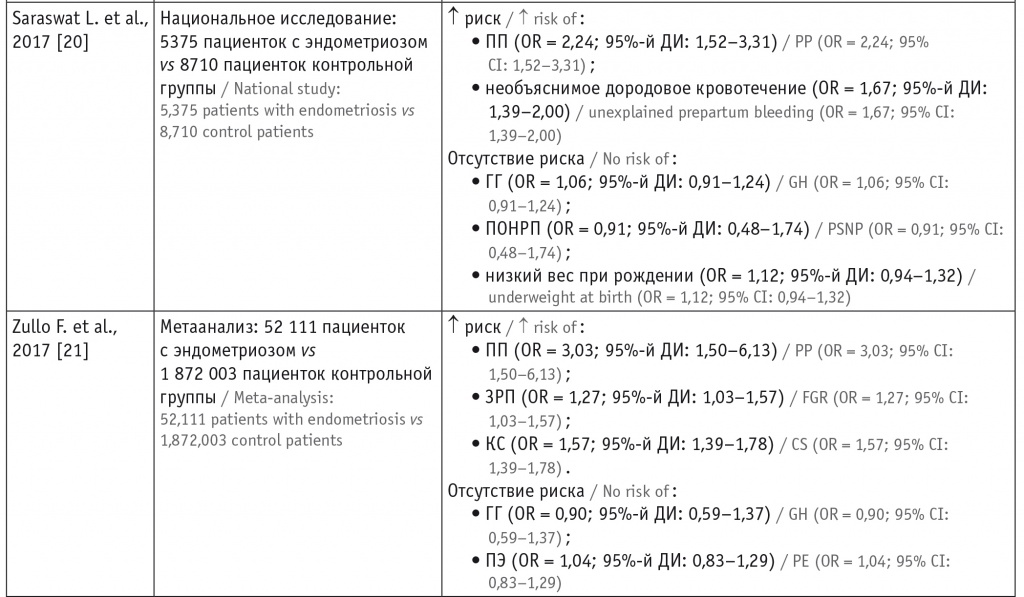
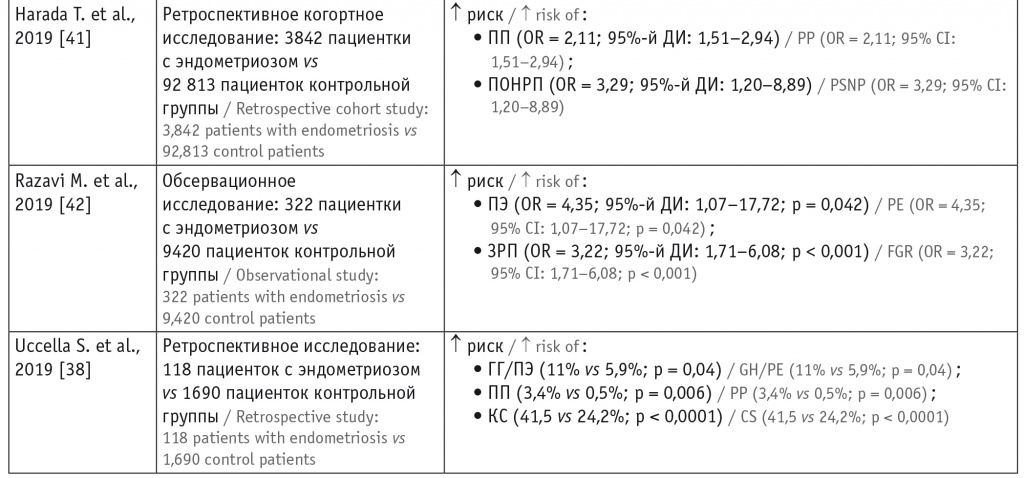
Примечание. ГГ — гестационная гипертензия; ЗРП — задержка роста плода; КС — кесарево сечение; ПОНРП — преждевременная отслойка нормально расположенной плаценты; ПП — предлежание плаценты; ПЭ — преэклампсия; OR — отношение шансов; RR — относительный риск.
В то же время имеются исследования, которые не выявили связи между эндометриозом и повышенным риском развития ГРВБ и ПЭ [21, 43]. Систематический обзор и метаанализ, проведенные F.R. Pérez-López и соавт. в 2018 г. с участием 39 816 беременных женщин с эндометриозом и 2 831 065 — без эндометриоза, показали, что пациентки с эндометриозом не имеют более высокого риска развития ПЭ, эклампсии и HELLP-синдрома по сравнению с контролем[43]. Кроме того, риск ПЭ, эклампсии и HELLP-синдрома в этой работе оказался одинаковым у пациенток с эндометриозом после спонтанного зачатия и после ВРТ.
Некоторые авторы изучали частоту возникновения ПЭ в зависимости от локализации эндометриоза. В японском проспективном когортном исследовании продемонстрировано, что женщины с аденомиозом имеют более высокий риск развития ПЭ средней степени тяжести по сравнению с женщинами без эндометриоза — 4,6% против 2,3%, в то время как у женщин с другими локализациями эндометриоза и без него значительного различия не выявлено — 2,6% против 2,3%[41]. Однако, по данным этого исследования, локализация эндометриоза не влияла на риск возникновения ПЭ тяжелой степени: 0,9% у женщин с аденомиозом и 1,2% у женщин с эндометриозом других локализаций против 1,0% в группе без эндометриоза.
Во многих исследованиях показана высокая распространенность предлежания плаценты (ПП) и приращения/прорастания плаценты у женщин с эндометриозом (см. табл. 3)[20, 21, 36–38, 41]. Авторы работы, выполненной в Японии, пришли к выводу, что риск ПП и отслойки плаценты (ОП) у женщин с эндометриозом в 3,6 и 1,3 раза выше, чем при его отсутствии[41]. Кроме того, по результатам данного исследования, риск ПП и ОП у женщин с аденомиозом был в 2,5 и 3 раза выше, чем у женщин без аденомиоза. Некоторые исследователи также обнаружили, что риск ПП при ретроцервикальном эндометриозе в несколько раз превышает таковой при эндометриозе других локализаций[38]. У пациенток после хирургического лечения эндометриоза констатирован более высокий риск ПП, что, по мнению авторов, может быть связано с более тяжелой стадией заболевания[44].
В 2018 г. H. Jeon и соавт. провели метаанализ с целью изучения риска ПП у женщин с эндометриозом, забеременевших с помощью ВРТ: из 8161 женщины 1640 страдали эндометриозом и подвергались ВРТ, у 6521 женщины эндометриоз отсутствовал[45]. Метаанализ показал, что пациентки с эндометриозом имеют повышенный риск ПП, наиболее высокий риск отмечен у тех из них, кто подвергался ВРТ.
Механизм, лежащий в основе повышенного риска ПП у женщин с эндометриозом, подвергшихся ВРТ, до сих пор неясен[46]. Согласно M. Dueholm, развитие ПП у таких пациенток может быть связано с нарушением имплантации эмбриона после ЭКО и переноса эмбриона[47]. J. Cha и соавт. предположили, что при эндометриозе причиной ПП может быть неадекватное сокращение матки в субэндометриальном слое в процессе имплантации эмбриона[48], тогда как M. Miura и соавт. высказали мнение, что плотные фиброзные спайки в области малого таза могут препятствовать миграции плаценты из области внутреннего зева[44]. Показано, что механически вызванные аномальные сокращения матки во время процедур ВРТ также могут привести к имплантации эмбриона в нижний маточный сегмент и тем самым повысить риск ПП[47]. Хотя, с другой стороны, в метаанализе S. Lalani и соавт. риск ПП у женщин после ВРТ был в 2 раза ниже, чем у женщин, которые зачали самостоятельно[2]. Эти же авторы продемонстрировали отсутствие связи между эндометриозом и высокой частотой ОП у пациенток, подвергшихся ВРТ.
M.G. Porpora и соавт. в исследовании, включавшем пациенток с эндометриозом (n = 145) и без него (n = 280), не обнаружили существенной разницы между ними в частоте возникновения ПП, ОП и врастания плаценты: 3% против 1%, 1% против 0% и 0% против 0,4% соответственно[49]. Однако данные авторы справедливо отметили, что их исследование имеет некоторые ограничения из-за небольшой выборки пациенток с аденомиозом.
Учитывая вышеизложенное, хроническое воспаление, вызываемое эндометриозом (особенно аденомиозом), может быть центральным патофизиологическим механизмом в развитии ПЭ и аномальной плацентации. Только адекватная имплантация и волны цитотрофобластической инвазии (на сроках 6–8 и 18–20 недель беременности) могут обеспечить полноценную гестационную перестройку спиральных артерий, плацентацию, маточно-плацентарную перфузию и рост плода. Неудачная имплантация у пациенток с эндометриозом связана с аномалиями расположения плаценты, а патологическая плацентация способствует развитию акушерских осложнений, таких как ПЭ и рождение недоношенных детей. Нарушение маточно-плацентарного кровообращения при аденомиозе может вызвать ишемию плаценты с последующим развитием ПЭ[41].
Таким образом, очевидно, что нарушение имплантации бластоцисты, плацентации и маточно-плацентарного кровотока у женщин с эндометриозом лежит в основе повышенного риска возникновения таких акушерских осложнений, как ПП, ОП, приращение/врастание плаценты, ГРВБ и ПЭ/эклампсия, задержка роста плода и мертворождение.
ОСТРЫЕ ОСЛОЖНЕНИЯ ПРИ ЭНДОМЕТРИОЗЕ
Спонтанный гемоперитонеум — опасное для жизни осложнение, которое может возникнуть во время беременности у пациенток с эндометриозом, чаще всего в третьем триместре[50, 51]. Согласно G. Brichant и соавт., частота данного осложнения занижена в связи с затруднительной диагностикой[52]. Из-за увеличенной матки на поздних сроках беременности и скрытого кровотечения иногда бывает сложно диагностировать гемоперитонеум у беременных до операции. В большинстве случаев местом кровотечения является задняя стенка матки, и врачи зачастую диагностируют гемоперитонеум только во время или после операции[51].
Гемоперитонеум у беременных с эндометриозом может быть следствием разрыва сосудов широкой маточной связки[53], разрыва маточно-яичниковых сосудов, кровотечения из эндометриоидных очагов[51, 53], разрыва матки[37, 51]. Псевдоаневризма маточной артерии (ПАМА) при ретроцервикальном эндометриозе также может стать причиной гемоперитонеума во время беременности, диагноз ее обычно подтверждается только с помощью послеродовой визуализации[54]. Согласно Z. Feld и соавт., ПАМА развивается из-за децидуальной реакции при ретроцервикальном эндометриозе[54].
Клиницисты должны помнить и о других возможных причинах гемоперитонеума во время беременности, таких как кровотечение из варикозно-расширенных вен матки, разрыв маточной трубы при внематочной беременности, апоплексия яичника (на ранних сроках беременности) и случаи разрыва матки, не связанные с эндометриозом[55].
Возможными острыми осложнениями беременности, особенно при глубоком инфильтративном эндометриозе, являются также перфорация и окклюзия кишечника, которые возникают крайне редко и непредсказуемо[56].
Кроме того, I. Chiodo и соавт. сообщили о редком случае урогемоперитонеума во время беременности с гибелью плода у пациентки с глубоким инфильтративным эндометриозом. У этой пациентки появились симптомы острого живота из-за кровотечения из правой маточной артерии и наличия свободной мочи в брюшной полости вследствие разрыва мочеточника, пораженного эндометриозом[57].
В соответствии с вышеизложенным, у пациенток с острой абдоминальной болью во время беременности, особенно если она сопровождается нарушением гемодинамики матери и дистрессом плода, всегда следует исключать спонтанный гемоперитонеум или разрыв матки, так как ранняя диагностика и своевременная операция имеют решающее значение для сохранения жизни матери и ребенка в таких ситуациях[51].
УЛУЧШЕНИЕ ИСХОДОВ БЕРЕМЕННОСТИ У ПАЦИЕНТОК С ЭНДОМЕТРИОЗОМ
Хроническое воспаление, ассоциированное с эндометриозом, вызывает образование спаек в малом тазу, которые искажают нормальную анатомию таза и ведут к бесплодию. С учетом этого методы лечения ассоциированного с эндометриозом бесплодия должны включать лапароскопию: проведение цистэктомии, лазерной абляции, плазменной коагуляции или электрокоагуляции при эндометриоме; эксцизию эндометриоидных очагов и ретроцервикального эндометриоза; адгезиолизис. Способ зачатия следует выбирать согласно индексу фертильности при эндометриозе. Выполнение ЭКО и переноса эмбриона может быть предложено в качестве первого этапа пациенткам, которые ранее оперировались и имеют низкий овариальный резерв, и/или при наличии мужского фактора бесплодия. Сверхдлительный протокол с агонистами ГнРГ увеличивает частоту наступления беременности у пациенток с эндометриозом III–IV стадии.
Эндометриоз связан не только с недостаточностью лютеиновой фазы — он также является причиной резистентности к прогестерону, нарушения рецептивности эндометрия, а следовательно, назначение прогестерона пациенткам с эндометриозом может стать ключом к предотвращению не только выкидышей и ПР, но и ПЭ/эклампсии, ПП, ОП и задержки роста плода[58, 59]. В настоящее время предпочтение отдается натуральному прогестерону в виде суппозиториев во влагалище (микронизированный прогестерон в дозе 800 мг/день до 16 недель беременности, затем в дозе 200 мг/день до 36 недель), так как недавний крупный систематический обзор рандомизированных исследований показал, что для профилактики ПР эффективен только натуральный прогестерон1. Кроме того, согласно рекомендациям ВОЗ, беременным женщинам с высоким риском развития ПЭ в период с 12 до 36 недель гестации следует назначать 75–150 мг ацетилсалициловой кислоты ежедневно, врачи должны помнить о том, что пациентки с эндометриозом относятся к группе высокого риска развития ПЭ2.
Прием фолиевой кислоты в дозе 400 мкг/день, начатый как можно раньше (лучше за 3 месяца до зачатия) и продолжающийся в течение первых 3 месяцев беременности, способствует нормальной плацентации и, следовательно, снижению риска развития ПР и ГРВБ[60] (табл. 4).
Таблица 4
Улучшение исходов беременности у пациенток с эндометриозом
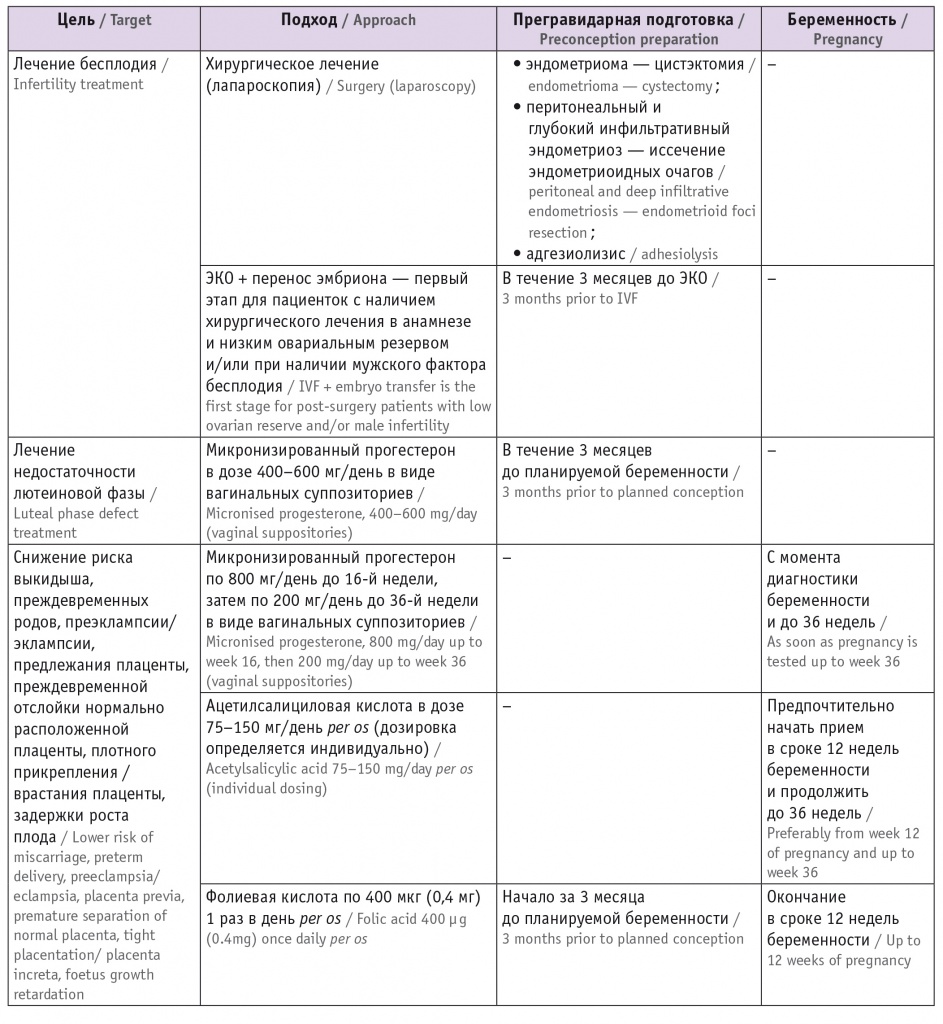
ЗАКЛЮЧЕНИЕ
Эндометриоз — фактор риска развития тяжелых осложнений во время беременности, причем не только на ранних сроках, но и во втором, третьем триместрах беременности и даже в послеродовом периоде. У пациенток с аденомиозом риск возникновения акушерских осложнений в несколько раз выше.
Патофизиологическое объяснение осложнений беременности у женщин с эндометриозом включает в себя множество сложных механизмов, а биохимические пути их до сих пор полностью не выяснены. Поэтому необходимы дальнейшие исследования, направленные в том числе на оптимизацию тактики ведения беременных с эндометриозом.
С целью предотвращения нарушения имплантации, плацентации, цитотрофобластической инвазии и маточно-плацентарной перфузии с последующим повышенным риском выкидышей, преждевременных родов, гипертензивных расстройств во время беременности, преэклампсии, предлежания плаценты, отслойки плаценты, приращения/врастания плаценты и задержки роста плода беременным с эндометриозом (особенно при III–IV стадии заболевания и аденомиозе) следует назначать прогестерон, ацетилсалициловую и фолиевую кислоту.
Поступила: 11.01.2021
Принята к публикации: 14.04.2021
_________
1 EPPPIC Group. Evaluating Progestogens for Preventing Preterm birth International Collaborative (EPPPIC): meta-analysis of individual participant data from randomised controlled trials. Lancet. 2021; 397(10280): 1183–94. DOI: 10.1016/S0140-6736(21)00217-8
2 World Health Organization. WHO Recommendations for Prevention and Treatment of Pre-Eclampsia and Eclampsia. Geneva: World Health Organization; 2011. 48 p. URL: https://www.ncbi.nlm.nih.gov/books/NBK140561/ (дата обращения — 01.04.2021).








