В настоящее время не вызывают сомнений приоритетность и значимость для акушерства проблем, связанных с преждевременными родами[2]. Несмотря на многочисленные исследования, направленные на повышение эффективности лечения угрозы преждевременных родов, их частота в различных странах колеблется в пределах 5–15%[2, 6]. В России этот показатель составляет в среднем 7%, причем 1–2% преждевременных родов происходят в срок до 28 недель[3].
По данным литературы, на долю недоношенных детей приходятся 60–70% случаев ранней неонатальной смерти и 50% неврологических нарушений, а заболеваемость среди недоношенных детей в 3,4 раза выше, чем среди доношенных[4]. В течение двух лет после выписки из отделения патологии новорожденных 2–5% детей умирают от причин, связанных с недоношенностью. Мертворождение при преждевременных родах наблюдается в 8–13 раз чаще, чем при срочных родах[2, 8]. Все это диктует необходимость своевременной диагностики преждевременных родов и поиска оптимальных способов лечения[2].
По рекомендации ВОЗ, преждевременные роды подразделяют по срокам гестации на очень ранние (22–27 недель), ранние (28–33 недели) и собственно преждевременные роды (34–37 недель). Такое разделение обусловлено тем, что их этиология, особенности ведения и исходы на данных этапах беременности различны. Так, в сроке 22–27 недель основными причинами преждевременных родов являются инфекция и истмико-цервикальная недостаточность, а в сроке 28–33 недель — внутриутробная инфекция, экстрагенитальные заболевания матери, стресс[2, 3, 5].
В настоящее время для предупреждения преждевременных родов чаще всего используют препараты, подавляющие сократительную деятельность матки, — β2-адреномиметики. Они применяются в виде монотерапии или в комбинации с препаратами прогестерона. Однако из-за неспецифичности действия их прием нередко приводит к развитию побочных эффектов у беременной женщины: тахикардии, тремора, тошноты, головной боли, боли в груди, гипергликемии, гипокалиемии. Нежелательные эффекты у плода не описаны[2].
Особого внимания заслуживают исследования, посвященные использованию при лечении угрозы преждевременных родов нового препарата атозибан — селективного антагониста рецепторов окситоцина. Он обладает специфической тропностью к рецепторам миометрия и уменьшает частоту его сокращений без неблагоприятного влияния на сердечно-сосудистую, дыхательную и нервную системы[7].
Цель исследования: сравнительная оценка эффективности и безопасности атозибана и β-адреномиметика гексопреналина при лечении угрозы преждевременных родов в сроке гестации 24–33 недели.
МАТЕРИАЛЫ И МЕТОДЫ
Проспективное сравнительное контролируемое исследование проводили в 2014 г. в ГБУЗ МО «Московский областной перинатальный центр». Из зарегистрированных за исследуемый период 6422 родов 541 (8,4%) были преждевременными, в том числе в 62 случаях в сроке беременности менее 28 недель, что составило 11,5% от всех преждевременных родов и 0,9% от общего количества родов.
В исследовании приняли участие 76 пациенток, которых стратифицировали на две сопоставимые группы: I группа — 38 беременных женщин, у которых для токолиза использовали атозибан; II группа — 38 беременных, которые в качестве токолитика получали гексопреналин.
Исследуемые лекарственные препараты прошли клинические испытания и разрешены к применению у беременных для лечения угрозы преждевременных родов на территории Российской Федерации[1].
Критерии включения в исследование: срок гестации 24–33 недели, возраст старше 18 лет, добровольное согласие на проведение токолитической терапии. Ни одна женщина не была исключена из исследования.
Возраст участниц — от 22 до 45 лет. Медианы среднего возраста пациенток выделенных групп не имели статистически значимых различий: в I группе — 32,5 года, во II группе — 33,1 года (р > 0,05).
Массо-ростовые показатели пациенток двух групп также существенно не различались: медиана ИМТ в I группе составила 24,8 кг/м2, во второй — 24,5 кг/м2 (р > 0,05).
Табакокурение (фактор риска преждевременных родов) было отмечено у 17,9% женщин I группы и у 16,6% II группы (р > 0,05).
Экстрагенитальные заболевания отмечены у 41,6% участниц I группы и у 39,8% во II группе (р > 0,05). Среди них наиболее часто встречались болезни мочевыделительной системы (45,2% и 43,2% соответственно), органов дыхания (32,7% и 33,0% соответственно) и системы кровообращения (10,8% и 12,0% соответственно).
В структуре гинекологических заболеваний у пациенток обеих групп первое место занимали хронические воспалительные заболевания органов малого таза (56,0% и 59,5% соответственно, р > 0,05). Инфекция половых путей сопровождала беременность у 72,3% участниц I группы и 68,1% II группы (р > 0,05). Основные возбудители: Candida albicans (51,0% и 52,4% соответственно), Ureaplasma urealyticum (43,3% и 44,6% соответственно), Gardnerella vaginalis (40,0% и 38,9% соответственно), Chlamydia trachomatis (30,0% и 32,6% соответственно). Следует отметить, что у большинства пациенток обеих групп в анамнезе были репродуктивные потери (52,2% и 49,9% соответственно, р > 0,05), что следует рассматривать как значимый фактор угрозы преждевременных родов[2, 5].
Диагноз угрозы преждевременных родов ставили на основании наличия регулярных сокращений матки продолжительностью не менее 20–30 секунд и частотой не менее четырех раз в течение 30 минут, а также структурных изменений шейки матки (длина шейки матки менее 25 мм по данным УЗИ)[3].
Решение о проведении токолитической терапии принимал консилиум врачей акушеров-гинекологов и неонатологов с учетом согласия самой пациентки.
Эффективность токолитической терапии оценивали по динамике маточных сокращений и состояния шейки матки.
Токолиз атозибаном в соответствии с инструкцией проводили в три последовательных этапа[3, 5]:
- первый этап — в/в болюсно один флакон 0,9 мл препарата без разведения в течение 1 минуты (начальная доза — 6,75 мг);
- второй этап — инфузионно на инфузомате в дозе 300 мкг/мин (скорость введения — 24 мл/ч) в течение 3 часов;
- третий этап — продолжительная инфузия в дозе 100 мкг/мин (скорость введения — 8 мл/ч) в течение 45 часов.
Максимальная курсовая доза атозибана не превышала 330 мг.
Токолиз гексопреналином в соответствии с инструкцией выполняли в следующем режиме:
- в/в болюсно 10 мкг препарата, разведенных в 10 мл 0,9%-го раствора хлорида натрия, в течение 5–10 минут;
- дальнейшая инфузия 0,3 мкг/мин до 48 часов.
Общая суточная доза гексопреналина составила 430 мкг.
Пролонгирование беременности на 48 часов дает возможность провести профилактику дистресс-синдрома плода глюкокортикоидами, поэтому для сравнительной оценки эффективности препаратов были взяты периоды «48 часов» как минимальный показатель эффективности токолитической терапии и «7 суток»[6, 9].
Безопасность препаратов определяли по частоте побочных эффектов, возникавших при проведении токолиза.
Статистическую обработку данных проводили на персональном компьютере с применением стандартных пакетов программ статистического анализа SPSS 17.0. Применяли методы описательной и аналитической статистики: вычисляли средние и относительные значения числовых показателей, стандартную ошибку, критерий Стьюдента, критерий Колмогорова — Смирнова, отношение шансов. Различия считали достоверными при p < 0,05.
РЕЗУЛЬТАТЫ
Данные, полученные при сравнительной оценке эффективности токолитической терапии атозибаном и гексопреналином, представлены в таблице 1.
Таблица 1
Эффективность токолитической терапии атозибаном и гексопреналином
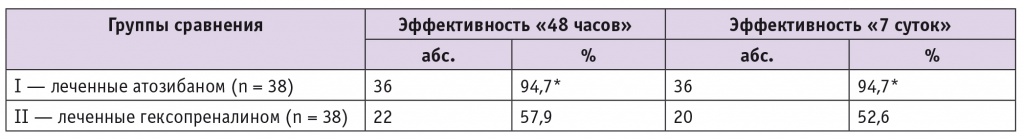
* Различия со II группой статистически значимы (р < 0,05).
Полученные результаты свидетельствуют, что по токолитическому эффекту атозибан превосходит гексопреналин (отношение шансов — 16,1; 95%-й ДИ = 15,7–16,5). Согласно данным литературы, атозибан может оказывать противотревожное действие. Он ингибирует синтез иммуносупрессорных цитотоксинов, что опосредованно способствует уменьшению маточных сокращений[5].
Нами проведен анализ токолитического эффекта атозибана и гексопреналина в зависимости от срока гестации: в 24–27 недель и 28–33 недели. Для этого пациентки обеих групп были стратифицированы на подгруппы Ia, IIa и Ib, IIb соответственно.
Как видно из данных, представленных в таблице 2, в сроках 24–27 недель гестации частота достижения токолитического эффекта в течение 48 часов и через 7 суток в группе женщин, леченных атозибаном, в 1,8 раза превышала таковую в группе леченных гексопреналином.
Таблица 2
Эффективность токолитический терапии атозибаном и гексопреналином в зависимости от срока гестации
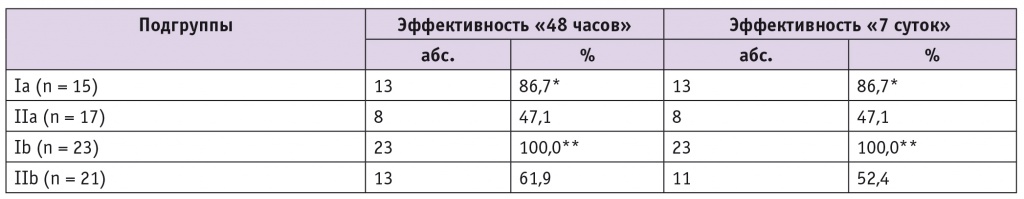
* Различия между подгруппами Ia и IIa статистически значимы (р < 0,05).
** Различия между подгруппами Ib и IIb статистически значимы (р < 0,05).
Примечание. Погруппа Ia — леченные атозибаном в сроке беременности 24–27 недель; IIa — леченные гексопреналином в сроке 24–27 недель; Ib — леченные атозибаном в сроке 28–33 недели; IIb — леченные гексопреналином в сроке 28–33 недели.
В сроках гестации 28–33 недели 48-часовой токолитический эффект при использовании атозибана наблюдали в 1,6 раза чаще, чем при применении гексопреналина, эффект в течение 7 суток — в 1,9 раза чаще.
В целом эффективность терапии в сроке 28–33 недели гестации была выше, чем в 24–27 недель (эффективность «48 часов»: 100,0% и 86,7% соответственно при токолизе атозибаном и 61,9% и 47,1% соответственно при токолизе гексопреналином; эффективность «7 суток»: те же значения при применении атозибана и 52,4% и 47,1% соответственно при использовании гексопреналина), что, возможно, обусловлено разными причинами преждевременных родов в этих сроках.
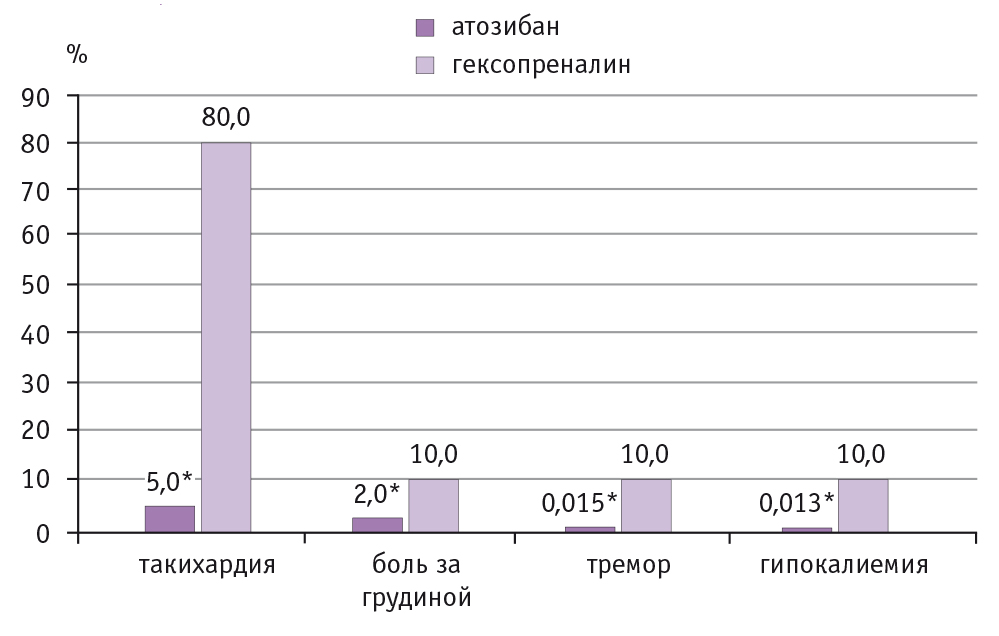
Согласно полученным данным, атозибан имеет лучший профиль безопасности, чем гексопреналин (рис. 1). Минимальные нежелательные эффекты атозибана позволяют применять его у пациенток с различными экстрагенитальными заболеваниями.
Рис. 1. Основные нежелательные явления при применении атозибана и гексопреналина, %.
* Р < 0,05
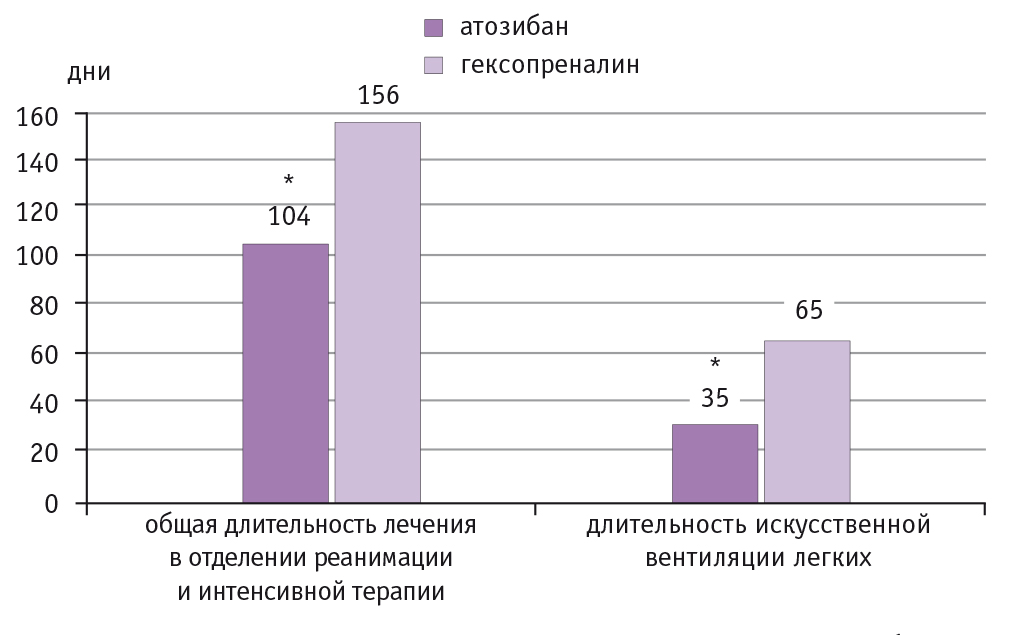
Следует отметить, что токолиз атозибаном позволил снизить продолжительность ИВЛ у недоношенных новорожденных, находившихся в отделении реанимации и интенсивной терапии. Во II группе продолжительность ИВЛ у новорожденных составила 41,7% от общей длительности лечения, а в I группе — 33,6%, что способствовало улучшению перинатальных исходов. Данные представлены на рисунке 2.
Рис. 2. Длительность искусственной вентиляции легких и общая длительность лечения недоношенных новорожденных в отделении реанимации и интенсивной терапии, дни.
* Р < 0,05
Таким образом, результаты проведенного исследования свидетельствуют, что применение препарата атозибан в качестве токолитика позволяет максимально пролонгировать беременность, снизить частоту нежелательных эффектов, сократить сроки лечения недоношенных новорожденных в отделении реанимации и интенсивной терапии.
ЗАКЛЮЧЕНИЕ
Атозибан — более эффективное средство токолитической терапии, чем гексопреналин.
Его применение фактически не сопровождается нежелательными эффектами со стороны матери, такими как тахикардия, тремор, тошнота, головная боль, боль в груди, гипергликемия, гипокалиемия, что расширяет возможности использования атозибана у беременных с экстрагенитальными заболеваниями.
Применение зарегистрированного в России современного токолитического препарата атозибан у пациенток с угрозой преждевременных родов позволяет завершить профилактику респираторного дистресс-синдрома плода и способствует улучшению перинатальных исходов.








