Угрожающий выкидыш (УВ) представляет собой клиническую ситуацию, сопровождающуюся кровотечением из половых путей с риском выкидыша или неразвивающейся беременности на ранних сроках. Согласно отечественным клиническим рекомендациям «Выкидыш», гестационный период до 22 недель подразделяется на преэмбриональный (до 4 недель 6 дней), эмбриональный (с 5 до 9 недель и 6 дней) и фетальный (с 10 до 21 недели и 6 дней)1. Если у женщины с развивающейся беременностью до 22 недель появляются кровяные выделения из половых путей или признаки отслойки хориона/плаценты, по данным УЗИ, то это состояние считается «угрожающим выкидышем»[1]2.
Кровотечение на ранних сроках встречается в 7–27% всех случаев беременности[1]. Около 15% клинически диагностированных беременностей заканчиваются выкидышем, что составляет примерно 23 млн выкидышей в год во всем мире[2]. И в большинстве случаев выкидыш происходит до 12 недель беременности[3]3.
При УВ оптимальная и своевременная терапия увеличивает шансы на сохранение беременности и живорождение. При УВ вероятность благоприятного прогноза достигает 85%, но зависит от срока беременности, возраста пациентки[4]4, а также от выбора гестагена и других факторов[5]5.
С учетом сложной демографической ситуации поиск наиболее эффективной терапии УВ для максимального количества женщин на сегодняшний день остается актуальной проблемой сообщества акушеров-гинекологов.
Важность прогестерона с физиологической точки зрения побудила исследователей и врачей рассматривать применение дополнительного прогестерона в течение ранних сроков беременности с целью предотвращения гестационных потерь у женщин с выкидышами в анамнезе и сохранения беременности у женщин, у которых началось кровотечение на ранних сроках[6].
Прогестины, или гестагены, — общее собирательное название подкласса стероидных гормонов, производимых в основном желтым телом яичников и частично корой надпочечников, а также плацентой[7].
Гестагены способствуют сохранению беременности в случае УВ вследствие недостаточности прогестерона. Это подтверждает многолетний опыт в рамках множества клинических исследований, проведенных за последние десятилетия.
Исторически сложилось так, что дидрогестерон (с момента его внедрения в практику в начале 1960-х годов) и прогестерон являются наиболее подходящими гестагенами для беременных женщин, так как представляют собой чистые агонисты рецепторов прогестерона[8, 9].
Данные последних прямых сравнительных исследований гестагенов демонстрируют более высокую эффективность дидрогестерона при беременности высокого риска, в том числе при УВ[10–12].
Дидрогестерон отличается от других гестагенов уникальностью своей молекулы. Он был получен в результате ультрафиолетового облучения прогестерона в 1950 году и представляет собой стереоизомер прогестерона, в котором атом водорода у 9-го атома углерода находится в β-положении, а метильная группа у 10-го атома — в положении α, то есть возникает обратная структура прогестерона (ретропрогестерон)[7, 12–14]. Кроме того, присутствует дополнительная двойная связь между атомами углерода 6 и 7, таким образом, вместо плокой стероидной структуры образуется «изогнутая» молекула с повышенной устойчивостью по сравнению с таковой у прогестерона[12–16]. Вышеперечисленные параметры приводят к более высокой селективности дидрогестерона к прогестероновым рецепторам и усилению гестагенной активности при минимальном воздействии на андрогенные, глюкокортикоидные и минералкортикоидные рецепторы или при его полном отсутствии[7, 12, 13, 17].
В отличие от прогестерона дидрогестерон характеризуется более высокой биодоступностью при пероральном приеме[7, 12, 13, 18], что совместно с его активностью и высокой специфичностью к прогестероновым рецепторам, а также эффективностью при относительно небольшой дозировке способствует уменьшению частоты побочных эффектов[12–14].
Дидрогестерон и прогестерон рекомендованы Российским обществом акушеров-гинекологов (РОАГ) в обновленных клинических рекомендациях «Выкидыш» (2021) и «Привычный выкидыш» (2022) с целью сохранения беременности. Актуальные клинические рекомендации РОАГ основаны на принципах доказательной медицины, отражают лучшие мировые и отечественные подходы, являясь консенсусной позицией ведущих специалистов страны, и служат для оценки качества медицинской помощи в РФ[19].
При выборе терапии УВ врачам необходимо ориентироваться на национальные клинические рекомендации и принимать во внимание все существующие исследования[19]. Для того чтобы максимально увеличить шансы на сохранение беременности и рождение здорового ребенка, рекомендованные РОАГ гестагены — дидрогестерон и прогестерон — постоянно сравнивают с точки зрения эффективности на ранних сроках беременности.
С целью оценки влияния лечения дидрогестероном на частоту выкидышей у женщин с УВ проведен данный систематический обзор. Уникальность и ценность работы заключается в том, что ранее не проводился метаанализ с включением всех исследований с использованием дидрогестерона при УВ.
В октябре 2021 года нами проведен поиск статей на любом языке в журнальных базах данных DIALOG (включая PubMed, EMBASE) и DIMENSIONS (база данных научных открытий, содержащая более 50 млн полнотекстовых статей) по следующим критериям:
-
оригинальные статьи с упоминанием дидрогестерона;
-
отчеты, посвященные результатам клинических исследований;
-
статьи, не относящиеся к обзорам, описаниям случаев, тезисам докладов на конференциях/собраниях, письмам, патентам, опросам и редакционным статьям.
Под описанием случая понимается публикация, в которой приводится случай одной пациентки. В обзоре могли быть использованы данные серий случаев (или серии клинических случаев), описывающие воздействие препарата и исходы у множества пациенток.
Проведена проверка каждого из отобранных источников, а также всех связанных с ними обзоров и метаанализов для получения дополнительных данных, которые можно было бы использовать в дальнейших клинических исследованиях.
Все рассмотренные статьи содержали описание исследований, которые были опубликованы в научной литературе. Поскольку вероятность публикации положительных результатов выше, чем других, отбор исследований для метаанализа может сопровождаться систематическими ошибками.
Итак, в обзор включены 55 клинических исследований, посвященных изучению эффективности и безопасности применения дидрогестерона у женщин с УВ (рис., табл. 1).
Рис. Схема отбора и исключения статей для обзора и метаанализа
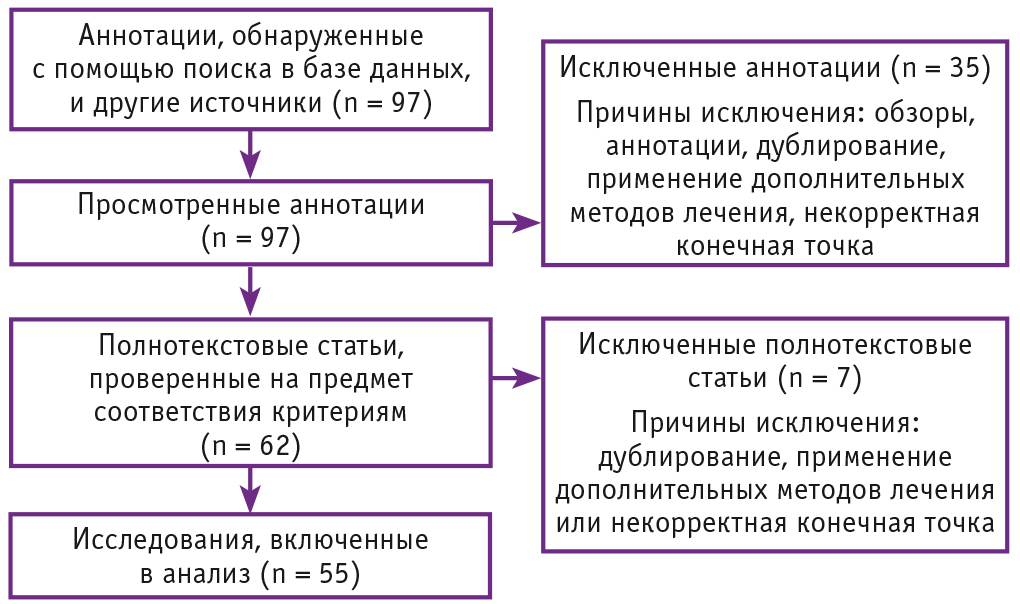
Таблица 1
Клинические исследования, включенные в обзор
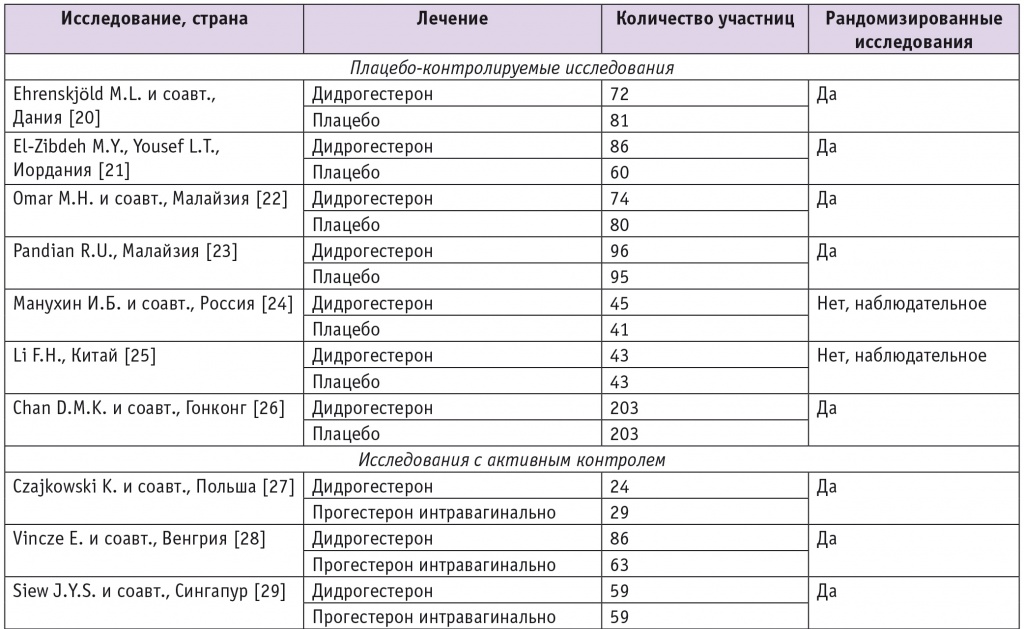
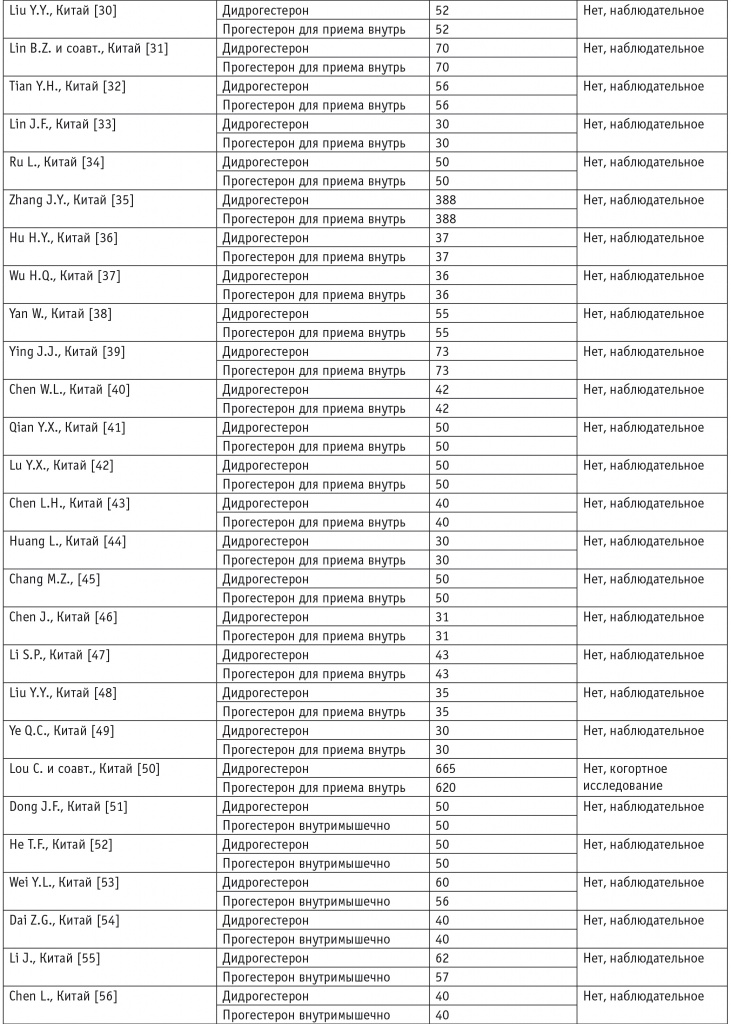
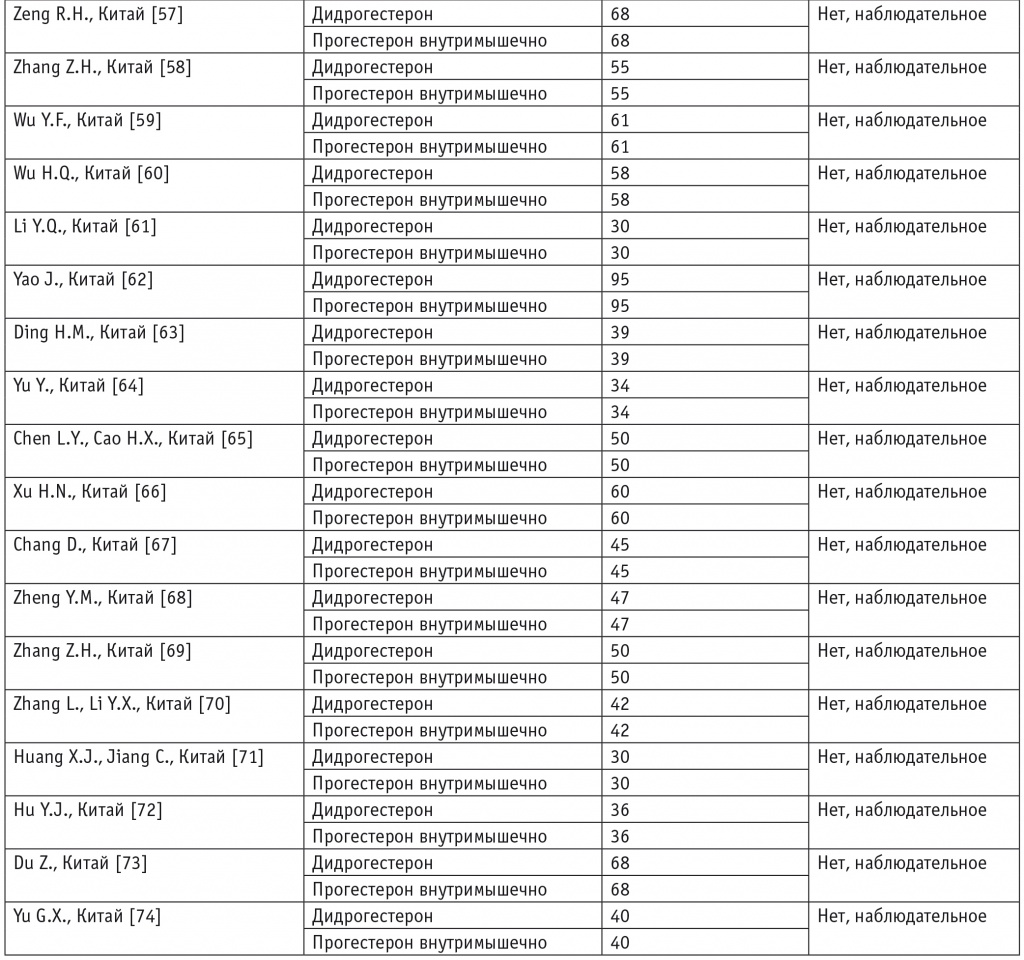
В этих исследованиях участвовали в общей сложности 7734 пациентки:
-
3911 женщин, получавших лечение дидрогестероном;
-
603 женщины, получавшие плацебо или не получавшие лечение;
-
3220 пациенток, получавших активное контрольное лечение прогестероном в лекарственных формах для приема внутрь, интравагинального или внутримышечного введения.
Поскольку данные рандомизированных исследований являются более надежными, проанализированы только рандомизированные исследования. В рамках данного проекта проведен метаанализ рандомизированных исследований, в которых дидрогестерон сравнивался с плацебо. Перед публикацией результатов осуществлен повторный поиск рандомизированных исследований в июле 2022 года, который подтвердил актуальность выбранной подборки статей.
Для проведения дальнейшего анализа получены значения разницы рисков выкидыша в группах лечения в рамках каждого исследования и определены соответствующие 95% ДИ. При расчете общей разницы рисков групп лечения и соответствующего 95% ДИ использовали метод обратной дисперсии с фиксированными и случайными эффектами. Анализ выполнялся с помощью программного обеспечения R (версия 3.6.0, пакет meta).
МЕТААНАЛИЗ ТОЛЬКО РАНДОМИЗИРОВАННЫХ ИССЛЕДОВАНИЙ, В КОТОРЫХ ДИДРОГЕСТЕРОН СРАВНИВАЛСЯ С ПЛАЦЕБО
Найдены 5 рандомизированных исследований, содержащих сравнение дидрогестерона и плацебо (табл. 2), с участием 531 пациентки, получавшей дидрогестерон, и 519 пациенток, получавших плацебо. Модель с фиксированными и случайными эффектами показала близкие значения общей разницы рисков выкидыша в группах дидрогестерона и плацебо. По результатам обоих анализов выявлено статистически значимое значение p, указывающее на значимые различия между двумя группами по частоте выкидышей.
-
Модель с фиксированными эффектами: –0,072 (95% ДИ: –0,117; –0,028), p = 0,0014.
-
Модель со случайными эффектами: –0,076 (95% ДИ: –0,129; –0,023), p = 0,0047.
Таблица 2
Метаанализ рандомизированных исследований, в которых дидрогестерон сравнивался с плацебо
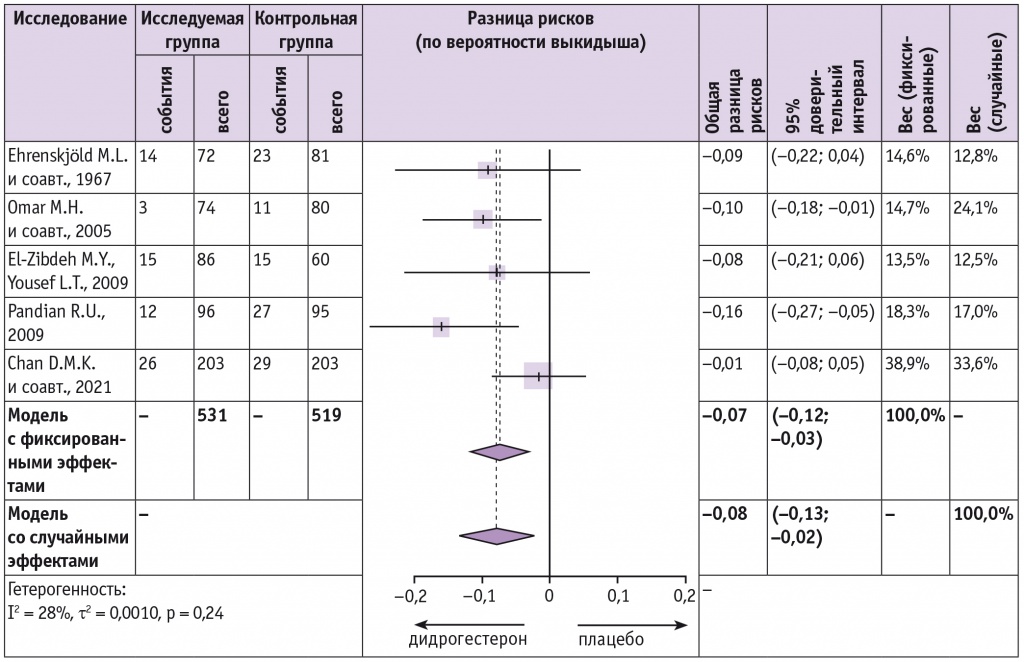
Следует отметить, что отрицательная величина разницы рисков и ее 95% ДИ, не включающий ноль, указывают на статистически значимо меньшую частоту выкидышей при применении дидрогестерона, чем при использовании плацебо.
Эти результаты коррелируют с предыдущими данными метаанализов и обзоров рандомизированных клинических исследований 2017–2021 гг., в которых дидрогестерон также значительно снижал риск потери беременности при угрожающем и привычном выкидыше[75–82]. Во включенных в Кокрейновские систематические обзоры исследованиях R.U. Pandian (2009) и A. Kumar и соавт. (2014) продемонстрировано, что при привычном выкидыше и УВ дидрогестерон статистически значимо увеличивает частоту живорождений (+10 и +16% соответственно). При этом статистически значимый результат получен для всех включенных пациенток, а не для отдельных подгрупп[23, 83].
Дидрогестерон в 2,1 раза повышает шанс сохранить беременность при УВ и в 2,4 раза уменьшает риск выкидыша по сравнению с плацебо. Но не все гестагены одинаково эффективны в снижении риска выкидыша и увеличении частоты живорождения при УВ[6, 78, 83–85]6.
В настоящее время меняется парадигма в планировании новых исследований — наибольший интерес вызывают прямые сравнительные исследования гестагенов, на которые сегодня целесообразно опираться при выборе препарата для терапии при беременности высокого риска.
Результаты крупнейшего прямого сравнительного рандомизированного исследования IPD LOTUS (2020), систематического обзора и метаанализа рандомизированных исследований по гестагенам для поддержки лютеиновой фазы в циклах ЭКО, выполненного в полном соответствии с актуальными международными требованиями к проведению клинических исследований и включившего более 2000 пациенток (номер исследования в базе PROSPERO [CRD42018105949]), свидетельствуют, что шанс наступления и сохранения беременности и шанс живорождения при применении дидрогестерона значимо выше, чем при использовании микронизированного прогестерона (р = 0,0075 и р = 0,0214 соответственно).
В исследовании доказана одинаковая безопасность дидрогестерона и микронизированного прогестерона для беременной и плода: не выявлено влияние гестагенов на частоту врожденных нарушений (в т. ч. врожденных пороков сердца) у детей[12]. Результаты показали, что пероральный дидрогестерон и вагинальный микронизированный прогестерон в первом триместре беременности в рекомендованных дозах оказывают минимальное действие на показатели функции печени. В то же время многие пациентки предпочитают пероральное применение дидрогестерона вагинальному введению прогестерона, что может оказывать существенное влияние на выбор препарата[12].
Хороший результат лечения дидрогестероном при беременности высокого риска обусловлен его химической структурой. Дидрогестерон обладает более высокой биодоступностью при пероральном приеме, демонстрирует более высокую специфичность к прогестероновым рецепторам, чем у прогестерона[7, 12, 13, 17]. Дидрогестерон также не инактивируется антипрогестероновыми антителами, поэтому может оказывать свой эффект даже в тех случаях, когда обычный прогестерон неэффективен[7].
Отличительное фармакологическое свойство дидрогестерона — наличие иммуномодулирующего эффекта. В многочисленных исследованиях показано, что под влиянием дидрогестерона иммунокомпетентные клетки вырабатывают прогестерон-индуцированный блокирующий фактор, который, воздействуя на иммунные клетки в эндометрии, способствует нормализации иммунных взаимоотношений «эндометрий — эмбрион» и продукции большого количества факторов роста и ангиогенеза, необходимых для физиологического развития беременности. В противном случае происходят активация лимфокин-активированных киллерных клеток с увеличением продукции провоспалительных цитокинов и стимуляция локальной тромбофилии, что ведет к отслойкам хориона, формированию ретрохориальных гематом и развитию плацентарной недостаточности, если беременность не прерывается[13].
Ранние потери беременности в большинстве наблюдений являются иммунообусловленными, поэтому применение дидрогестерона не только оправданный, но крайне необходимый компонент терапии привычной потери беременности.
ЗАКЛЮЧЕНИЕ
Согласно результатам данного обзора, всех опубликованных к настоящему моменту клинических исследований и их метаанализа, частота выкидышей при лечении дидрогестероном статистически значимо ниже, чем при применении плацебо. Эти данные подтверждают ранее опубликованные результаты по высокой эффективности дидрогестерона при беременности высокого риска для предотвращения акушерских осложнений.
Поступила: 02.09.2022
Принята к публикации: 21.09.2022
________
1 Привычный выкидыш. Клинические рекомендации РОАГ, 2022. URL: https://diseases.medelement.com/disease/%D0%BF%D1%80%D0%B8%D0%B2%D1%8B%D1%87%D0%BD%D1%8B%D0%B9-%D0%B... (дата обращения — 15.05.2022).
2 Там же.
3 Выкидыш (самопроизвольный аборт). Клинические рекомендации РОАГ, 2021. URL: https://diseases.medelement.com/disease/%D0%B2%D1%8B%D0%BA%D0%B8%D0%B4%D1%8B%D1%88-%D1%81%D0%B0%D0%B... (дата обращения — 15.05.2022).
4 Там же; Management of early pregnancy miscarriage. Clinical practice guideline. Institute of Obstetricians and Gynaecologists, Royal College of Physicians of Ireland and Directorate of Strategy and Clinical Programmes, Health Service Executive. April 2012, Guidel. 2014; 22 p.
5 Выкидыш (самопроизвольный аборт). Клинические рекомендации РОАГ...
6 Серов В.Н. Комментарий к статье «Применение перорального гестагена у женщин с угрожающим выкидышем в первом триместре: рандомизированное двойное слепое плацебо-контролируемое исследование». Акушерство и гинекология — online. Опубликовано 18.01.2021. URL: https://aig-journal.ru/content/news/Primenenie-peroralnogo-gestagena-u-jenshin-s-ugrojaushim-vykidys... (дата обращения — 15.05.2022).








