ВВЕДЕНИЕ
В настоящее время, по данным ВОЗ, во всем мире увеличивается доля в популяции лиц старшей возрастной группы[1–3]. В среднем почти треть своей жизни наши современницы проводят в периоде постменопаузы. Менопауза является естественным переходом к нерепродуктивному периоду жизни, причем у 40–80% пациенток накопленные к этому времени соматические и психические нарушения сопутствуют менопаузальному синдрому (МПС) разной степени выраженности[4–6].
Продолжительность активного периода в значительной степени зависит от образа жизни женщины, социально-экономических условий проживания, характера питания, наличия и особенностей течения сопутствующих соматических заболеваний, а также от качества и доступности медицинской помощи[7–11]. Особенно это важно для пациенток с наиболее часто встречающимся тяжелым течением МПС (распространенность в среднем — 51%)[12–14].
Поскольку у женщин во время перименопаузы часто встречаются соматические заболевания, врачи различных специальностей проявляют большой интерес к изучению изменений, происходящих в организме женщины в этот период, и поиску рациональных путей оптимальной коррекции всех возникающих нарушений с целью улучшения качества жизни[2, 5, 15, 16].
Менопаузальная гормонотерапия (МГТ) остается наиболее эффективным методом лечения вазомоторных симптомов, генитоуринарного менопаузального синдрома, профилактики потери костной массы и остеопоротических переломов. Согласно положениям Североамериканского общества изучения менопаузы (North American Menopause Society), МГТ назначают женщинам моложе 60 лет или с длительностью менопаузы менее 10 лет при отсутствии противопоказаний[1, 12].
Доказано, что МГТ улучшает качество сна у женщин с МПС. Эстрогены, как в монорежиме, так и в комбинации с прогестагенами, уменьшают еженедельную частоту приливов жара на 75%, значительно снижают тяжесть симптомов в сравнении с плацебо. Ни одна другая схема фармакологической и/или альтернативной терапии не дает большего эффекта[12, 15].
Метаанализ множества рандомизированных контролируемых клинических исследований свидетельствует о существенном снижении смертности от всех причин у женщин, начинающих прием МГТ в возрасте моложе 60 лет и/или в течение 10 лет после наступления менопаузы[1, 2, 17]. Различные исследования демонстрируют, что МГТ не только купирует проявления МПС, но и облегчает течение сопутствующих заболеваний[3, 7, 11, 12].
Цель данного исследования: оценить распространенность экстрагенитальной патологии у пациенток с МПС средней и тяжелой степени, а также эффективность его терапии двухфазным препаратом МГТ, содержащим эстрадиола гемигидрат и дидрогестерон.
МАТЕРИАЛЫ И МЕТОДЫ
В соответствии с поставленной целью проведено наблюдательное клиническое исследование 166 женщин в возрасте от 45 до 55 лет, страдающих МПС средней и тяжелой степени, на базе университетской клиники ФГБОУ ВО «Тюменский государственный медицинский университет» Минздрава РФ в период с 2003 по 2018 г. (главный врач — к. м. н. Ю.В. Хасанова). Обследование и лечение проведено в соответствии с Приказом МЗ РФ № 572н от 01.11.2012 г. «Об утверждении Порядка оказания медицинской помощи по профилю “акушерство и гинекология (за исключением использования вспомогательных репродуктивных технологий)”».
Все пациентки перименопаузального периода страдали МПС средней и тяжелой степени, возникшим в результате естественного угасания функции яичников. Все участницы консультированы терапевтом, при наличии показаний — врачами-специалистами: эндокринологом, маммологом, гастроэнтерологом и т. д. — с последующим назначением персонифицированной медикаментозной коррекции выявленной патологии.
Критерии включения:
- возраст 45–55 лет и наличие МПС средней и тяжелой степени у женщин в перименопаузе;
- информированное согласие на участие в исследовании.
Критерии исключения:
- экстрагенитальные заболевания в стадии декомпенсации, в том числе являющиеся противопоказанием для назначения МГТ;
- онкологические заболевания;
- зависимость от психоактивных веществ;
- состояния, угрожающие жизни;
- курение.
Женщинам с МПС при оформлении добровольного информированного согласия назначали средство МГТ (Фемостон 2), содержащее эстрогенный (17β-эстрадиол — эстрадиола гемигидрат 2,06 мг, в пересчете на эстрадиол — 2,0 мг) и гестагенный компонент (дидрогестерон 10 мг), по 1 таблетке в день курсом 6 месяцев. Данный лекарственный препарат — единственный препарат МГТ, содержащий дидрогестерон (производное 17-гидроксипрогестерона). Его главная роль в том, что он является аналогом натурального женского прогестерона, полностью лишенным андрогенных эффектов, защищает эндометрий от развития гиперпластических процессов, не ограничивает защитное действие эстрогенов на сердечно-сосудистую систему, не влияет на метаболизм глюкозы и функции печени, не вызывает повышение массы тела[2, 3, 15].
Положительное влияние МГТ на нервную и сердечно-сосудистую систему отмечается к концу 6-го месяца терапии: у пациенток исчезают психоэмоциональные симптомы и приступы симпатоадреналовых кризов[2, 15].
Таким образом, препараты МГТ с дидрогестероном (линейка препаратов Фемостон) предпочтительны для женщин, у которых МПС протекает на фоне ожирения, инсулинорезистентности, метаболического синдрома и СД, а также для тех, кому показана длительная МГТ. Лекарственные средства, содержащие 17β-эстрадиол и дидрогестерон, нейтральны в отношении андрогенного статуса женщины, не оказывают ни андрогенное, ни антиандрогенное влияние.
Степень тяжести МПС оценивали с подсчетом менопаузального индекса, предложенного в 1959 году H. Kupperman и соавт., в модификации Е.В. Уваровой. При суммарной оценке выраженности симптомов 35–58 баллов диагностировался МПС средней тяжести (n = 70; 42,2%); при 59 баллах и более — тяжелый МПС (n = 96; 57,8%). Динамику состояния здоровья женщин и степень тяжести МПС определяли до начала МГТ, через 1, 3 и 6 месяцев.
Статистическая обработка результатов исследования была проведена современными методами анализа на персональном компьютере с использованием стандартного пакета программ Microsoft Office 2010 (Microsoft Excel) и Statistica for Windows 6.0. Количественные показатели презентированы в работе в виде М ± m, где М — среднее арифметическое, m — его стандартное отклонение. Достоверность межгрупповых различий проверялась по t-критерию Стьюдента. Различия считались статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Средний возраст обследованных пациенток составил 48,0 ± 2,7 года.
В акушерском анамнезе роды были у всех женщин: у 130 (78,3%) — двое родов, у 36 (21,7%) — одни роды. Артифициальный аборт отметили в анамнезе 86% пациенток.
Структура генитальных заболеваний: хронические воспалительные заболевания внутренних половых органов (сальпингоофорит, метроэндометрит, цервицит) — 78 (47,0%), миома матки — 24 (14,5%), диффузная форма фиброзно-кистозной мастопатии — 14 (8,4%).
При обследовании у смежных специалистов у всех участниц выявлены сопутствующие эктрагенитальные заболевания: хронический тонзиллит, синусит — 136 (82,0%), заболевания щитовидной железы (гипотиреоз) — 102 (61,4%), ожирение II и III степени — 74 (44,6%), хронический гастрит, холецистит — 36 (21,7%), артериальная гипертензия — 21 (12,7%), хронический пиелонефрит — 18 (10,8%), анемия — 17 (10,2%). В среднем на одну женщину приходилось 2,3 соматических заболевания.
При изучении анамнеза обнаружилось, что экстрагенитальная патология в большинстве случаев (95%) была диагностирована до наступления менопаузы. В постменопаузальном периоде у 46 (62,2%) из 74 пациенток наблюдалось прогрессирование ожирения, что согласуется с данными литературы[1, 17, 18]. До назначения МГТ проводилась коррекция соматической патологии.
Возможно, заболевания внутренних органов ухудшают адаптационные возможности организма, ослабляют компенсаторно-приспособительные механизмы и таким образом способствуют развитию МПС и усиливают выраженность его клинических проявлений. Поэтому профилактику МПС необходимо начинать в репродуктивном периоде. Она заключается в предупреждении и своевременном лечении экстрагенитальных заболеваний, поддержании нормального веса, в сбалансированном питании, соблюдении рационального режима труда и отдыха[17, 18].
Все пациентки при первичном обращении к врачу акушеру-гинекологу предъявляли жалобы на нейровегетативные симптомы: приливы жара — 146 (88,0%), ночная потливость — 154 (92,8%), головные боли — 152 (91,6%) — и психоэмоциональные: депрессия — 156 (94,0%), раздражительность — 93 (56,0%), плаксивость — 65 (39,2%), когнитивные нарушения — 30 (18,1%).
При средней тяжести МПС через 1 месяц терапии двухфазным препаратом, содержащим 17β-эстрадиол и дидрогестерон, наблюдалось статистически значимое снижение модифицированного менопаузального индекса (ММИ) в среднем на 18 баллов (37,5%), через 3 месяца — на 22 балла (45,8%) (p < 0,05), через 6 месяцев — на 34 балла (70,8%) (p < 0,05) (табл.).
Таблица
Эффективность терапии менопаузального синдрома (МПС) двухфазным препаратом, содержащим 17β-эстрадиол и дидрогестерон, баллы модифицированного менопаузального индекса (ММИ)
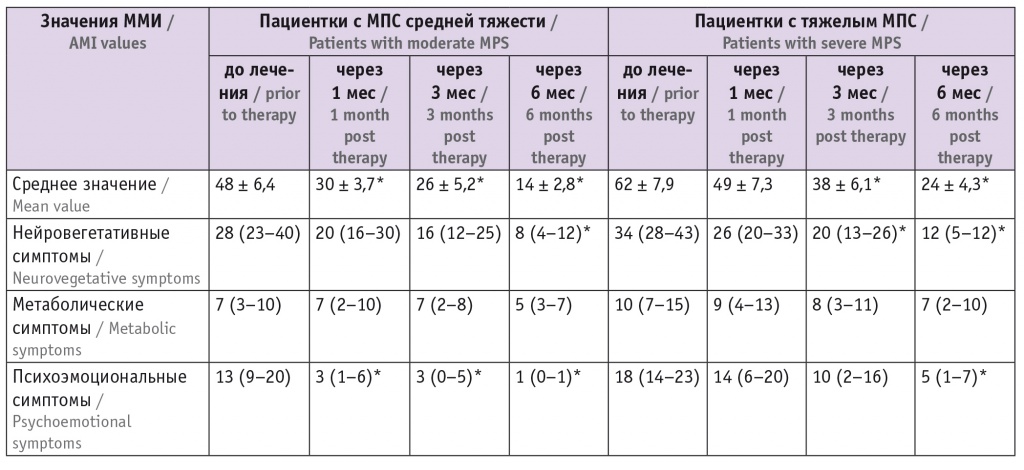
* Отличия от показателей до лечения статистически значимы (p < 0,05).
При тяжелой степени МПС через 1 месяц препарат купировал симптомы менее эффективно: ММИ уменьшился статистически незначимо — на 13 баллов (21,0%) (p > 0,05). Однако через 3 и 6 месяцев гормонотерапии у женщин с тяжелым МПС это явление компенсируется: через 3 месяца ММИ у них снизился на 24 балла (38,7%) в сравнении с показателем до лечения (p < 0,05), а через 6 месяцев — на 38 баллов (61,3%) (p < 0,05).
При анализе своего психоэмоционального состояния пациентки отмечали с 1 месяца приема МГТ улучшение настроения, исчезновение плаксивости, беспокойства, уменьшение раздражительности, рост работоспособности.
Из нейровегетативных симптомов наиболее «чувствительными» к действию МГТ оказались приливы — они полностью исчезли у всех женщин через 1 месяц применения препарата МГТ. Менее «чувствительными» были головная боль, артериальная гипертензия, снижение полового влечения, их выраженность статистически значимо снизилась только через 6 месяцев МГТ.
Таким образом, представленные статистически значимые данные свидетельствуют о положительном влиянии Фемостона 2 на течение МПС на фоне коррекции сопутствующей соматической патологии.
ЗАКЛЮЧЕНИЕ
Выявлена высокая частота экстрагенитальной патологии у пациенток с менопаузальным синдромом. После коррекции соматических заболеваний у них продемонстрирована высокая терапевтическая эффективность двухфазного препарата, содержащего 17β-эстрадиол и дидрогестерон, в купировании нейровегетативных и психоэмоциональных нарушений при климактерическом синдроме.
Поступила: 27.12.2019
Принята к публикации: 21.01.2020








