ВВЕДЕНИЕ
Самым частым осложнением при монохориальном типе плацентации является фето-фетальный трансфузионный синдром (ФФТС) вследствие формирования плацентарных анастомозов. ФФТС встречается с частотой в среднем 15% случаев среди монохориальных диамниотических двоен[1, 2]. Среди механизмов развития синдрома трансфузии близнецов — патология формирования плаценты плода-донора, повышение периферического кровотока в плаценте, наличие глубоких артериовенозных анастомозов, нарушение механизмов гуморальной регуляции, сосудистого тонуса, неоангиогенеза[3]. При отсутствии коррекции данного состояния неблагоприятный исход беременности наблюдается в 80–100% случаев[4].
Основными причинами неблагоприятных исходов при ФФТС являются наличие мелких и остаточных ветвей анастомозов после фетоскопии, наличие анастомозов на стороне плодовой поверхности плаценты плода-донора[5].
Методы лечения ФФТС и тяжелых его проявлений при монохориальной беременности включают серийные амниоредукции, фетоскопическую лазерную коагуляцию плацентарных анастомозов, селективный фетоцид одного из плодов монохориальной двойни.
Фетоскопическая лазерная коагуляция плацентарных анастомозов при ФФТС впервые была предложена J.E De Lia и соавт. в 1990 году как метод превращения монохориальной плаценты в дихориальную путем тотальной коагуляции сосудов на поверхности плаценты, пересекающих межамниотическую границу[4, 6, 7]. Методика селективной лазерной коагуляции плацентарных анастомозов является общепринятой и обеспечивает выживаемость близнецов до 62–77%[7–9].
В настоящее время стала применяться модифицированная методика селективной лазерной коагуляции плацентарных анастомозов, так называемая методика Соломона, которая впервые была описана группой специалистов из Нидерландов. Ее суть заключается в непрерывной линейной коагуляции поверхности плаценты на отрезках, соединяющих соседние коагуляционные зоны, образовавшиеся после первого этапа, от одного до другого края плаценты[10]. Существующие в настоящее время методы коррекции ФФТС постоянно модифицируются, однако монохориальная многоплодная беременность и ее осложнения до сих пор представляют одну из значимых проблем современного акушерства.
Лазерная коагуляция анастомозов плаценты под контролем УЗИ и фетоскопического исследования применяется в ФГБУ «Уральский научно-исследовательский институт охраны материнства и младенчества» Минздрава РФ с 2010 года[11].
Цель данного исследования: оценить эффективность фетоскопической лазерной коагуляции плацентарных анастомозов у женщин, беременность у которых при монохориальной диамниотической двойне осложнилась ФФТС. Исследование одобрено локальным этическим комитетом, у беременных получено информированное согласие на участие.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включены 95 женщин, беременных монохориальной диамниотической двойней, разделенных на две группы в зависимости от наличия или отсутствия ФФТС. В 1-ю группу включены 45 пациенток, у которых течение беременности во втором триместре осложнилось формированием ФФТС (TOPS и TAPS). Диагноз ФФТС устанавливался по данным УЗИ на основании общепринятой классификации R. Quintero и соавт.[12].
Фетоскопическая лазерная коагуляция плацентарных анастомозов выполнялась при наличии II и не более IV стадии, в сроке беременности от 16 до 26 недель, согласно международным рекомендациям[13] и протоколу ФГБУ «Уральский НИИ ОММ» Минздрава РФ (Ведение многоплодной беременности с монохориальным типом плацентации, № 3 2013 г.).
Пациентки (n = 50), у которых при УЗИ ФФТС не выявили, составили 2-ю группу (сравнения).
Для выполнения фетоскопии использовали комплект оборудования и инструментов фирмы Karl Storz, АИГ-лазер Dornier. Для доступа в амниотическую полость использовали прямой и изогнутый тубус фетоскопа диаметром 3,9 мм со стилетами. Доступ осуществлялся через все слои передней брюшной стенки в амниотическую полость плода-реципиента. При локализации плаценты по передней стенке матки применялся изогнутый троакар, а при локализации плаценты по задней стенке матки — прямой троакар.
Для коагуляции плацентарных анастомозов использовали хирургический полупроводниковый АИГ-лазер Dornier Medilia fiberto 8100 1 mWt, устанавливали мощность 45–50 Ватт в режиме «лапароскопия + режим стандарт + ЛПС».
На первостепенном этапе проводили идентификацию межплодовой перегородки и прослеживали ход сосудов, пересекающих ее. Ход сосудов прослеживался до зоны анастомозов. Обращали внимание не только на количество, но и на тип анастомозов (артерио-артериальный, артериовенозный, вено-венозный) и диаметр сосудов.
Хирургическая коррекция ФФТС осуществлялась под эндотрахеальным наркозом с медленной инфузией гексопреналина в условиях эндоскопической операционной при ультразвуковом мониторинге.
При госпитализации в стационар проводилось стандартное клинико-лабораторное обследование пациенток с обязательным исследованием бактериологического посева из цервикального канала. На акушерском консилиуме обсуждались показания для оперативной коррекции ФФТС, обязательно проводилась беседа с пациенткой, оформлялось письменное информированное согласие на операцию.
В послеоперационном периоде по показаниям назначались антибактериальная терапия, токолитики (гексопреналин), гестагены. Контрольное УЗИ делали на 1-е, 3-и и 7-е сутки после операции.
Эффективность операции оценивалась по двум критериям: течение и исход самой операции и раннего послеоперационного периода, а также исход беременности. Благоприятным исход считался в случае рождения хотя бы одного живого плода[14].
Критерий включения в исследование: пациентки с монохориальной диамниотической двойней без тяжелой соматической патологии. Критерии исключения: тяжелая экстрагенитальная патология в стадии декомпенсации; ФФТС I и V стадии, преэклампсия, наличие врожденных пороков развития у плода(ов), отказ от обследования и лечения.
Оценка состояния женщин включала анализ соматического, акушерско-гинекологического анамнеза. Учитывали возраст матери, особенности течения предшествующей беременности и родов, применение методов внутриутробной хирургии в группе ФФТС, способ родоразрешения.
Статистическую обработку материала проводили при помощи пакета программ Statistiсa 7.0. Проверку нормальности распределения признаков осуществляли с помощь критерия χ2. При анализе количественных показателей, распределение которых отличалось от нормального, использовали непараметрические методы (критерий Краскела — Уоллиса), затем переходили к попарным сравнениям с применением критерия Манна — Уитни, данные представляли в виде медианы (Mе), верхнего (Р25) и нижнего (Р75) квартилей.
Качественные показатели сравнивали при помощи критерия χ2. Для оценки зависимости между количественными переменными использовали коэффициент корреляции Спирмена, между качественными и количественными переменными — коэффициент корреляции Кенделла тау. При оценке корреляционных взаимосвязей уровень значимости p принимали равным 0,05.
РЕЗУЛЬТАТЫ
Многоплодная беременность в исследуемых группах в 57% случаев наступила у женщин старше 30 лет. Средний возраст в 1-й группе составил 30,1 ± 5,2 года, во 2-й группе — 30,6 ± 4,3 года (p > 0,05). Анализ антропометрических данных обследованных женщин не выявил статистически значимых различий в росто-весовых показателях. Масса тела женщин в 1-й и 2-й группах — 66,6 ± 12,8 кг и 69,1 ± 14,7 кг, рост — 162 ± 8,4 см и 164,5 ± 7,1 см соответственно. Большинство женщин основной группы и группы сравнения были соматически здоровы.
При анализе гинекологического анамнеза установлено, что возраст менархе и начала половой жизни, продолжительность менструального цикла у женщин исследуемых групп не различались (p > 0,05). В структуре гинекологических болезней доминировали заболевания шейки матки — 7 (15,6%) и 8 (16%) случаев в 1-й и 2-й группах; бесплодие встречалось в 4 (8,9%) и 6 (12%), миома матки — в 3 (6,7%) и 2 (4%) наблюдениях (р > 0,05 во всех случаях). В структуре паритета обследованных женщин в группе ФФТС доминировали повторнородящие — 33 (73,3%) против 12 (26,7%) (p < 0,001), в группе сравнения количество перво- и повторнородящих было одинаковым (50% и 50%) (р > 0,05). Статистически значимые различия в частоте медицинских абортов (9 (20%) и 10 (20%) пациенток), самопроизвольного прерывания беременности (3 (6,7%) и 3 (6%) случая), регрессирующей беременности (7 (15,6%) и 6 (12%) случаев) у женщин 1-й и 2-й групп не выявлены (p > 0,05 во всех случаях).
Кесарево сечение в анамнезе отмечалось в обеих группах с почти одинаковой частотой: 5 (11,1%) и 9 (18%) (p > 0,05).
Анализ клинического течения настоящей беременности показал, что в структуре патологических состояний у всех обследованных женщин превалировала анемия беременных — 27 (60%) и 20 (40%) случаев в 1-й и 2-й группах (р < 0,05), что согласуется результатами Л.Г. Сичинава (2014)[15].
Угроза прерывания беременности с формированием истмико-цервикальной недостаточности (ИЦН) наблюдалась в 1,4 раза чаще в группе женщин с ФФТС (19 (42,2%) против 15 (30%); р > 0,05). Повышенная частота формирования ИЦН в 1-й группе обусловлена наличием многоводия у плода-реципиента, что приводит к дополнительной механической нагрузке на шейку матки.
Согласно данным зарубежных авторов, у беременных с ФФТС наблюдаются высокая частота формирования ИЦН, а также укорочение шейки матки, что является одним из факторов риска неблагоприятного исхода беременности после оперативной коррекции синдрома трансфузии, особенно при длине шейки матки менее 20 мм[16]. Субкомпенсированная плацентарная недостаточность с нарушением маточно-плацентарного кровообращения 1Б степени отмечалась у 3 (6,7%) женщин 1-й группы и у одной (2%) участницы 2-й группы (p > 0,05).
C целью коррекции ФФТС в 1-й группе, согласно протоколу по ведению монохориальной беременности, проведено оперативное вмешательство способом фетоскопии и лазерной коагуляции плацентарных анастомозов при наличии II–IV стадии ФФТС.
В данном исследовании из 45 пациенток группы ФФТС у 8 (17,8%) была II стадия синдрома трансфузии, у 29 (64,4%) — III стадия, у одной (2,2%) пациентки — IV стадия ФФТС, у 7 (15,6) — ФФТС (TAPS). В большинстве случаев наблюдалась III стадия, что свидетельствует о запоздалой диагностике на амбулаторном этапе, когда уже имеются выраженные гемодинамические нарушения в виде нулевого или отрицательного диастолического кровотока в артерии пуповины. В одном из наблюдений имела место IV стадия, когда тяжелое течение ФФТС привело к формированию гидроперикарда, кардиомегалии у плода-реципиента.
Средний срок беременности, при котором выполнялась операция, в данном исследовании составил 19,6 ± 2,1 недели, минимальный срок гестации — 16 недель, максимальный срок гестации, при котором выполнялось оперативное вмешательство, — 24 недели, что согласуется с общепринятыми рекомендациями[17]. У 32 (71,1%) женщин плацента локализовалась по задней стенке матки.
В среднем операция длилась 44,2 ± 19,2 минуты. Амниоредукция практически во всех случаях производилась однократно, в двух случаях была необходимость повторной амниоредукции в связи с выраженным многоводием плода-реципиента. В среднем объем редукции околоплодных вод составил 838,4 ± 565 мл. Эвакуация околоплодных вод в значительных объемах не проводились ввиду высокого риска осложнений, таких как начало родовой деятельности, излитие околоплодных вод на фоне быстрого уменьшения объема полости матки.
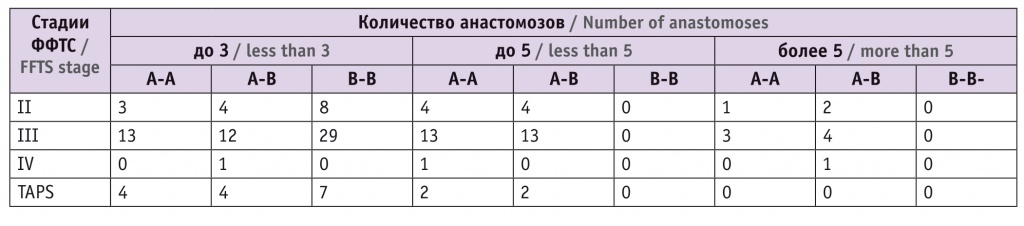
Наибольшее число анастомозов наблюдалось при III стадии ФФТС, в противоположность этому при синдроме анемии и полицетемии (TAPS) регистрировалось наименьшее количество анастомозов (табл. 1).
Таблица 1
Количество анастомозов и стадии фето-фетального трансфузионного синдрома (ФФТС)
Первым признаком эффективности оперативного вмешательства считали появление эхо-тени мочевого пузыря у плода-донора на следующие сутки, отмечаемое при УЗИ. В дальнейшем, с увеличением прошедшего после операции времени, регистрировались исчезновение маловодия у донора, нормализация пуповинного кровотока и уменьшение диссоциации плодов в массе.
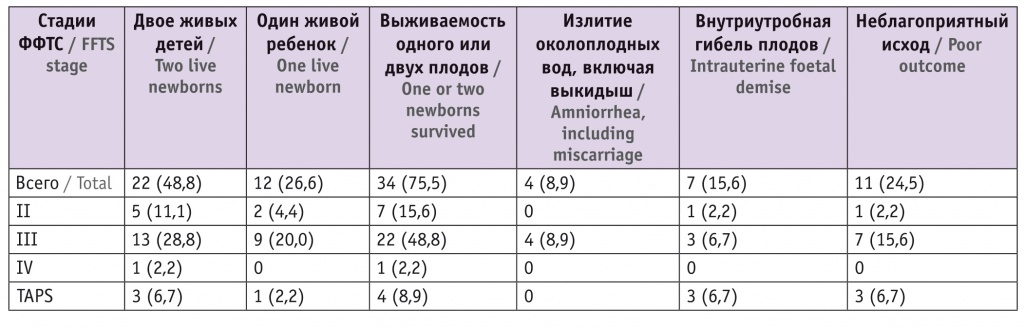
Доля пациенток, родоразрешенных двумя живыми плодами, была наибольшей при III стадии ФФТС (TOPS) и наименьшей — при синдроме анемии и полицетемии (TAPS-синдроме) (табл. 2).
Таблица 2
Исходы беременности после фетоскопии и лазерной коагуляции плацентарных анастомозов при фето-фетальном трансфузионном синдроме (ФФТС), n (%)
Из дополнительных методов оперативной коррекции в раннем послеоперационном периоде ФФТС необходимо отметить следующие оперативные вмешательства: лазерную коагуляцию сосудов пуповины, диагностический кордоцентез с последующим внутриутробным внутрисосудистым переливанием крови плоду. Коагуляция сосудов пуповины плода-донора производилась в четырех случаях: в одном случае в связи с критическим состоянием плода и в трех случаях в связи с формированием синдрома анемии и полицитемии в послеоперационном периоде, и в дальнейшем беременность пролонгировалась одним плодом. В трех случаях осуществлялся диагностический кордоцентез с последующим внутриутробным внутрисосудистым переливанием крови в связи с диагностированной тяжелой анемией.
После операции госпитализация продолжалась не менее 7 дней. Всем беременным в послеоперационном периоде назначали сохраняющую терапию гестагенами, токолитики не менее 3 дней (гексопреналин), антибактериальную терапию. При выписке рекомендовались контроль УЗИ не менее чем каждые 14 дней, госпитализация в критические сроки 22–23, 27–28 недель и непосредственно перед родоразрешением.
Средний срок родоразрешения пациенток при ФФТС составил 31,9 ± 3,6 недели, положительный исход беременности наблюдался в 75,5% случаев. Роды через естественные родовые пути при наличии ФФТС произошли у 13 (28,8%) женщин против 4 (8%) в группе сравнения (р < 0,001).
Из них практически в половине случаев имели место роды в доношенном сроке.
Неблагоприятный исход беременности ввиду таких осложнений раннего послеоперационного периода, как преждевременный разрыв плодных оболочек, антенатальная гибель обоих плодов, регистрировался у 7 (15,6%) (III стадия ФФТС) и 1 (2,2%) (II стадия ФФТС) пациентки (p < 0,001). В дальнейшем беременность была завершена медикаментозной индукцией плодоизгнания.
ЗАКЛЮЧЕНИЕ
Проведение фетоскопической лазерной коагуляции плацентарных анастомозов в сроке гестации 19,6 ± 2,1 недели позволяет пролонгировать беременность в среднем на 13 недель. Эффективность фетальной хирургии (положительный исход беременности) составляет 75,5%. Установлено, что количество осложнений зависит от типа и стадии фето-фетального трансфузионного синдрома (ФФТС). При III стадии ФФТС неблагоприятный исход беременности регистрируется значительно чаще, чем при II стадии.
Таким образом, число осложнений зависело от типа и тяжести ФФТС, наибольшее количество осложнений в раннем послеоперационном периоде наблюдалось при ФФТС III стадии (TOPS) и синдроме анемии-полицитемии (TAPS).
Поступила: 19.01.2021
Принята к публикации: 19.02.2021








