ВВЕДЕНИЕ
В настоящее время учеными разных стран доказано, что у пациентов с нарушением репродуктивной функции (НРФ) генетические изменения встречаются в разы чаще, чем в общей популяции[1, 2]. «Золотым стандартом» генетического обследования супружеских пар с НРФ стало цитогенетическое исследование лимфоцитов крови (исследование кариотипа). Частота структурных перестроек в хромосомах у этой группы пациентов может варьировать от 1,8% до 8%. В общей популяции хромосомные изменения встречаются с частотой от 0,1% до 0,5%[1, 2]
Хромосомные транслокации являются самой частой структурной перестройкой кариотипа. Транслокации подразделяют на робертсоновские и реципрокные.
При робертсоновских транслокациях происходит слияние двух акроцентрических хромосом с образованием одной метацентрической или субметацентрической хромосомы. Кариотип пациента содержит 45 хромосом.
При реципрокных транслокациях происходит взаимный обмен участками между хромосомами. В этом случае кариотип пациента содержит 46 хромосом.
Сбалансированные хромосомные перестройки, как правило, не влияют на здоровье человека. Однако у носителей хромосомных изменений в мейозе могут формироваться гаметы с несбалансированными вариантами. Эмбрионы, зачатые из таких половых клеток, будут иметь патологию кариотипа, которая может привести как к рождению генетически больного ребенка, так и к остановке развития беременности, способствовать самопроизвольному ее прерыванию.
С учетом вышесказанного следует помнить, что наличие хромосомных аберраций в кариотипе у пациентов программы ВРТ приводит к снижению числа благоприятных исходов.
В рамках ЭКО профилактические мероприятия должны сводиться к селекции и переносу только здорового эмбриона в полость матки. Решить эту задачу возможно, применяя преимплантационное генетическое тестирование (ПГТ), которое проводится обычно на клетках, полученных от пятидневных бластоцист.
ПГТ-СП (преимплантационное генетическое тестирование структурных перестроек) у пациентов с измененным кариотипом является одним из главных звеньев в цепочке профилактических мероприятий по предотвращению не только рождения больного ребенка, но и наступления беременности больным плодом [3].
При проведении ПГТ-СП у пациентов с нарушениями в кариотипе необходимо не только изучить хромосомы, вовлеченные в транслокацию, но и дополнительно исследовать их на самые распространенные хромосомные нарушения (синдромы Дауна, Патау, Эдвардса).
До настоящего времени основными методами ПГТ-СП были FISH (флуоресцентная гибридизация in situ), количественная флуоресцентная ПЦР, aCGH (сравнительная геномная гибридизация). Однако эти методы имеют ряд принципиальных ограничений и не всегда отражают полную картину исследования хромосомного набора эмбриона.
Современный метод высокопроизводительного секвенирования (Next Generation Sequencing, NGS) сейчас вытесняет другие методы ПГТ и находит все более широкое применение в клиниках ВРТ за рубежом и в России. Секвенирование более четко указывает не только на анеуплоидии, но и на наличие делеций/дупликаций. Принцип NGS принципиально отличается от принципов других методов ПГТ. Данный метод основан на определении последовательности нуклеиновых кислот.
ПГТ-СП методом NGS завоевывает все бо’льшую популярность при диагностике хромосомных нарушений у эмбриона. Публикации авторов из разных стран указывают на успешное применение секвенирования нового поколения у пациентов с нарушенным кариотипом[4, 5].
Цель исследования: определить частоту и структуру хромосомных нарушений методом NGS у эмбрионов, полученных в программе ВРТ у супружеских пар с хромосомными транслокациями.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включены супружеские пары, в которых у одного из супругов в кариотипе была выявлена хромосомная перестройка. Пары разделили на две группы — с робертсоновскими и с реципрокными транслокациями в кариотипе.
Работа проводилась с 2015 по 2019 год в Клиническом госпитале на Яузе, Центре генетических исследований «Хайтек Генетикс».
Критерием включения стало наличие хромосомной перестройки в кариотипе, критерием исключения — нормальный кариотип.
Материалом исследования служили клетки трофэктодермы 236 эмбрионов, полученных от 54 супружеских пар, в которых у одного из супругов отмечали изменения кариотипа; возраст женщин составлял от 28 до 42 лет.
Стимуляцию суперовуляции проводили согласно стандартным протоколам в зависимости от гормонального профиля и индивидуальных особенностей женщины.
Диагностика осуществлялась методом NGS на приборе MiSeq компании Illumina. Данные, полученные прибором, обрабатывали с помощью программного обеспечения BlueFluse Multi (рис.).
Рис. Примеры анализов результатов секвенирования клеток трофэктодермы методом высокопроизводительного секвенирования на платформе Illumina в программе BlueFluse Multi у пациентов с хромосомными транслокациями в кариотипе. А — Seq(1q42->1q44)×3, (5q13->5q35.3)×1, (X)×2. Выявлены дополнительный генетический материал участка 1q42->1q44 хромосомы 1 и недостача генетического материала участка 5q13->5q35.3 хромосомы 5. Б — Seq(5q23.3-5q35.3)×1, (20p13-20p12.1)×3, (X)×2. Выявлены недостача генетического материала участка 5q23.3-5q35.3 хромосомы 5 и дополнительный генетический материал участка 20p13-20p12.1 хромосомы 20. В — Seq (2q32.2->2q37.2)×3, (7q33->7q36.3)×1, (Х)×2. Выявлены дополнительный генетический материал участка 2q32.2->2q37.2 хромосомы 2 и недостача генетического материала участка 7q33->7q36.3 хромосомы 7. Г — Seq (4q21.1-> 4q35.2)×1, (6p25.3->6p21.1)×3, (XY)×1. Выявлены недостача генетического материала участка 4q21.1->4q35.2 хромосомы 4 и дополнительный генетический материал участка 6p25.3->6p21.1 хромосомы 6
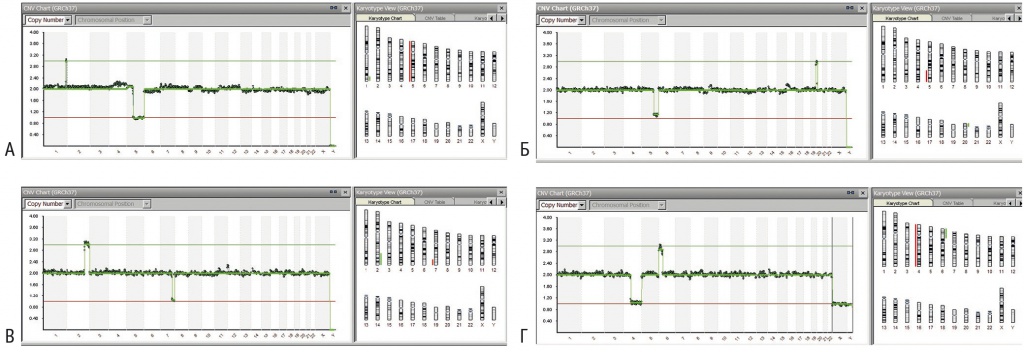
Для тестирования брали клетки 5–6-дневных эмбрионов, полученных в программе ВРТ. Все эмбрионы были получены оплодотворением методом ИКСИ. Диагностику производили согласно протоколу Illumina. Перед секвенированием осуществляли полногеномную амплификацию ДНК клеток трофэктодермы. Анализ качества полученного продукта WGA проводили с помощью электрофореза.
Статистическая обработка данных проводилась с использованием точного критерия Фишера (программа Statistica 7.0). Различия считали статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ
Представляет интерес исследование частоты и структуры хромосомной патологии у эмбрионов в зависимости от пола носителя хромосомной аберрации в семье. Всего у 54 пар проведены 65 циклов стимуляции суперовуляции. Для секвенирования были пригодны 236 эмбрионов. Анализ результатов секвенирования показал, что из 236 эмбрионов 51 имел нормальный молекулярный кариотип, а 153 — хромосомную патологию. Частота и структура хромосомной патологии, выявленной у эмбрионов, подробно представлена в таблицах 1 и 2.
Таблица 1
Результаты преимплантационного генетического тестирования структурных перестроек методом высокопроизводительного секвенирования у супружеских пар, в которых один из супругов является носителем хромосомной транслокации
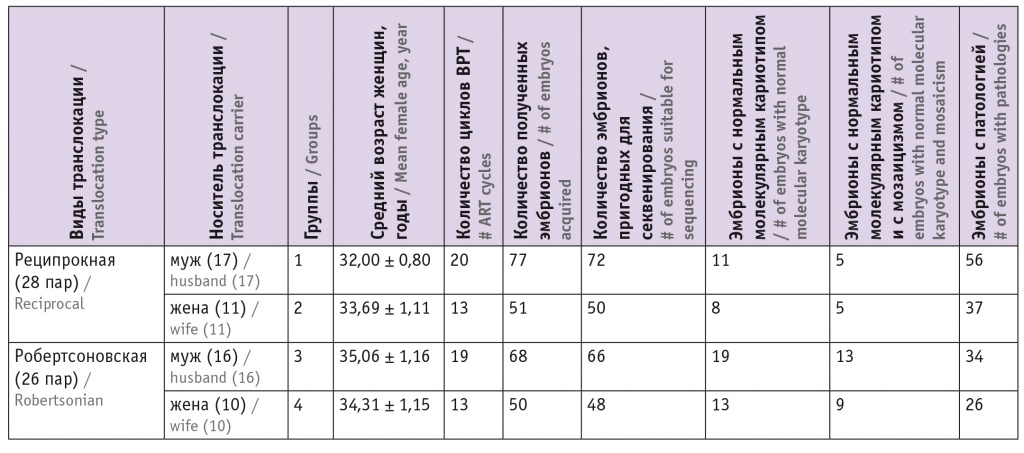
Таблица 2
Структура хромосомной патологии, выявленной при преимплантационном генетическом тестировании структурных перестроек методом высокопроизводительного секвенирования у супружеских пар, в которых один из супругов является носителем хромосомной транслокации
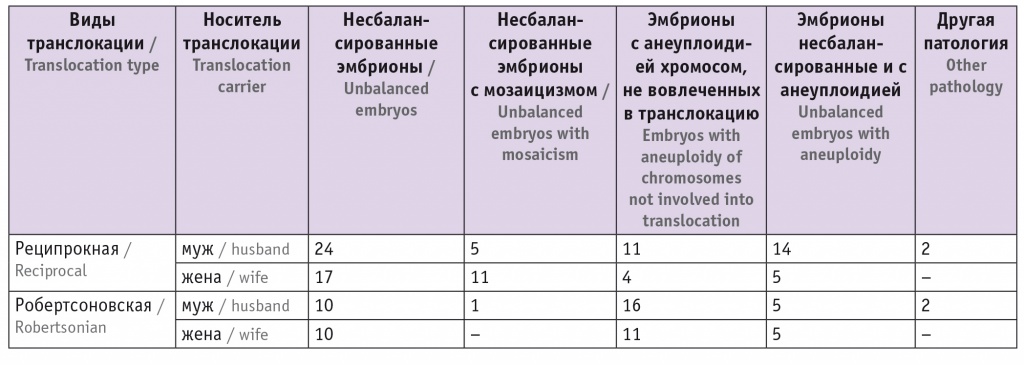
Эмбрионов с патологией было статистически значимо больше у супружеских пар с реципрокными транслокациями в кариотипе (табл. 3).
Таблица 3
Статистическая значимость различий между группами сравнения, p
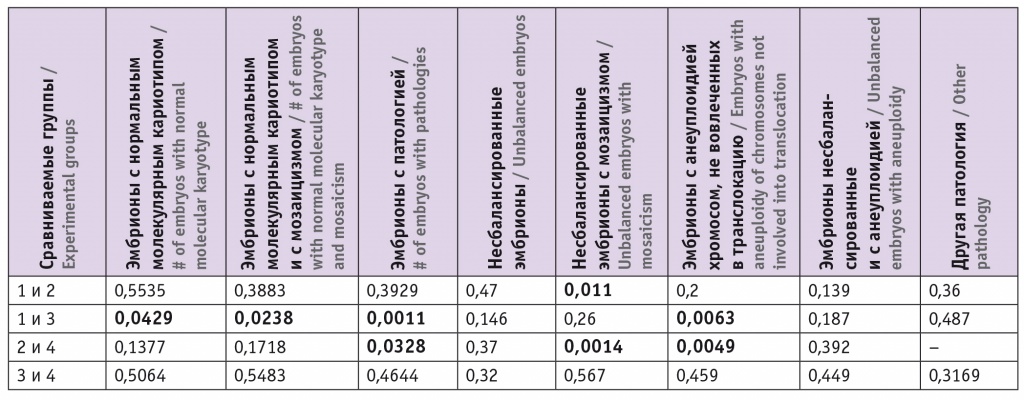
Процент эмбрионов с анеуплоидией хромосом, не вовлеченных в транслокацию, был статистически выше у супружеских пар с робертсоновскими транслокациями в кариотипе, что совпадает с данными других авторов[6], которые показали, что соотношение спорадических анеуплоидий и анеуплоидий, связанных с хромосомами, вовлеченными в транслокацию, 50 на 50 процентов.
У супружеских пар с реципрокными транслокациями найдена статистически значимая зависимость количества эмбрионов с несбалансированным кариотипом и мозаицизмом от пола носителя транслокации, чего не отмечалось в группе с робертсоновскими транслокациями.
ОБСУЖДЕНИЕ
Существующие на сегодняшний день современные диагностические морфокинетические предикторы не отражают генетический статус эмбриона[7]. Только быстрое развитие новых молекулярно-генетических методов исследования изменяет известные представления о НРФ: о возможных причинах бесплодия, остановки развития беременности.
Пациенты с изменениями в кариотипе представляют собой одну из самых сложных групп, получающих лечение методами ВРТ. Женщины из этих пар в основном имеют тяжелый отягощенный анамнез: выкидыши, неразвивающиеся беременности, малое кесарево сечение, проблемы с эндометрием и т. д. Включая их в программы ЭКО, врачи сталкиваются с проблемами не только гинекологическими, но и генетическими.
Расходятся мнения исследователей разных стран по поводу включения супружеских пар с измененным кариотипом у кого-либо из супругов, но не имеющих бесплодия, в программу ВРТ. Одни считают, что у пациенток из таких пар может наступить самостоятельная беременность плодом без хромосомной патологии, другие полагают, что нельзя рисковать здоровьем женщины и необходимо сократить время до наступления долгожданной беременности здоровым плодом.
J. Wang и соавт.[8] показали, что процент эмбрионов с анеуплоидией ниже, когда в перестройку хромосом в кариотипе вовлечены акроцентрические хромосомы (5,9% против 14,8%). Они не нашли статистически значимую зависимость между полом носителя перестройки и уровнем патологии у эмбрионов[8].
Тот факт, что у эмбрионов пациентов с транслокациями в кариотипе отмечаются анеуплоидии хромосом, не вовлеченных в перестройку, указывает на необходимость тестировать эмбрионы у них на все хромосомы[6]. Таким образом, метод NGS, который позволяет это делать, имеет большие преимущества в диагностике по сравнению с другими применяемыми методами.
При медико-генетическом консультировании таких пациентов врач-генетик может представить им только вероятностные риски возникновения хромосомной патологии у ребенка. Для решения вопроса о пролонгировании самостоятельно наступившей беременности женщине необходимо пройти пренатальную диагностику. В случае необходимости прерывания беременности у пациентки возможна, помимо осложнений от процедуры прерывания, еще и психологическая травма.
С учетом вышесказанного, по нашему мнению, во время медико-генетического консультирования пациентке должны быть предложены все существующие на сегодняшний день методы профилактики наступления у нее беременности плодом с хромосомным нарушением.
Полученные результаты исследования молекулярного кариотипа у эмбрионов пациентов со структурными перестройками хромосомного набора способствуют более полному пониманию процесса мейоза у таких людей. Новые знания в области данного процесса помогут разрабатывать более современные методы преимплантационного тестирования и четких расчетов риска возникновения у ребенка хромосомной патологии в зависимости от вида транслокации, от пола носителя данного нарушения и т. д.[8].
Наше исследование показало, что применение секвенирования нового поколения с использованием платформы компании Illumina может служить хорошим профилактическим методом в ПГТ-СП. J.F.C. Сhow и соавт. также подтвердили, что метод NGS у пациентов с транслокациями в кариотипе — самый точный для выявления патологии у эмбрионов. Они ретроспективно исследовали продукт WGA после aCGH методом NGS, и в ряде случаев, когда aCGH показал норму, метод NGS обнаружил de novo изменения участков хромосом и низкий уровень мозаицизма[4].
Как продемонстрировано выше, метод NGS дает возможность четко диагностировать у эмбрионов не только анеуплоидии, делеции и дупликации, но и мозаицизм.
Особенностью ПГТ является то, что у семей с высоким риском рождения больного ребенка появляется возможность перейти от вероятностного прогнозированию исхода беременности к однозначному.
ЗАКЛЮЧЕНИЕ
Преимплантационная генетическая диагностика методом высокопроизводительного секвенирования является на сегодняшний день самым точным методом выявления генетической патологии у эмбрионов и может быть рекомендована для профилактики невынашивания беременности и рождения больного ребенка в рамках программы ВРТ. B.C.F.K. Brunet и соавт. решительно придерживаются того же мнения[5].
Преимплантационная диагностика может стать альтернативой пренатальной диагностике для фертильных супружеских пар, имеющих высокий риск рождения ребенка с наследственной или врожденной патологией, которые в случае обнаружения у плода генетической патологии выступают против медицинского аборта по моральным, религиозным или другим мотивам.
Преимплантационное генетическое тестирование помогает решить главную задачу ВРТ — рождение здорового ребенка.
Поступила: 26.09.2019
Принята к публикации: 29.11.2019








