ВВЕДЕНИЕ
Внедрение в клиническую практику препаратов инсулина третьей генерации — аналогов инсулина — стало одним из наиболее значимых достижений последних десятилетий. Инсулиновые аналоги имеют улучшенные фармакокинетические и фармакодинамические характеристики, максимально близко к физиологическим имитирующие эффекты эндогенного инсулина, а также более низкую вариабельность действия по сравнению с человеческими инсулинами, что способствует достижению оптимального гликемического контроля при СД [1, 2].
Создание инсулиновых аналогов, помимо изменения длительности и времени начала действия инсулиновых препаратов, значительного снижения гипогликемических реакций и вариабельности гликемии, привело к уменьшению частоты побочных реакций, среди которых — инсулиновые отеки и аллергия на инсулин [3, 4].
В связи с редкостью возникновения аллергических реакций на инсулины последнего поколения — инсулиновые аналоги — мы решили представить клинический случай развития аллергической реакции на инсулин детемир у ребенка с впервые выявленным СД 1 типа.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
В педиатрическое отделение № 2 БУ ХМАО-Югры «Сургутская городская клиническая больница» в марте 2019 г. поступила пациентка В., 11 лет, с жалобами на момент поступления на повышенный уровень гликемии и тошноту.
Анамнез заболевания. Из анамнеза известно, что в 06:00 утра текущего дня девочка проснулась от сильной боли в животе. Накануне вечером выпила около 1,0 л газированного напитка (Кока-Колы), съела манты, греческий салат. Врачом скорой помощи с учетом анамнеза заподозрена острая хирургическая патология, в связи с чем ребенок был доставлен в детское хирургическое отделение. После исключения острой хирургической патологии девочку перевели в педиатрическое отделение в связи с повышением уровня гликемии до 14,5 ммоль/л, определением глюкозурии и кетонурии.
Анамнез жизни. Ребенок от первой физиологически протекавшей беременности, самостоятельных срочных родов в головном предлежании. При рождении длина тела — 53 см, масса тела — 3500 г. Росла и развивалась по возрасту, прививки по календарю. Наследственность по СД не отягощена.
Из анамнеза жизни известно, что в течение 4 лет у девочки отмечались проявления атопического дерматита (высыпания, сухость, шелушение и зуд кожи) при употреблении цитрусовых, а также как реакция на холод. При обострении получала местную терапию: метилпреднизолона ацепонат (Адвантан), увлажнение, питание кожи, — и соблюдала гипоаллергенную диету.
В течение последних двух лет наблюдалась у отоларинголога с диагнозом аллергического ринита с весенним обострением, проходила сезонный курс антигистаминного и противовоспалительного лечения.
Объективно. При осмотре состояние пациентки средней тяжести за счет дегидратации, самочувствие — умеренно страдает. Вялая, плохо идет на контакт. Масса тела — 46,5 кг, рост — 160 см, ИМТ = 18,2 кг/м2, SDS ИМТ = +0,42, SDS роста = +2,51. Кожные покровы бледно-розовой окраски, сухие, чистые, яркие сухие губы. Периферические лимфоузлы не увеличены. Щитовидная железа не увеличена, эластичная, безболезненная при пальпации.
В легких дыхание везикулярное, проводится по всем полям, хрипов нет, ЧДД — 24 в минуту, перкуторный звук легочный. Тоны сердца ритмичные, звучные, ЧСС — 92 в минуту.
Живот мягкий, безболезненный. Половые органы сформированы по женскому типу, Ma2Ax1P2Meabs — половое развитие соответствует возрасту.
При обследовании: общий анализ крови без особенностей. В общем анализе мочи: удельный вес — 1,030 г/мл, содержание глюкозы — 28 ммоль/л, кетоновых тел — 3,9 ммоль/л, белка — 1 г/л, лейкоцитов — 15 л/мкл. В биохимическом анализе крови гликемия — 14,5 ммоль/л, уровень гликированного гемоглобина — 10,42%. Кислотно-основное состояние газов и крови: гипергликемия (14,3 ммоль/л), pH = 7,35, остальные показатели без патологии.
УЗИ органов брюшной полости: диффузные изменения поджелудочной железы.
Консультация невролога: на момент осмотра данных о неврологической патологии нет. Консультация офтальмолога: миопия легкой степени (Н52.1).
После проведенного опроса, осмотра и обследования клинический диагноз не вызывал сомнений. Основной диагноз: Сахарный диабет 1 типа, манифестация (Е10.9). Целевой уровень гликированного гемоглобина < 7,5%. Сопутствующий диагноз: Миопия легкой степени (Н52.1).
Была инициирована интенсифицированная базис-болюсная инсулинотерапия: инсулин детемир и инсулин аспарт в суточной дозе 0,62 Ед/кг массы тела. Получена положительная динамика в состоянии ребенка (табл.).
Таблица
Гликемический профиль пациентки В., ммоль/л
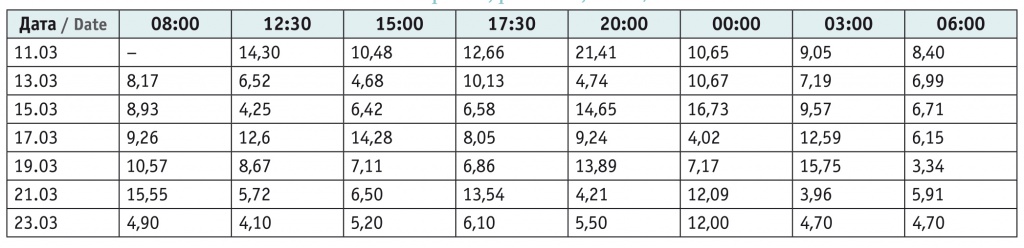
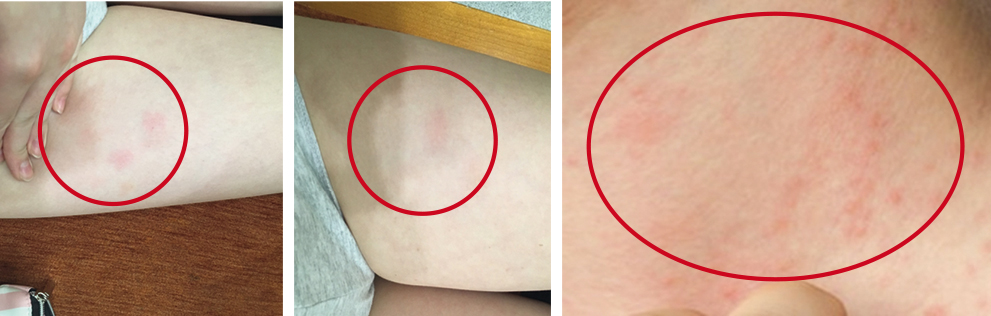
На 5-й день проведения инсулинотерапии (с 17.03) у девочки развилась аллергическая реакция в виде мелкоточечной сыпи в области подмышечных впадин, а также непосредственно в местах инъекций инсулина детемир — диффузная гиперемия, отек подкожной клетчатки, уплотнение, зуд (рис. 1). Оценка гликемического профиля показала значительную вариабельность гликемии на фоне аллергических проявлений (см. табл.).
Рис. 1. Местная аллергическая реакция. Фото авторов
Проведена консультация аллерголога. С учетом аллергического анамнеза и объективной симптоматики выставлен диагноз: Аллергический дерматит. Круглогодичный аллергический ринит. В течение 3 дней пациентка В. получала десенсибилизирующую терапию — кремния диоксид коллоидный (Полисорб), антигистаминный препарат хлоропирамин (Супрастин). На фоне проводимого лечения достигнут положительный эффект: уменьшились и исчезли зуд, гиперемия, уплотнения.
При постепенной отмене терапии получен возврат более яркой клинической картины аллергической реакции, локализованной в местах инъекций инсулина. Выставлен сопутствующий диагноз: Рецидивирующий дерматит, обусловленный применением инсулина детемир (L23.3). Развитие аллергической реакции не сопровождалось ухудшением гликемического профиля.
Из-за развития индивидуальной аллергической реакции на препарат инсулин детемир, проявляющейся мелкоточечной несливающейся сыпью на кожных покровах, а также уплотнением, гиперемией, отеком в местах инъекций произведена замена базисной терапии инсулина длительного действия детемир на инсулин сверхдлительного действия деглудек.
Введение инсулина деглудек не привело к возникновению местной аллергической реакции. В день смены препарата инсулина количество и объем высыпаний уменьшились, остаточные высыпания зарегистрированы только на конечностях, прекращение зуда отмечено в течение первой половины дня. На второй день после смены препарата аллергическая реакция в виде гиперемии, высыпаний и уплотнений, как в местах инъекций, так и на других областях тела не наблюдалась. В местах введения инсулина деглудек аллергических проявлений не было. Гликемические профили показали стабилизацию гликемии в последующие дни (рис. 2).
Рис. 2. Суточное мониторирование гликемии у пациентки В. на фоне терапии инсулином деглудеком
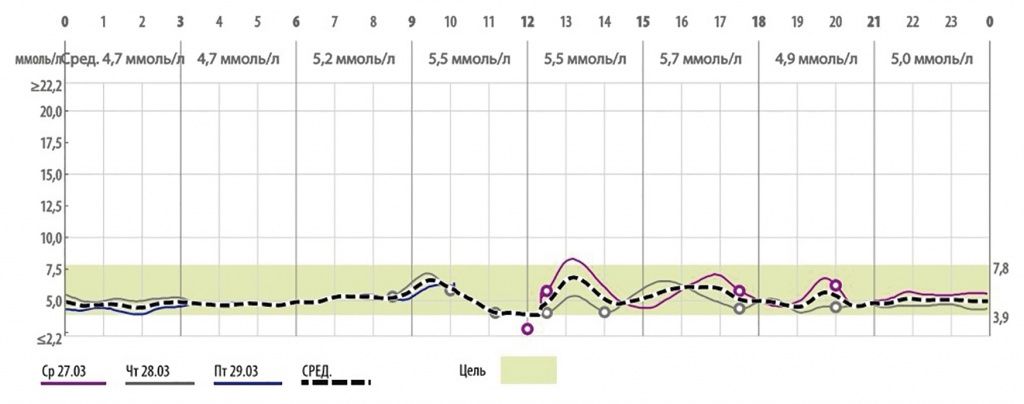
В течение 3 дней у ребенка проведено непрерывное мониторирование гликемии с помощью системы Medtronic iPro на фоне подобранной схемы базис-болюсной терапии инсулинами деглудек и аспарт (см. рис. 2). Получена низкая вариабельность гликемии со средним уровнем 5,1 ммоль/л. Время нахождения ее в диапазоне целевых значений составило 98%, превышение значений более 7,8 ммоль/л — 1%, ниже 3,9 ммоль/л — также 1%.
ОБСУЖДЕНИЕ
В зависимости от источников получения различают инсулины животного происхождения (преимущественно препараты свиного инсулина), полусинтетические препараты инсулина человека (полученные из свиного инсулина методом ферментативной трансформации), генно-инженерные препараты инсулина человека (ДНК-рекомбинантные, получаемые методом генной инженерии) [2-4].
При использовании инсулинов животного происхождения пациенты и врачи часто сталкивались с различными осложнениями инсулинотерапии, связанными с наличием различных примесей в растворах инсулина, а также обусловленными чужеродной молекулой инсулина [4-7]. Аллергические реакции на инсулин возникали достаточно редко, но были значимы для клиники.
Первое сообщение об аллергических реакциях в результате введения недостаточно очищенного бычьего инсулина зафиксировано в самом начале применения инсулинотерапии, оно опубликовано в 1922 году [7]. Тогда выявили выраженную аллергическую реакцию по типу крапивницы. Впоследствии обнаружилось, что свиной инсулин является менее аллергенным, чем бычий, и именно его длительно использовали в практической медицине [3, 7].
Ввиду широкого спектра иммуноопосредованных осложнений инсулиновой терапии большое внимание стали уделять снижению иммуногенности и аллергенности высокоочищенного свиного инсулина и более поздних доступных рекомбинантных и полусинтетических препаратов человеческого инсулина. В 1936 году создан протамина-цинк-инсулин, в 1946 году — нейтральный протамин Хагедорна (НПХ), в 1952 году — инсулин Ленте, и наконец в 1977 году начали использование рекомбинантных технологий для синтеза генно-инженерных человеческих инсулинов [2, 8, 9].
С введением в широкую практику человеческих генно-инженерных препаратов частота аллергических реакций значительно сократилась, хотя эти побочные эффекты продолжали встречаться [8-10]. Первый рекомбинантный человеческий инсулин одобрен Food and Drug Administration (FDA) в 1982 году.
Новой эрой в инсулинотерапии стала разработка в 1990-е годы аналогов инсулина быстрого действия, затем базальных аналогов в начале 2000-х годов. Аналог инсулина ультракороткого действия (инсулин лизпро) одобрен FDA в 1996 году. Первым базальным аналогом стал инсулин гларгин, созданный в 2000 году, в 2005 году разработан инсулин детемир [1, 11].
С этого времени частота развития аллергической реакции на инсулин существенно уменьшилась за счет перехода на высокоочищенные ДНК-рекомбинантные человеческие инсулины [8, 11].
Хотя большинство пациентов, получающих инсулин, вырабатывают инсулин-специфический IgE, у очень немногих из них развиваются значительные аллергические симптомы [6]. По данным разных авторов, аллергия обычно возникает не на белковую молекулу инсулина, а связана с низким качеством очистки препарата или с компонентами, входящими в состав инсулинов: пролонгаторами, стабилизаторами, консервантами — цинком, протамином, метакрезолом [4, 12, 13]. Местные аллергические реакции могут возникать и в результате неправильного введения инсулина (внутрикожно или поверхностно подкожно), чрезмерной травматизации кожи при инъекции, введения сильно охлажденного препарата, неправильного выбора места для инъекции [14, 15].
В настоящее время при использовании инсулиновых аналогов распространенность аллергических реакций составляет менее 2,4%. И только в трети случаев они считаются связанными с самим препаратом инсулина [1, 16]. Однако в инструкциях по применению инсулиновых аналогов обозначены различные побочные реакции, среди которых есть крапивница (кожное заболевание, которое характеризуется появлением сильно зудящих волдырей) и аллергические высыпания [12, 17].
Инсулин детемир — аналог инсулина длительного действия для терапии пациентов с СД 1 и 2 типов. Пролонгирование действия в препарате достигнуто соединением аминокислоты лизина в позиции В29 с цепью С14 жирной кислоты, а треонин (В30) удален. Высокая способность инсулина к самоассоциации, возможность обратимой связи с альбумином в подкожно-жировой клетчатке и в плазме крови замедляют его системную абсорбцию из мест инъекции и обеспечивают буферный эффект с низкой вариабельностью, определяя его продленное действие [9]. Результаты исследований инсулина детемир у детей показали, что его включение в базис-болюсный режим инсулинотерапии для детей и подростков является более эффективным и безопасным по сравнению с применением НПХ инсулина и инсулина гларгин [11, 17].
Отдельные сообщения о немедленных и отсроченных кожных реакциях на инсулин детемир привели к необходимости проведения исследований с указанным инсулином для выяснения потенциальных механизмов, стоящих за такими кожными реакциями [11, 15, 18–20]. Аллергические кожные реакции замедленного типа в местах введения инсулина детемир представлены гистологической картиной воспаления с эозинофильной инфильтрацией. Применение инсулина детемир в исследованиях показало значимо более частое развитие замедленной кожной реакции. Реакции немедленного типа были крайне редки, однако возможно развитие и отека Квинке, что представляет опасность для жизни больного [5, 20, 21].
Таким образом, по данным литературы, аллергические реакции на инсулин детемир чаще проявляются как реакции замедленного типа, через 48–72 часа после введения препарата, в виде крапивницы, эритематозных узелков, уплотнений, гиперемий в местах инъекций, а также сопровождаются локализованным или генерализованным зудом [22].
Нами представлен клинический случай аллергического дерматита, ассоциированного с аналогом человеческого инсулина пролонгированного действия детемир. Возникновение аллергической реакции в месте введения инсулина на 5-е сутки его использования подтверждает развитие замедленной кожной реакции у ребенка с отягощенным аллергическим фоном [19, 21]. Повторное возникновение аналогичных проявлений после прекращения симптоматической терапии подтверждает связь развития местных аллергических реакций с введением инсулина детемир.
Назначение инсулина сверхдлительного действия деглудек не вызвало аллергической реакции у пациентки и подтвердило ее связь с введением именно инсулина детемир. Следует отметить, что появление аллергических реакций сопровождалось значительной вариабельностью гликемии. Смена инсулинового аналога привела к стабилизации гликемического профиля с увеличением времени в диапазоне целевых значений до 98%.
Несмотря на то что использование инсулиновых аналогов практически исключает вероятность развития аллергических реакций, в условиях высокой распространенности отягощенного аллергического фона в детской популяции развитие таковых проявлений возможно. В литературе представлен ряд исследований и клинических случаев, демонстрирующих возникновение аллергических реакций на современные инсулиновые аналоги [16-18, 20]. Данные о наличии сенсибилизации и аллергических реакций на детемир накапливаются, о чем свидетельствует и наш клинический опыт развития нежелательных (побочных) реакций на аналоговые инсулины.
Исследования показали возможность развития аллергии, преимущественно на инсулины пролонгированного действия, в связи с формированием ответной реакции на неинсулиновые добавки в лекарственных препаратах, которые вводятся в их состав для стабилизации, обеспечения их стерильности, увеличения времени действия препарата [6, 10, 13]. Этими компонентами в препарате детемир являются гидроксибензол — фенол (консервант), метакрезол, дигидрат гидрофосфата натрия, ацетат цинка (пролонгатор) [16, 18, 19]. Сравнение состава препаратов показало, что в инсулине деглудек содержатся такие составляющие, как глицерол, метакрезол, цинк (цинка ацетат), кислота хлористоводородная/натрия гидроксид (для коррекции pH). Принципиальным отличием стало отсутствие в составе инсулина деглудек консерванта фенола, который является аллергеном.
Фенол (карболовая кислота, гидроксибензол) — углеводород, химическое органическое вещество, которое применяется в фармацевтической промышленности, так как входит в состав многих лекарственных препаратов (антисептиков, обезболивающих, антиагрегантов) как консервант, в генной инженерии его используют для очистки ДНК [23].
Применение препаратов, в состав которых входит фенол, может привести к развитию аллергических реакций, особенно в условиях отягощенного аллергического фона [16, 17].
К настоящему времени в мировой литературе описано небольшое число клинических случаев развития аллергических реакций на аналоги инсулина, в связи с этим нет отработанных алгоритмов ведения пациентов в подобных ситуациях. Следует отметить, что первым шагом при развитии аллергических реакций должна быть смена препаратов инсулина в процессе их использования, что является, по нашему мнению и по мнению ряда авторов, основным методом лечения [17, 19, 21].
ЗАКЛЮЧЕНИЕ
Аллергические реакции на инсулиновые аналоги встречаются достаточно редко и чаще характеризуются развитием местных проявлений, определяя сложности проведения терапии инсулином. Чаще всего подобные реакции развиваются у аллергически компрометированных пациентов и связаны не с самим инсулином, а с наличием вспомогательных веществ в препарате, обеспечивающих стабилизацию молекулы и ее пролонгированное действие.
Отсутствие положительной реакции на десенсибилизирующую терапию или возобновление аллергических проявлений после ее отмены — показание к смене инсулина, что чаще всего способствует исчезновению аллергических реакций. В случае сохранения аллергических проявлений и на фоне введения других инсулинов (другого препарата, другого производителя), поскольку бо́льшая вероятность появления аллергических реакций характерна именно для инсулинов продленного действия или смешанных, имеющих больший процент стабилизаторов, пролонгаторов, показан перевод пациента на инсулин короткого действия, в том числе на инсулиновую помпу.
Поступила: 23.04.2020
Принята к публикации: 03.06.2020








