Лечение некротического энтероколита (НЭК) у новорожденных остается актуальной проблемой детской хирургии, что объясняется большим процентом гнойно-септических осложнений и высокой летальностью у данной группы больных [7, 9]. Крайне важным является поиск технологий, позволяющих не только уменьшить количество неблагоприятных исходов, но и улучшить качество жизни пациента [3, 4, 8, 9, 13, 18].
Согласно современным представлениям НЭК является полиэтиологическим заболеванием [16]. Тем не менее отмечается высокая значимость нарушения кровоснабжения стенки кишечника у новорожденных [1, 10]. В последнее время пристальное внимание уделяют изменению подхода к проведению обезболивания хирургических больных за счет развития технологии быстрой реабилитации (Fast Track) [8, 15]. Эта методика наиболее изучена у новорожденных с кардиохирургической патологией [14]. Показано также статистически значимое снижение числа послеоперационных осложнений при использовании метода Fast Track в амбулаторной хирургии, у онкологических больных и пациентов, оперируемых на толстом кишечнике и органах панкреатодуоденальной зоны [2, 8, 18].
По нашему мнению, применение Fast Track у новорожденных после вмешательства по поводу НЭК может существенно сократить количество послеоперационных осложнений и сроки пребывания пациентов в стационаре, не снижая эффективности обезболивания после оперативного вмешательства.
Цель исследования: изучение влияния пресакральной анестезии ропивакаином на ускорение реабилитации новорожденных после оперативного вмешательства по поводу НЭК.
МАТЕРИАЛЫ И МЕТОДЫ
В краевой детской клинической больнице г. Ставрополя в 2012–2014 гг. проведено рандомизированное двойное слепое контролируемое проспективное исследование, в которое были включены 28 новорожденных (18 мальчиков и 10 девочек) с явным и прогрессирующим НЭК. Гестационный возраст пациентов составлял 31,8 ± 0,7 недели, масса тела при рождении — 1580,3 ± 83,5 г.
Методом генерации случайных чисел с использованием пакета статистических программ Statistica 6.0 новорожденные были рандомизированы на две группы. В первую группувошли 15 детей с НЭК, в комплексном лечении которых применялась пресакральная анестезия раствором ропивакаина в дозе 2 мг/кг. Вторую группу составили 13 новорожденных с НЭК, получавших, наряду с хирургическим лечением, интенсивную терапию традиционными методами.
В качестве оперативного пособия в обеих группах проводили лапаротомию с ревизией брюшной полости. При выявлении некротических изменений со стороны кишечной трубки выполняли резекцию пораженного отдела с наложением кишечной стомы: илеостомы были наложены у 24,3% пациентов, илеоколостомы — у 45,4%, колостомы — у 30,3% детей. У большей части пациентов первым этапом хирургического лечения являлся лапароцентез для снятия внутрибрюшного напряжения.
Контрольная группа состояла из 20 доношенных новорожденных без признаков НЭК. Пациенты выделенных групп были сопоставимы по возрасту, массе тела и полу.
Наряду с общепринятыми показателями (ЧСС, частота дыхания, АД и оценка по визуально-аналоговой шкале боли) определяли степень выраженности болевого синдрома по шкале боли Детской больницы Восточного Онтарио (англ. Children’s Hospital of Eastern Ontario Pain Scale — CHEOPS). Оценку проводили при поступлении, а также через 2, 4, 8 и 16 часов после начала терапии НЭК. Сравнивали дозу фентанила, введенного в ходе оперативного вмешательства, и длительность выполнения ИВЛ по группам; оценивали сроки экстубации больных после выполнения оперативного вмешательства. Конечными точками исследования были летальность и количество интра- и экстраабдоминальных осложнений (парез кишечника, перфорация полого органа, развитие разлитого перитонита, легочно-плевральные и септические осложнения).
Для обработки полученных данных применяли стандартные методы описательной и аналитической статистики. Анализ статистической значимости различий в группах проводили методами вариационной статистики в лицензионной компьютерной программе Statistica 6.0 (StatSoft, США). Различия оценивали по критерию Манна — Уитни, считая их статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
При установлении диагноза НЭК уровень болевого синдрома у больных в обеих группах исследования был существенно выше, чем у новорожденных группы контроля, где он составил 5,6 + 0,1 балла. При этом оценка по CHEOPS в первой и второй группах при поступлении в стационар статистически значимо не различалась и составляла 11,7 ± 0,03 балла и 12,0 ± 0,01 балла соответственно (p = 1,0) (рис.).
Рис. Динамика выраженности болевого синдрома по CHEOPS у новорожденных с некротическим энтероколитом на фоне лечения, баллы.
* P < 0,05 по сравнению с исходными данными группы 2.
** P < 0,001 по сравнению с исходными данными группы 1.
*** P < 0,001 по сравнению с данными группы 2 в аналогичные сроки наблюдения.
Примечание. В первой группе комплексное лечение дополняли пресакральной анестезией, во второй группе применяли стандартную схему ведения больных
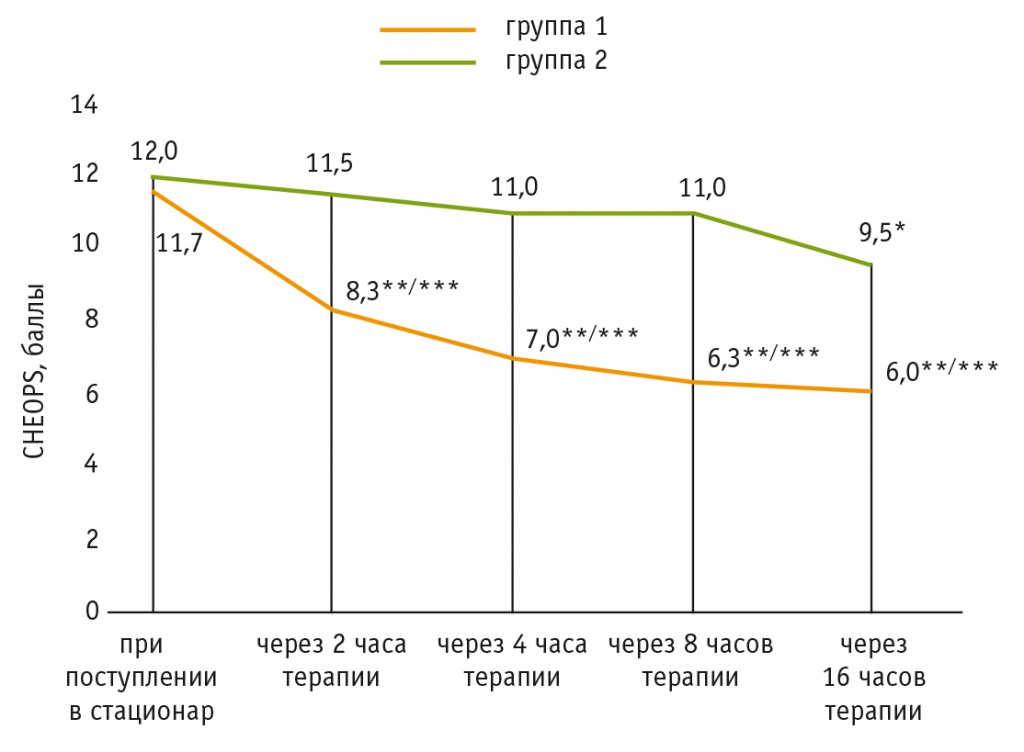
На фоне лечения в первой группе уже через 2 часа было отмечено статистически значимое снижение выраженности болевого синдрома по сравнению с исходными данными. Указанные различия сохранялись на протяжении длительного времени, причем обращала на себя внимание стойкая тенденция к уменьшению выраженности болевого синдрома с приближением оценки по CHEOPS к показателям группы контроля (5,6 ± 0,1 балла) к 16 часам от начала лечения (см. рис.).
Во второй группе наблюдалась иная картина. Статистически значимые различия с исходными данными в группе были отмечены лишь через 16 часов лечения. Но при этом, несмотря на дополнительно проведенную анальгетическую терапию, уровень болевого ощущения по CHEOPS во второй группе даже через 16 часов от начала терапии НЭК оказался существенно выше, чем в аналогичный период наблюдения в первой группе: показатель составил 9,5 ± 0,28 балла и 6,0 ± 0,5 балла соответственно (p < 0,001) (см. рис.).
Динамика изменения болевого ощущения у новорожденных отчетливо продемонстрировала, что в первой группе длительность и степень выраженности анальгетического эффекта были значительно выше, чем во второй. Это проявлялось статистически значимым снижением показателя боли по CHEOPS относительно исходных данных на всех этапах его оценки и стойкой тенденцией к уменьшению выраженности болевого синдрома в динамике наблюдения с приближением к нормальным величинам на 16-й час от начала терапии НЭК.
Следует отметить, что в первой группе доза фентанила при проведении оперативного вмешательства была существенно ниже (p < 0,05), чем во второй (табл.). Несомненно, это явилось одной из основных причин сокращения сроков нахождения новорожденных на ИВЛ после операции. Кроме того, число легочных осложнений и длительность пареза кишечника в первой группе оказались существенно меньше, чем во второй. Аналогичным образом различалась и общая частота инфекционных осложнений в группах исследования.
Таблица
Сравнительная характеристика групп новорожденных с некротическим энтероколитом
после его хирургического лечения, М ± m
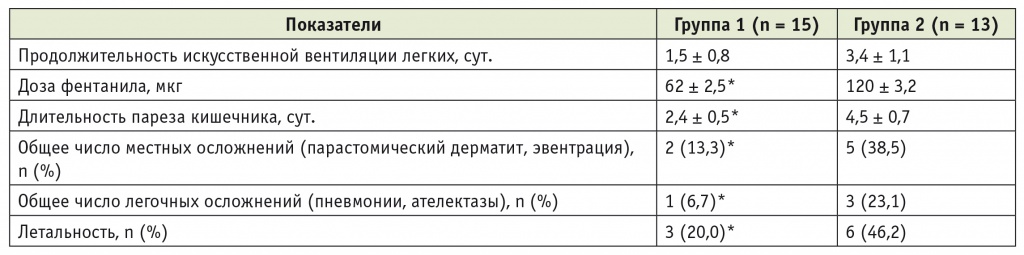
* Различия со второй группой статистически значимы: p < 0,05.
Примечание. В первой группе комплексное лечение дополняли пресакральной анестезией, во второй
группе применяли стандартную схему ведения больных.
ОБСУЖДЕНИЕ
В ходе проведенного нами ранее исследования была выявлена высокая эффективность анальгезии ропивакаином при НЭК у новорожденных [6]. При применении стандартной схемы ведения больных статистически значимые различия с исходными высокими значениями выраженности боли по CHEOPS проявлялись только через 16 часов, несмотря на дополнительную анальгетическую терапию. При применении мультимодальной схемы обезболивания блокируется передача болевого импульса на уровне нервных окончаний, что приводит к надежному и длительному анальгетическому эффекту, который, в свою очередь, позволяет уменьшить опиоидную нагрузку без снижения эффективности анальгезии. Все это дает возможность реализовать основные положения протокола ускоренной реабилитации больного после оперативного вмешательства.
Основную роль в развитии протокола Fast Track играют минимизация хирургической агрессии и изменение подхода к анестезиологическому пособию путем уменьшения введения опиатов и раннего отлучения пациента от аппарата ИВЛ [7, 18]. Учитывая имеющиеся доказательства негативного влияния опиатов на развивающийся мозг младенцев, технология Fast Track в педиатрии имеет большое будущее [11, 15]. С точки зрения патогенеза развития НЭК у новорожденных интересны работы, подтверждающие взаимосвязь между степенью болевого синдрома и выраженностью сосудистого спазма внутренних органов, в том числе кишечника [2, 16]. Следует предположить, что эффективное обезболивание может способствовать уменьшению количества осложнений и снижению летальности у новорожденных с развившимся НЭК [5, 12, 17].
У новорожденных с НЭК из первой группы реже возникали местные и системные осложнения, которые требовали проведения хирургического вмешательства. Кроме того, отмечалось уменьшение летальности в группе больных, получавших терапию с использованием пресакральных блокад. Таким образом, технология ускоренной реабилитации новорожденных с НЭК имеет большие перспективы в плане уменьшения числа осложнений и снижения летальности, но требуется проведение дальнейших научных исследований в этом направлении, ориентированных на выяснение степени безопасности методов ускоренной реабилитации после операций по поводу НЭК у новорожденных.
ЗАКЛЮЧЕНИЕ
В комплексе лечения пациентов с некротическим энтероколитом (НЭК) следует широко применять пресакральные блокады с раствором ропивакаина как эффективный и безопасный метод анальгезии у новорожденных.
Проведение пресакральных блокад ропивакаином позволяет существенно уменьшить дозировку фентанила в периоперационном периоде и сократить сроки проведения искусственной вентиляции легких у новорожденных с НЭК в послеоперационном периоде, что способствует их ускоренной реабилитации и приближает ведение пациентов к технологии Fast Track.








