Сахарный диабет 2 типа (СД2) представляет собой одно из самых серьезных неинфекционных заболеваний, оно характеризуется высокой распространенностью, значительной частотой сосудистых осложнений, а также широким спектром сопутствующей патологии[1]. СД2 в мире в среднем страдают 8,5% взрослой популяции, а в некоторых странах (например, в США) этот показатель достигает более 12%1[2]. По данным Всероссийского эпидемиологического исследования NATION, в настоящее время СД2 в России диагностирован у более 6 млн человек. Результаты исследования также показали, что 54% больных, которые имеют данное заболевание, о нем не знают, а у каждого пятого жителя нашей страны отмечаются нарушения углеводного обмена, угрожающие развитием СД2[3].
Количество пациентов с СД2 непрерывно растет. В связи со старением глобальной популяции и увеличением распространенности таких факторов риска, как низкая физическая активность и неправильное питание, ожидается, что к 2045 г. число больных СД2 в мире увеличится до 700 млн человек[2].
САХАРНЫЙ ДИАБЕТ 2 ТИПА КАК ОСНОВНОЙ ФАКТОР КАРДИОВАСКУЛЯРНОГО РИСКА
Развитие СД2 вызывает 2–4-кратное увеличение риска сердечно-сосудистых заболеваний (ССЗ), прежде всего ИБС, мозгового инсульта и гипертонической болезни[4, 5]. В свою очередь, даже умеренное повышение АД у мужчин молодого возраста является негативным фактором, способствующим трансформации функциональных изменений сосудов в органические с последующим формированием АГ как самостоятельной нозологической формы[6]. АГ приводит к атеросклеротическому поражению брахиоцефальных артерий с увеличением размеров комплекса интима-медиа и артерий почек, а при сопутствующем СД2 процесс формирования генерализованного атеросклероза значительно ускоряется[7, 8].
У больных СД2, помимо общепопуляционных факторов риска ССЗ (таких как АГ, дислипидемия, гиперкоагуляция, курение, злоупотребление алкоголем, ожирение, менопауза и низкая физическая активность), имеются специфические факторы риска: гипергликемия, гиперинсулинемия, инсулинорезистентность. Сочетание общих и специфических факторов у больных СД2 создает предпосылки для большей уязвимости системы кровообращения и развития ее патологии (рис. 1).
Рис. 1. Уязвимость сердечно-сосудистой системы при сахарном диабете 2 типа (по данным[9])
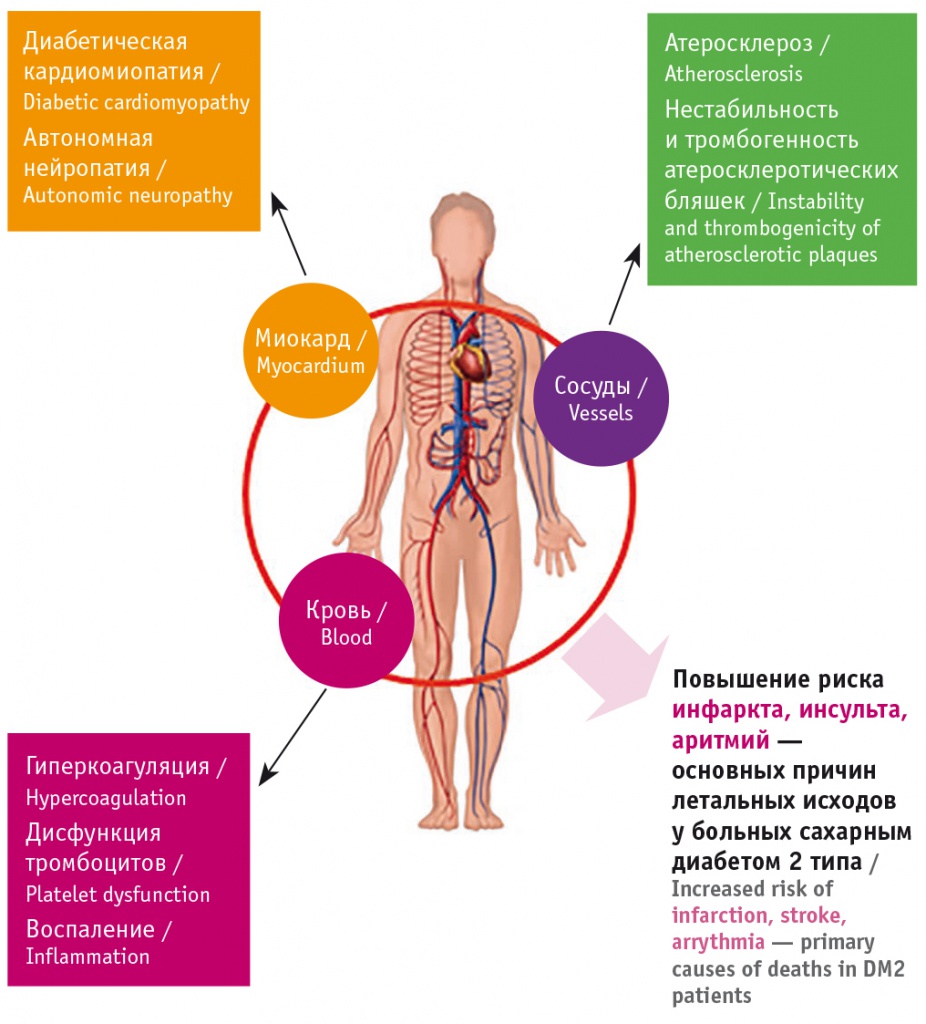
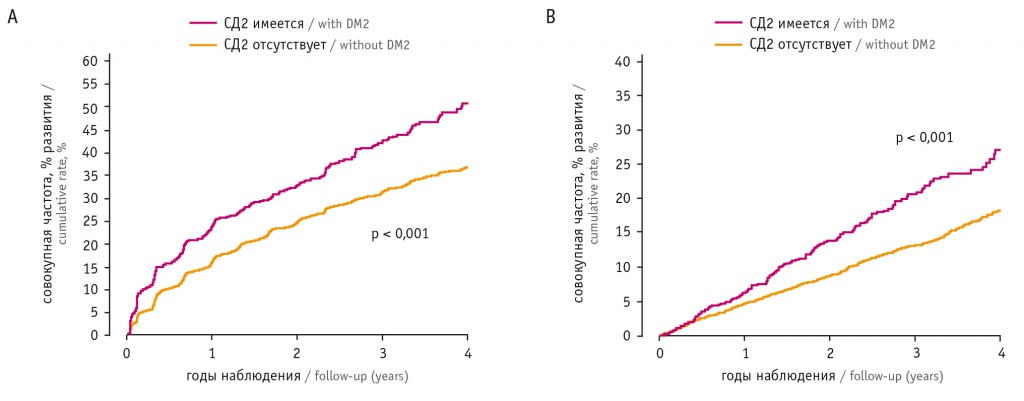
Установлено, что до 80% пациентов с СД2 погибают от сердечно-сосудистых осложнений (ССО). Ожидаемая продолжительность жизни у мужчин 60 лет, страдающих СД2, оказалась на 6–12 лет меньше, чем у их сверстников с нормальным состоянием углеводного обмена, что объясняется главным образом увеличением риска сердечно-сосудистой смерти на 58%[10]. По результатам исследования SOLVD-P (Studies Of Left Ventricular Dysfunction), наличие СД2 четко сопряжено с повышением риска таких сердечно-сосудистых исходов, как ХСН или сердечно-сосудистая смерть, а также смерть от любых причин (рис. 2).
Рис. 2. А — риск развития хронической сердечной недостаточности (ХСН), госпитализации по поводу ХСН или сердечно-сосудистой смерти у пациентов с/без сахарного диабета 2 типа (СД2); В — риск смерти от любых причин у пациентов с/без СД2 (по данным[11])
Серьезной проблемой современной диабетологии остается эффективное управление комплексом факторов сердечно-сосудистого риска. За последние годы у пациентов с СД2 несколько улучшился контроль гликемии, АД и показателей липидного профиля. Это привело к сокращению числа ССО и микрососудистых осложнений, а также повысило продолжительность жизни населения. Вместе с тем, по результатам проведенного в 2018 г. в России исследования, целевые значения гликированного гемоглобина (HbA1с) на уровне менее 7% зарегистрированы лишь у 52% пациентов[12].
Сходные данные получены в ходе популяционного исследования 2020 г. в США: у 50% больных СД2 содержание HbA1c составило ≥ 7%[13].
Недостаточно эффективное управление комплексом факторов сердечно-сосудистого риска подтверждается и в норвежском регистре с участием 9342 пациентов в возрасте 18 лет и старше, страдающих СД2 на протяжении ≥ 6 месяцев и получающих амбулаторное лечение у 281 врача общей практики. Целевые значения HbA1с (≤ 7,0%) были достигнуты у 64%, целевые значения АД (≤ 135/80 мм рт. ст./≤ 140/85 мм рт. ст. при использовании/не использовании антигипертензивной терапии) — у 50%, а целевые значения холестерина ЛПНП (≤ 1,8 ммоль/л при наличии ССЗ, ≤ 2,5/≤ 3,5 ммоль/л при отсутствии ССЗ и использовании/не использовании гиполипидемической терапии) — у 52% обследованных участников. При этом доля пациентов, достигших всех трех целевых показателей, оказалась крайне низкой — всего 17%[14].
СОВРЕМЕННЫЕ ПОДХОДЫ К МЕДИКАМЕНТОЗНОЙ КОРРЕКЦИИ САХАРНОГО ДИАБЕТА 2 ТИПА ПРЕПАРАТАМИ ИЗ ГРУППЫ АГОНИСТОВ РЕЦЕПТОРОВ ГЛЮКАГОНОПОДОБНОГО ПЕПТИДА 1 ТИПА С УЧЕТОМ КАРДИОВАСКУЛЯРНОГО РИСКА
Исследования последних лет показали различное влияние отдельных классов сахароснижающих препаратов на наиболее частые заболевания сердечно-сосудистой системы и их осложнения. Так, длительное применение традиционных противодиабетических препаратов у пациентов с СД2 сопровождается постепенным снижением функции β-клеток и ухудшением показателей гликемии, что создает предпосылки для прогрессирования поздних диабетических осложнений.
Серьезным препятствием на пути снижения риска ССО у больных, получающих инсулинотерапию, является высокая частота таких нежелательных явлений, как гипогликемия и увеличение массы тела, что может приводить к росту числа острых сердечно-сосудистых событий.
Эти обстоятельства были учтены в решении Управления по контролю качества пищевых продуктов и лекарственных средств США 2008 г. касательно повышения требований к регистрации новых антигипергликемических препаратов, которые должны не только снижать уровень гликемии, но и обладать безопасным кардиологическим профилем2.
В соответствии с современными отечественными клиническими рекомендациями, для улучшения качества лечения пациентов с СД2 и сопутствующими ССЗ целесообразно применять противодиабетические препараты, обеспечивающие снижение сердечно-сосудистого риска. Эта цель может быть достигнута не только за счет контроля углеводного обмена при минимальном риске развития гипогликемий, но и благодаря плейотропным эффектам в виде дополнительного снижения массы тела, АД, улучшения показателей липидного спектра, а также положительного влияния на миокард, почки и артериальное сосудистое русло. Результатом такого подхода станет улучшение клинических исходов лечения пациентов с СД2 — уменьшение смертности, частоты инфарктов и инсультов, госпитализаций и т. д.
Новые требования, предъявляемые к сахароснижающим препаратам, привели к инициации множества крупных рандомизированных исследований, направленных на изучение сердечно-сосудистой безопасности новых лекарственных препаратов для лечения СД2. Одной из таких групп препаратов, относящихся к инкретиновым, стали агонисты рецепторов глюкагоноподобного пептида 1 типа (АрГПП-1), которые, кроме надежного антигипергликемического действия, продемонстрировали выраженные кардио- и нефропротективные свойства[13, 15].
В настоящее время АрГПП-1 рассматривают как возможные препараты первой линии в стартовой терапии СД2, в том числе в комбинации с другими антигипергликемическими средствами3. Механизм действия АрГПП-1 включает активизацию функции β-клеток поджелудочной железы за счет стимуляции транскрипции гена инсулина, а также экспрессии матричной РНК внутриклеточных переносчиков глюкозы — глюкокиназы и GLUT2, которые обеспечивают периферическую утилизацию глюкозы. АрГПП-1 стимулируют глюкозозависимую секрецию инсулина, подавляют апоптоз β-клеток, вызывая их гипертрофию и пролиферацию (на животных моделях), а также активизируют дифференцировку и неогенез β-клеток из эпителиальных клеток-предшественников. Кроме того, АрГПП-1 снижают секрецию глюкагона как за счет прямого воздействия на панкреатические α-клетки, так и путем увеличения секреции соматостатина, что приводит к подавлению продукции и высвобождения глюкозы из печени[16].
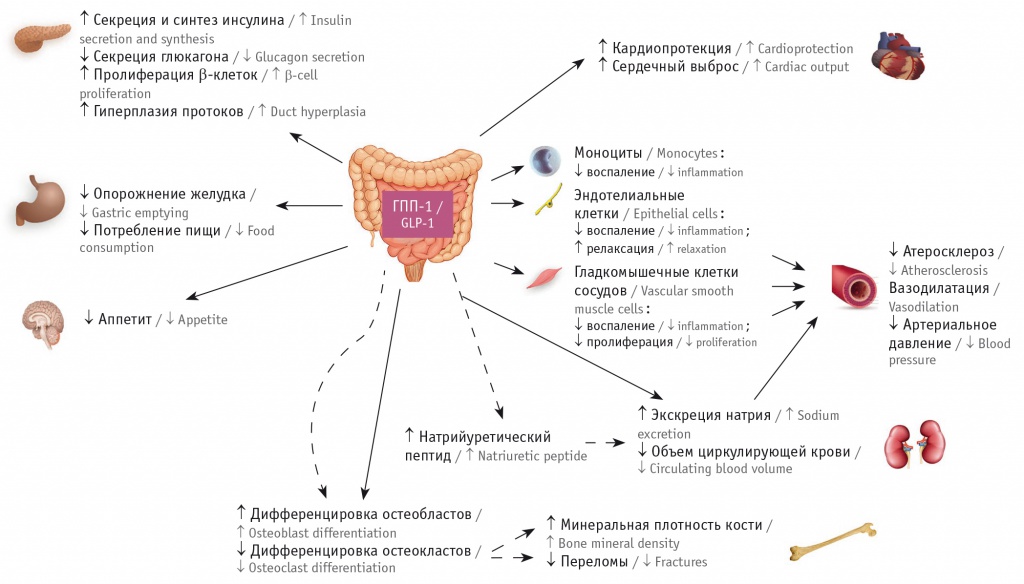
Рецепторы ГПП-1, помимо β-клеток поджелудочной железы, обнаружены в нервной системе, эндотелиальных клетках, макрофагах, желудке, костях, почках, а также в кардиомиоцитах[17]. Основные системные эффекты ГПП-1 представлены на рисунке 3.
Рис. 3. Системные эффекты глюкагоноподобного пептида 1 типа (ГГП-1) в организме (по данным[17])
МЕХАНИЗМЫ КАРДИОПРОТЕКТИВНОГО ДЕЙСТВИЯ АГОНИСТОВ РЕЦЕПТОРОВ ГЛЮКАГОНОПОДОБНОГО ПЕПТИДА 1 ТИПА
Накопленные к настоящему времени результаты клинических и экспериментальных исследований позволяют говорить о множественных влияниях инкретиномиметиков на сердечно-сосудистую систему. Кардиотропное действие препаратов данной группы осуществляется за счет активации рецепторов к ГПП-1 в кардиомиоцитах. Кроме того, кардиопротективный эффект АрГПП-1 обусловлен увеличением уровней антиоксиданта гемсинтетазы 1, ингибитора апоптоза Bcl-2, а также фосфорилированной серин-треониновой киназы Akt, что способствует восстановлению толщины стенки сердца после перенесенной ишемии и улучшению функции кардиомиоцитов[18].
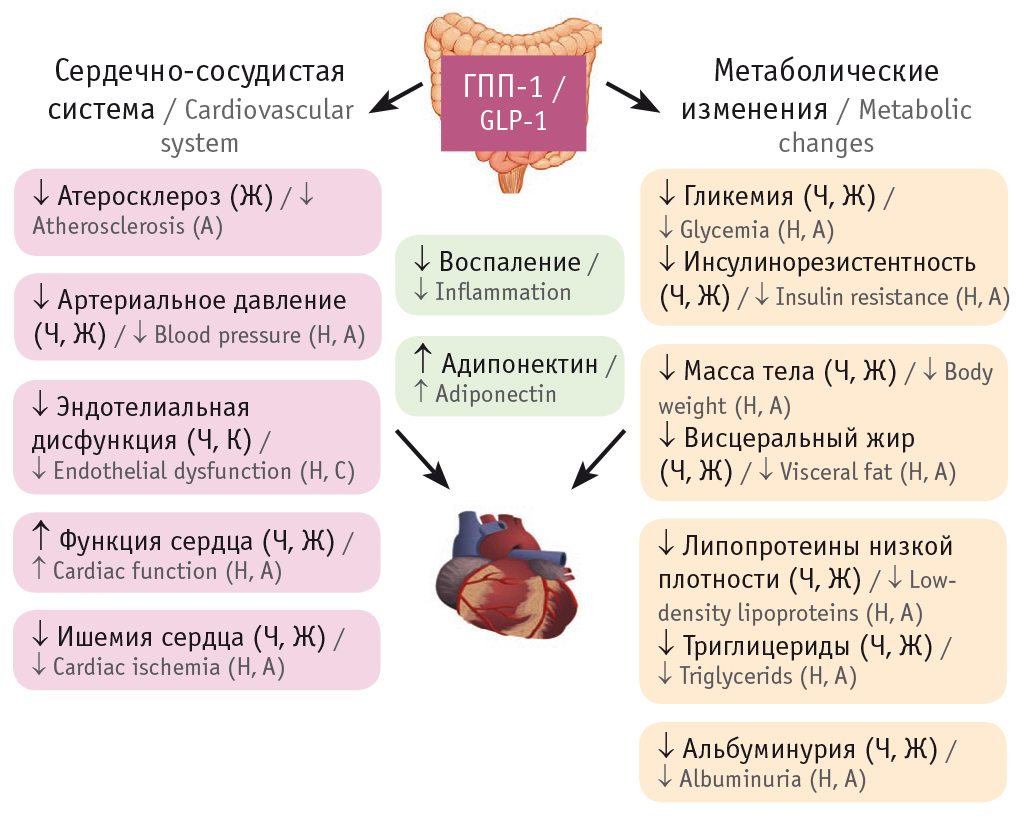
Получены данные о дозозависимом увеличении выработки NO в культуре эндотелиальных клеток за счет активации эндотелиальной NO-синтазы, а также о сопутствующем угнетении экспрессии генов молекул клеточной адгезии и маркеров воспаления (VCAM-1, E-селектина, ICAM-1, хемоаттракционного белка моноцитов 1)[19]. Эти механизмы объясняют положительные сердечно-сосудистые эффекты представителей класса АрГПП-1. Потенциальные пути влияния ГПП-1 на сердечно-сосудистую систему представлены на рисунке 4.
Рис. 4. Потенциальные пути влияния глюкагоноподобного пептида 1 типа (ГПП-1) на сердечно-сосудистую систему (по данным[17]).
Примечание: Ч — исследования у человека, Ж — исследования у животных, К — исследования на культуре клеток
В зависимости от продолжительности эффекта используемые в настоящее время в клинической практике лекарственные препараты из класса АрГПП-1 можно разделить на две группы: короткого действия, имеющие разные периоды полувыведения, но требующие введения 1–2 раза в сутки (эксенатид, ликсисенатид, лираглутид), и длительного действия, кратность введения которых составляет 1 раз в неделю (эксенатид пролонгированного действия, дулаглутид, семаглутид, албиглутид). Все они реализуют свои эффекты за счет стимуляции секреции инсулина и угнетения секреции глюкагона, а также усиления чувства насыщения после приема пищи.
При использовании в качестве средств монотерапии препараты данного класса характеризуются низким риском гипогликемии, способностью снижать массу тела, а также риски сердечно-сосудистых и почечных осложнений. АрГПП-1 длительного действия обладают несколько более высокой эффективностью в достижении целевых показателей HbA1c, а также нормализации уровня гликемии натощак, чем короткодействующие АрГПП-1.
Применение препаратов АрГПП-1 в клинической практике показало их хорошую переносимость и низкую частоту нежелательных явлений в виде отдельных случаев тахикардии и диспепсических явлений (тошноты и дискинезии желчевыводящих путей). Изредка отмечены случаи развития острого панкреатита. По результатам исследования SUSTAIN 6 (Trial to Evaluate Cardiovascular and Other Long-term Outcomes with Semaglutide in Subjects with Type 2 Diabetes), частота формирования диабетической ретинопатии среди пациентов из группы лечения семаглутидом в дозах 0,5 мг или 1 мг оказалась выше (3%), чем в группе плацебо (1,8%)[20].
При инициации терапии следует обучать пациентов методике выполнения инъекции, а также правилам борьбы с возможными диспепсическими явлениями (дробное питание, уменьшение объема потребляемой за один прием пищи4).
КАРДИОПРОТЕКТИВНЫЕ ЭФФЕКТЫ АГОНИСТОВ РЕЦЕПТОРОВ ГЛЮКАГОНОПОДОБНОГО ПЕПТИДА 1 ТИПА В ИССЛЕДОВАНИЯХ СЕРДЕЧНО-СОСУДИСТОЙ БЕЗОПАСНОСТИ
При проведении клинических и экспериментальных исследований получены обширные сведения о позитивном влиянии АрГПП-1 на факторы сердечно-сосудистого риска, показатели гемодинамики и функцию сердца у пациентов с СД2. Вместе с тем в последние годы в ходе завершившихся масштабных исследований кардиоваскулярной безопасности получены убедительные данные о различном воздействии препаратов класса АрГПП-1 на конечные сердечно-сосудистые и почечные точки, что позволило выделить наиболее предпочтительные препараты этой группы.
В 2016 г. завершено крупное рандомизированное исследование LEADER (Liraglutide Effect and Action in Diabetes: Evaluation of Cardiovascular Outcome Results) с участием более 9 тыс. пациентов с СД2 и высоким сердечно-сосудистым риском (с наличием по меньшей мере одного сердечно-сосудистого заболевания — ИБС, цереброваскулярной болезни, атеросклеротического поражения периферических сосудов, хронической болезни почек 3-й стадии и выше либо ХСН II и III функционального класса). Период наблюдения — более 5 лет. Всех пациентов разделили в соотношении 1 : 1 на группы лечения 1,8 мг (или максимальной переносимой дозой) лираглутида и плацебо в дополнение к стандартной сахароснижающей терапии. Результаты исследования показали, что при применении лираглутида ОР больших нежелательных сердечно-сосудистых явлений (MACE), включая сердечно-сосудистую смерть, нефатальный инфаркт миокарда и нефатальный мозговой инсульт, был статистически значимо (на 13%) ниже, риск сердечно-сосудистой смерти — на 22%, смерти от всех причин — на 15% ниже, чем в группе плацебо.
При оценке влияния лираглутида на риск госпитализаций по поводу ХСН отмечено, что ОР в группе лираглутида был на 13% меньше, чем в группе плацебо (p = 0,14)[21].
Долгосрочные сердечно-сосудистые результаты и иные конечные точки безопасности другого представителя группы препаратов АрГПП-1 семаглутида в дозах 0,5 мг и 1,0 мг изучали в исследовании SUSTAIN-6, которое завершилось в 2016 г. Всего в этом исследовании рандомизировали более 3 тыс. пациентов с СД2, которые получали лечение в течение 104 недель. Исследование SUSTAIN-6 показало, что частота больших нежелательных сердечно-сосудистых явлений (MACE) была статистически значимо (на 26%) ниже в группе активного лечения, чем в группе плацебо, что объяснялось значимым уменьшением распространенности нефатального мозгового инсульта (на 39%) и незначимым — нефатального инфаркта (на 26%). При этом различия между группами лечения по частоте сердечно-сосудистой смерти отсутствовали[22].
В 2015 г. были представлены результаты еще одного проспективного исследования сердечно-сосудистой безопасности АрГПП1 ликсисенатида — ELIXA (Evaluation of LIXisenatide in Acute Coronary Syndrome) (6068 участников: группа ликсисенатида — 3034; группа плацебо — 3034; средний возраст — 60 лет, средняя длительность СД2 — 9,3 года)[23]. В это многоцентровое рандомизированное двойное слепое плацебо-контролируемое исследование включили больных с СД2 и острым коронарным синдромом (83% — острый инфаркт миокарда, 17% — нестабильная стенокардия). Исходно у 22,3% в группе плацебо и у 22,5% больных группы ликсисенатида имелись проявления ХСН.
В результате различия по первичной конечной точке (сердечно-сосудистая смерть, нефатальный инфаркт миокарда, нефатальный инсульт или госпитализация по поводу нестабильной стенокардии) обнаружены не были (13,4% и 13,2% соответственно; ОР = 1,02; 95%-ный ДИ: 0,89–1,17). Анализ составляющих вторичной конечной точки показал, что частота госпитализаций по поводу ХСН также не различалась в группах (ОР = 0,96; 95%-ный ДИ: 0,75–1,23).
Одним из важнейших исследований последнего времени, посвященных изучению кардиопротективных эффектов АрГПП-1, стало REWIND (Researching cardiovascular Events with a Weekly INcretin in Diabetes), которое проводилось с целью оценки влияния АрГПП-1 пролонгированного действия дулаглутида в еженедельной дозе 1,5 мг на риск ССО у взрослых больных СД2 по сравнению с плацебо. В данном исследовании принимали участие более 9900 пациентов с СД2 со средней продолжительностью заболевания около 10 лет[24]. Особенностью исследования REWIND было то, что лишь 31% больных исходно имели ССЗ (перенесенный инфаркт миокарда, ишемический инсульт, нестабильную стенокардию, операции по реваскуляризации коронарных, сонных или периферических сосудов, госпитализацию по поводу ИБС с нестабильной стенокардией или зарегистрированной ишемией миокарда)[24, 25].
Анализ результатов исследования REWIND показал значимое положительное влияние дулаглутида на уровни HbA1c и холестерина ЛПНП, систолическое АД, массу тела (данные представлены на рисунке 5).
Рис. 5. Влияние дулаглутида на факторы сердечно-сосудистого риска по результатам исследования REWIND[24].
Примечание: ДИ — доверительный интервал, ЛПНП — липопротеины низкой плотности, МНК —` метод наименьших квадратов, САД — систолическое артериальное давление, HbA1c — гликированный гемоглобин
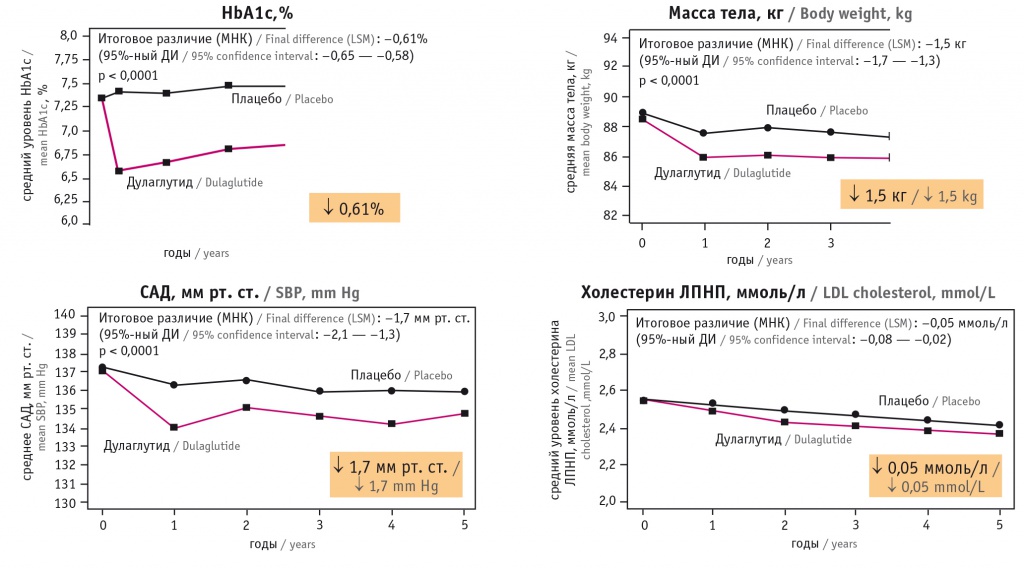
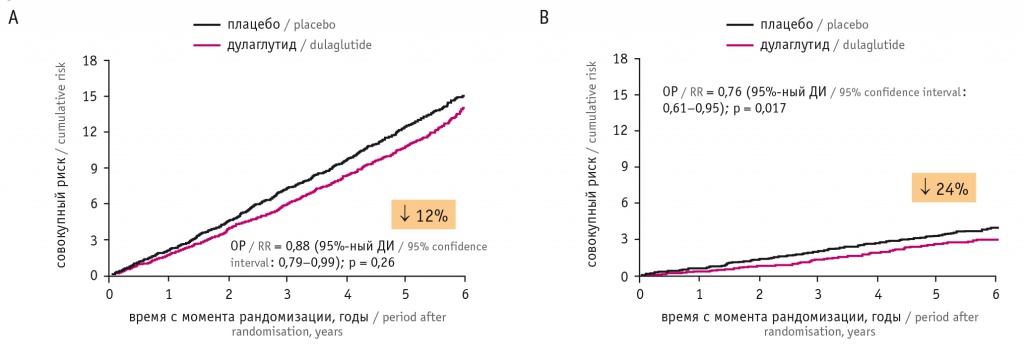
Кроме того, дулаглутид снижал частоту наступления первичной трехкомпонентной сердечно-сосудистой точки 3P-MACE на 12%, а нефатальных инсультов — на 24% (рис. 6).
Рис. 6. Влияние дулаглутида на частоту трехкомпонентной сердечно-сосудистой точки 3P-MACE (А) и нефатальных инсультов (В) по результатам исследования REWIND[24].
Примечание: ДИ — доверительный интервал, ОР — относительный риск
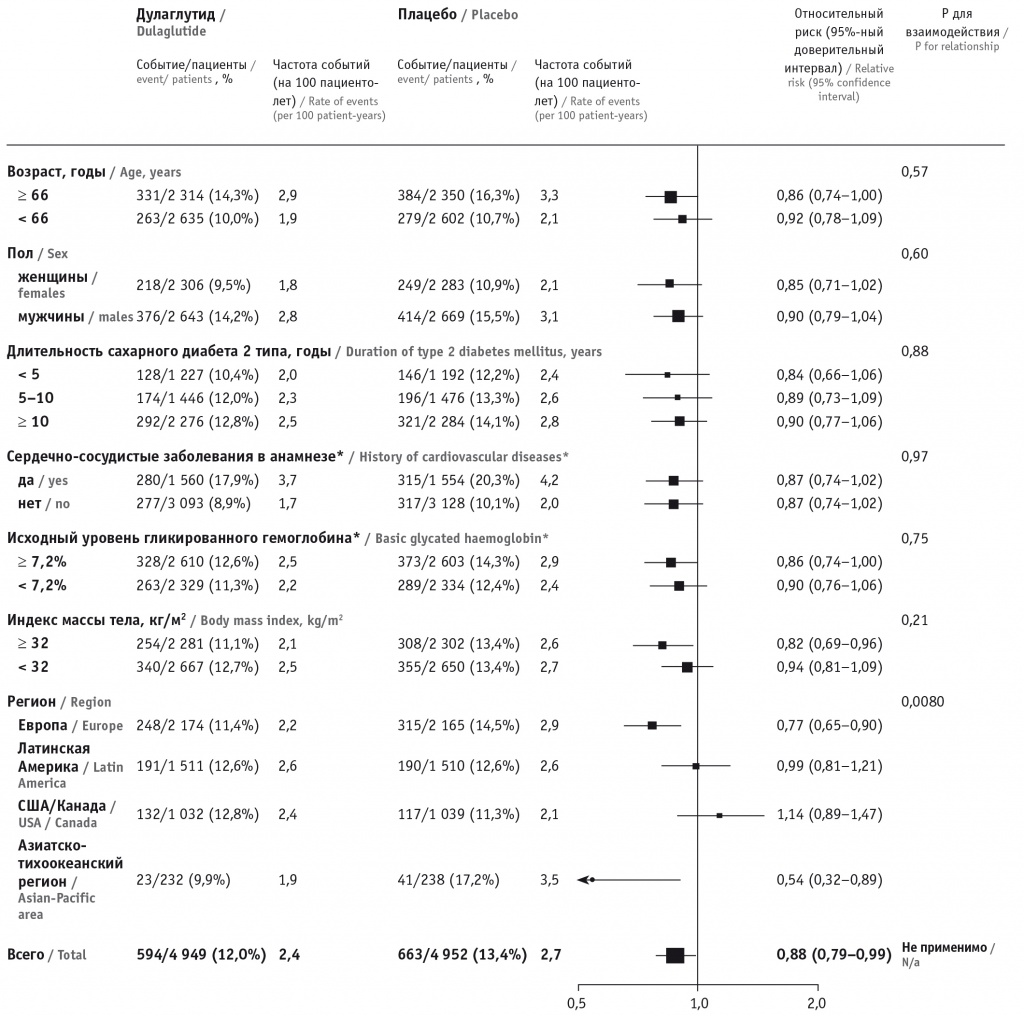
Особое значение имеет субанализ данных REWIND, в котором изучалась эффективность дулаглутида в отдельных подгруппах пациентов, выделенных в зависимости от сердечно-сосудистого анамнеза. Показано, что снижение частоты 3Р-MACE происходило независимо от наличия в анамнезе пациентов ССЗ (p = 0,97) (рис. 7).
Рис. 7. Частота достижения 3P-MACE в разных подгруппах пациентов, по данным субанализа результатов исследования REWIND[24].
* Пациенты не включались в группу, если необходимые критерии или результаты исследования были неизвестны
Полученные результаты свидетельствуют о возможности использования дулаглутида как для вторичной, так и для первичной профилактики ССО у пациентов с СД2, что послужило основанием для внесения изменений в инструкцию по медицинскому применению препарата. Помимо этого, дулаглутид значимо (на 15%) уменьшил частоту композитной почечной точки (включавшей новые случаи макроальбуминурии, снижение на 30% скорости клубочковой фильтрации (СКФ) или начало заместительной почечной терапии) (p = 0,0004).
Таким образом, полученные данные позволяют сделать вывод о наличии у дулаглутида выраженных кардио- и нефропротективного эффектов в популяции пациентов СД2, большинство которых ранее не имели ССЗ атеросклеротического генеза.
На основании результатов исследования REWIND действующий Консенсус Американской диабетической ассоциации и Европейской ассоциации по изучению диабета предложил использовать АрГПП-1 при неэффективности метформина у пациентов с атеросклеротическими ССЗ, а также у больных
без них, но с факторами высокого риска (возраст 55 лет и старше, стеноз сонных артерий, артерий нижних конечностей или коронарных артерий > 50%, гипертрофия левого желудочка, СКФ < 60 мл/мин, альбуминурия)[26].
Европейское общество кардиологов в своих рекомендациях еще более расширило показания к применению АрГПП-1, рекомендовав их в качестве терапии первой линии у пациентов с атеросклеротическими ССЗ, а также у лиц с высоким и очень высоким сердечно-сосудистым риском (т. е. при сочетании трех и более больших факторов риска либо при наличии СД2 без поражения органов-мишеней в сочетании с любым другим дополнительным фактором риска)[27].
Согласно этим международным рекомендациям, более 60% пациентов с СД2 соответствуют критериям для назначения АрГПП-1. По мнению Управления по контролю качества пищевых продуктов и лекарственных средств США, среди всех представителей группы АрГПП-1 только дулаглутид может применяться как для вторичной, так и для первичной профилактики ССО у взрослых пациентов с СД25.
ЗАКЛЮЧЕНИЕ
Итак, очевидно, что для снижения смертности населения трудоспособного возраста, в том числе смертности от болезней системы кровообращения, целесообразно уделять особое внимание не только вторичной, но и первичной профилактике сердечно-сосудистых осложнений. Это требует перехода от преобладающего использования традиционных схем сахароснижающей терапии на основе метформина, препаратов сульфонилмочевины и инсулинов к раннему назначению инновационных препаратов, включая агонисты рецепторов глюкагоноподобного пептида 1 типа (АрГПП-1). Результаты проведенных исследований кардиоваскулярной безопасности показали, что АрГПП-1, в том числе дулаглутид, обладают доказанными преимуществами в отношении влияния на сердечно-сосудистые исходы. Это определяет их приоритетное использование в современных алгоритмах терапии пациентов с СД 2 типа. Применение АрГПП-1 может существенно увеличить эффективность не только вторичной, но и первичной профилактики сердечно-сосудистых осложнений.
Поступила: 05.03.2021
Принята к публикации: 23.03.2021
_______
1 International Diabetes Federation. IDF Diabetes Atlas. 2019. URL: https://www.diabetesatlas.org/upload/resources/material/20200302_133351_IDFATLAS9e-final-web.pdf (дата обращения — 05.04.2021); U.S. Department of Health and Human Services Centers for Disease Control and Prevention. National Diabetes Statistics Report 2020. Estimates of diabetes and its burden in the United States. 2020. URL: https://www.cdc.gov/diabetes/pdfs/data/statistics/national-diabetes-statistics-report.pdf (дата обращения — 05.04.2021).
2 U.S. Food and Drug Administration. Guidance for industry. Diabetes mellitus — evaluating cardiovascular risk in new antidiabetic therapies to treat type 2 diabetes, December 2008. URL: https://www.fda.gov/media/71297/download (дата обращения — 15.02.2021).
3 U.S. Food and Drug Administration. Guidance for industry. Diabetes mellitus — evaluating cardiovascular risk in new antidiabetic therapies to treat type 2 diabetes, December 2008...
4 Medication Guide TRULICITY® (TRU-li-si-tee) (dulaglutide) injection, for subcutaneous use. US Food and Drug Administration. Revised. 2020. URL: https://www.accessdata.fda.gov/drugsatfda_docs/label/2020/125469s033lbl.pdf#page=26 (дата обращения — 15.01.2021).
5 Medication Guide TRULICITY® (TRU-li-si-tee) (dulaglutide) injection, for subcutaneous use…








