Острый панкреатит и обострение хронического панкреатита характеризуются некрозом ацинарных клеток поджелудочной железы в результате их самопереваривания с развитием воспаления и, впоследствии, фиброза. Таким образом, повреждающее действие собственных ферментов поджелудочной железы выступает в качестве одного из основных и начальных факторов патогенеза заболевания. Снижение секреции поджелудочной железы (создание «функционального покоя») является одним из принципов консервативного лечения острого панкреатита и обострения хронического панкреатита[4].
Для реализации данного принципа могут быть использованы разные способы: голод, эвакуация желудочного сока тонким зондом, зондовое энтеральное питание, парентеральное питание, медикаментозное лечение — октреотид, холинолитики, блокаторы желудочной секреции, в том числе ингибиторы протонной помпы (ИПП). Блокада синтеза соляной кислоты приводит к повышению рН в двенадцатиперстной кишке, что обеспечивает уменьшение выработки естественных стимуляторов активности поджелудочной железы — секретина и холецистокинина. Происходит снижение секреции поджелудочной железы с уменьшением протокового и тканевого давления, что приводит к редукции отека и болевых ощущений[2, 4].
Скорость наступления кислотоблокирующего эффекта может быть одним из факторов, определяющих эффективность лечения: эффект действия ИПП при пероральном применении далеко не всегда развивается в первый день терапии, нередко максимальное снижение секреции соляной кислоты достигается лишь к 3–5-му дню лечения, когда сроки возможного эффективного воздействия упущены. Будет логичным предположение, что инъекционное введение ИПП более эффективно, чем пероральное.
Цель исследования: сравнительная оценка эффективности инъекционного и перорального применения ИПП пантопразола (Панум®) при курсовом лечении больных острым панкреатитом или с обострением хронического панкреатита.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проведено в ГКБ № 51 (на клинической базе Учебно-научного медицинского центра Управления делами Президента РФ). В него было включено 30 пациентов с острым или обострением хронического панкреатита.
Критерии включения
- Возраст старше 18 лет.
- Клинические и ультразвуковые критерии острого панкреатита или обострения хронического панкреатита.
Критерии исключения
- Злокачественные заболевания ЖКТ.
- Тяжелые сопутствующие заболевания сердечно-сосудистой системы, органов дыхания, почек и печени; психические заболевания; злокачественные заболевания или ВИЧ-инфекция.
- Беременность, в том числе беременность, планируемая во время данного исследования.
- ЖКБ, билиарнозависимый панкреатит.
- В исследование не включались пациенты, применявшие изучаемый препарат за 30 или менее дней до начала исследования, а также пациенты, которые, как ожидалось, должны были применять изучаемый препарат в рамках другого исследования.
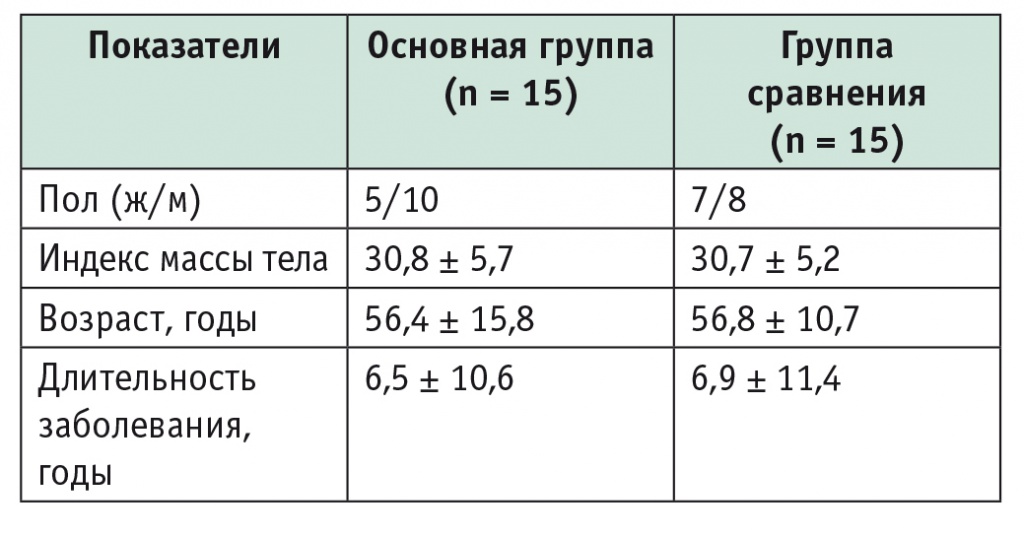
В основной группе и в группе сравнения было по 15 пациентов, распределенных случайным образом (табл. 1). Представленные в таблице 1 данные свидетельствуют о том, что группы были сопоставимы по полу, возрасту и длительности заболевания.
Таблица 1
Характеристика пациентов основной и контрольной групп
Пациентам, включенным в исследование, назначали препарат Панум® в инъекционной или таблетированной форме. Препарат Панум® (пантопразол, производство «Юник Фармасьютикал Лабораториз» — отделения фирмы «Дж. Б. Кемикалс энд Фармасьютикалс Лтд») представлен в двух лекарственных формах: лиофилизата для приготовления раствора для внутривенных инъекций и таблеток.
Основная группа (15 больных) 5 дней получала препарат Панум® в дозе 40 мг 2 раза в сутки внутривенно медленно с последующим переходом на пероральный прием в дозе 40 мг 2 раза в день в течение 20 дней в составе комплексной терапии. Последняя предусматривала дезинтоксикационную терапию, ферментные препараты и анальгетики по требованию. Группа сравнения включала 15 больных острым панкреатитом или с обострением хронического панкреатита, которые в составе комплексной терапии получали только таблетированную форму препарата Панум® в аналогичных дозах в течение 25 дней.
В задачи исследования входили:
- оценка клинической эффективности препарата (по динамике симптомов);
- изучение изменения ультразвуковой картины к окончанию терапии;
- исследование качества жизни (по данным визуальной аналоговой шкалы — ВАШ);
- определение переносимости и побочных эффектов препарата Панум®.
Контроль клинических, ультразвуковых показателей и оценку качества жизни по данным ВАШ проводили до лечения, на 5-й и 25-й дни терапии. Изучение результатов клинического и биохимического анализов крови осуществляли до и после лечения.
Динамика симптомов в баллах отражалась пациентами в индивидуальных дневниках по следующей градации:
- 1 балл — симптом отсутствует;
- 2 балла — выраженность симптома слабая (можно не замечать, если не думать);
- 3 балла — выраженность симптома умеренная (не удается не замечать, но не нарушает дневную активность или сон);
- 4 балла — выраженность симптома сильная (нарушает дневную активность или сон);
- 5 баллов — выраженность симптома очень сильная (значительно нарушает дневную активность или сон, требуется отдых).
При оценке эффективности терапии учитывали субъективные жалобы пациента (болевой синдром, диспептический синдром, частота стула) и сроки наступления эффекта (скорость купирования симптомов) на фоне терапии препаратом Панум® по данным индивидуального дневника пациента. Для определения срока наступления эффекта на фоне терапии препаратом Панум® регистрировали день приема препарата, когда было отмечено уменьшение интенсивности симптома на 1 балл и более.
Общую эффективность терапии оценивали по следующим параметрам:
- 1 — отличная эффективность, лечение приводит к полному разрешению болей и/или нормализации УЗИ-данных, не вызывая осложнений или побочных реакций;
- 2 — хорошая эффективность, лечение приводит к уменьшению болей на 1 балл и более и к положительной динамике ультразвуковой картины;
- 3 — удовлетворительная эффективность, лечение приводит к уменьшению болей на 1 балл и более при отсутствии положительной динамики ультразвуковой картины.
Зарегистрированные в рамках исследования данные представлены в виде среднего значения (М) и стандартного отклонения (СО, σ) для количественных переменных, а также в виде процентов по частотным показателям для качественных переменных. Результаты исследования проанализированы с помощью компьютерной программы Statistica 6.0 (StatSoft, США) с применением параметрических и непараметрических методов статистического анализа (критерий Стьюдента, критерий Вилкоксона) в зависимости от вида переменной. При значениях p < 0,05 различия считали статистически значимыми.
РЕЗУЛЬТАТЫ
Оценка клинической эффективности
Клиническую эффективность оценивали по динамике симптомов, сравнивали средние значения симптома по пятибалльной шкале исходно, к 5-му и 25-му дням лечения (табл. 2).
Таблица 2
Оценка клинической эффективности лечения (М ± σ), баллы
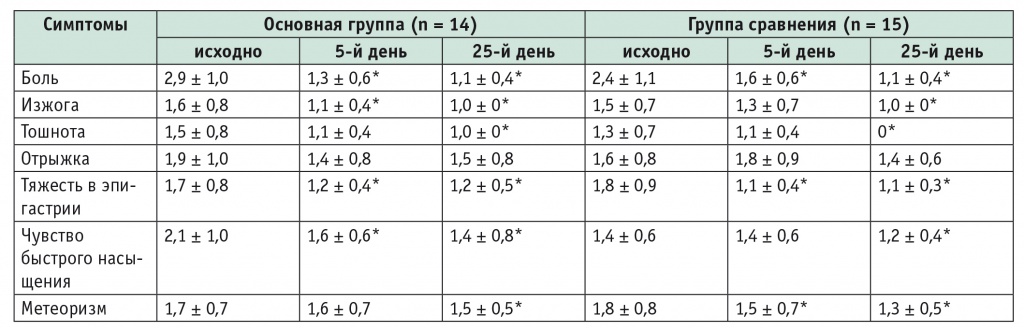
Примечания.
- Один пациент основной группы выбыл из исследования.
- Знаком (*) отмечены статистически значимые различия с исходным показателем в группе (p < 0,05).
Как видно из таблицы 2, исходные показатели интенсивности симптомов в группах были сопоставимы. К 5-му дню лечения в отношении практически всех симптомов отмечалась положительная динамика. Статистически значимое уменьшение интенсивности боли наблюдалось к 5-му дню терапии. Степень уменьшения была одинаковой в основной и контрольной группах, однако сроки наступления эффекта в основной группе составили 3,2 ± 1,7 дня, в то время как в группе сравнения — 5,5 ± 2,2 дня (различия статистически значимы: t = 2,7; р = 0,01).
Более выраженный эффект инъекционной формы препарата наблюдали и в отношении изжоги и чувства быстрого насыщения: статистически значимое уменьшение интенсивности этих симптомов в основной группе отметили к 5-му дню лечения. В группе сравнения аналогичные результаты были получены только к 25-му дню лечения.
Сходный положительный эффект терапии в обеих группах отметили при изучении динамики выраженности тошноты и чувства тяжести в эпигастрии после еды. В отношении метеоризма более выраженная положительная динамика была получена в группе сравнения.
Таким образом, применение препарата Панум® в терапии больных острым панкреатитом и с обострением хронического панкреатита сопровождалось достоверным уменьшением/исчезновением болевого и диспептического синдромов. Динамика симптомов в группах была сходной, однако более быстрый эффект был получен при использовании инъекционной формы препарата в первые 5 дней лечения.
Динамика ультразвуковой картины
Результаты УЗИ, отражающие динамику размеров поджелудочной железы в исследуемых группах, представлены в таблице 3.
Таблица 3
Динамика размеров поджелудочной железы на фоне лечения (М ± σ), мм
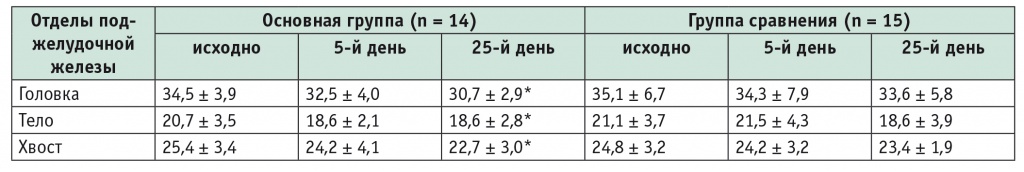
Примечание. Знаком (*) отмечены статистически значимые различия с исходным показателем в группе (p < 0,05).
Приведенные данные свидетельствуют о положительной динамике размеров поджелудочной железы к окончанию лечения. При этом в основной группе средние размеры поджелудочной железы к концу терапии практически нормализуются (размеры в норме: головка — 30 мм, тело — 20 мм, хвост — 25 мм). Уменьшение размеров головки, тела и хвоста железы является статистически значимым. В группе сравнения отличия средних размеров поджелудочной железы к 25-му дню терапии от исходных показателей статистически значимыми не являются, несмотря на явную тенденцию к уменьшению.
Таким образом, применение инъекционной формы препарата Панум® в первые 5 дней лечения оказало более выраженное положительное влияние на отек и воспаление поджелудочной железы, о чем свидетельствует достоверное уменьшение ее размеров к концу терапии.
Динамика качества жизни
Результаты изучения качества жизни по данным ВАШ представлены на рисунке 1.
Рис. 1. Динамика качества жизни по данным визуальной аналоговой шкалы (ВАШ), мм.
* Различия с исходным показателем в группе статистически значимы
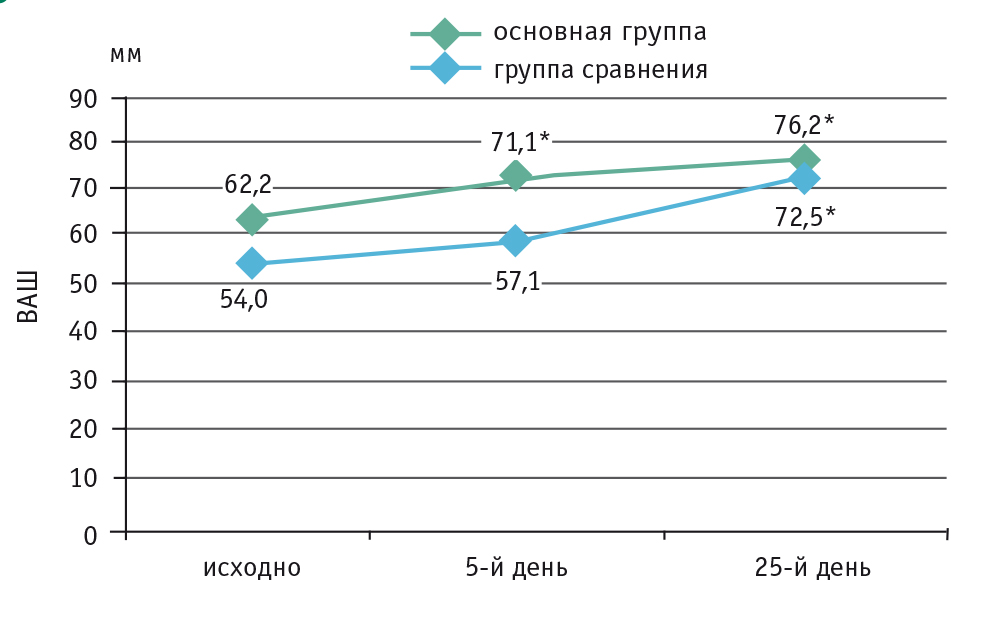
Статистически значимых различий между группами в исходных показателях ВАШ не выявлено. Достоверное улучшение показателей ВАШ в основной группе наблюдали уже к 5-му дню лечения, в эти же сроки в группе сравнения отчетливой положительной динамики не отмечено. К 25-му дню лечения достоверное улучшение было достигнуто в обеих группах.
Переносимость и побочные эффекты препарата Панум®
У 3 пациентов (1 пациента из основной группы и двоих — из группы сравнения) в ходе лечения отмечались явления диспепсии (горечь во рту, тошнота), которые могли иметь связь с исследуемым препаратом или быть проявлением основного заболевания. У данных больных переносимость оценена как хорошая, так как симптомы прошли самостоятельно, без использования вспомогательного лечения.
В одном случае инъекции препарата были отменены в связи с развитием болей средней интенсивности в эпигастрии, которые возникали вскоре после начала введения препарата и прекращались через 20 минут после окончания введения. Боли возникали при каждом введении, были выполнены 3 инъекции, после чего от введения препарата отказались. В данном случае переносимость препарата расценена как плохая.
У остальных пациентов переносимость препарата была отличной.
В рамках исследования безопасности использованного препарата проводилось изучение показателей клинического (количества гемоглобина, эритроцитов, лейкоцитов и тромбоцитов) и биохимического анализов крови. Каких-либо изменений в изучаемых показателях крови не наблюдали. Динамика биохимических показателей крови представлена в таблице 4.
Таблица 4
Динамика биохимических показателей исследуемых больных, n = 29
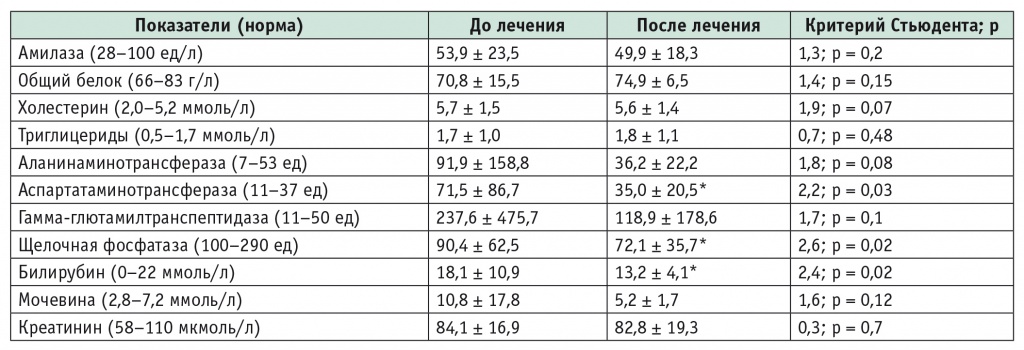
Примечание. Знаком (*) отмечены статистически значимые различия с исходными показателями (p < 0,05).
Исходное повышение средних значений трансаминаз и гамма-глютамилтранспептидазы объясняется сопутствующей патологией печени (у 9 больных имел место алкогольный стеатогепатит, у 3 — компенсированный цирроз печени). После курса лечения уровни АСТ, щелочной фосфатазы и билирубина статистически значимо снизились, что было связано с улучшением состояния печени, при этом негативного влияния препарата на биохимические показатели не наблюдалось.
Оценка эффективности лечения
Данные по оценке эффективности лечения согласно приведенным выше критериям представлены в таблице 5.
Таблица 5
Эффективность лечения в основной группе и группе сравнения, n (%)
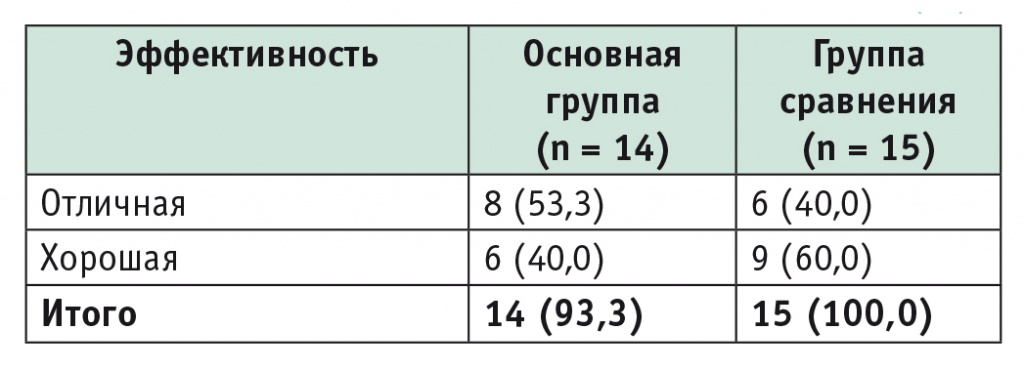
Примечание. Один пациент основной группы выбыл из исследования.
Как показано, отличная и хорошая эффективность в основной группе и группе сравнения составила 93,3% и 100% соответственно.
ОБСУЖДЕНИЕ
Настоящее исследование было выполнено для сравнительной оценки эффективности инъекционного и перорального применения препарата Панум® при курсовом лечении больных острым панкреатитом и с обострением хронического панкреатита.
Наиболее эффективно подавляют секрецию соляной кислоты ИПП. Пероральное применение препаратов этой группы характеризуется относительно медленным началом действия. Стабильный кислотосупрессивный эффект развивается к 3–5-му дню лечения [8]. Конечный эффект определяется абсорбцией препарата и зависит от приема пищи (прием препарата за 30–60 минут до еды является оптимальным, так как ИПП действуют на функционирующие обкладочные клетки)[10].
Больные острым панкреатитом и с обострением хронического панкреатита нередко имеют нарушения переваривания и всасывания, а основной диетической рекомендацией при ведении таких пациентов в первые несколько дней является голодание. В этих условиях эффект ИПП при пероральном приеме может быть существенно снижен. Внутривенное введение приводит к более быстрому и полному подавлению желудочной секреции по сравнению с пероральным применением препарата, так как не зависит от всасывания и состояния моторики верхних отделов ЖКТ. После внутривенного введения пантопразол начинает действовать через 15 минут, причем введение 80 мг подавляет секрецию на 86% уже через 60 минут[1].
Еще одним из основных принципов консервативного лечения является купирование прогрессирования отечно-интерстициальной стадии панкреатита с целью предотвращения развития «хирургических» осложнений[3]. Этот принцип может быть реализован при максимально быстром воздействии на основные патогенетические факторы заболевания, в том числе и на подавление желудочной секреции. Поэтому скорость наступления кислотосупрессивного эффекта может определять эффективность терапии больных острым панкреатитом и с обострением хронического панкреатита, влиять как на темпы купирования болевого синдрома, так и на прогноз.
Разные группы ИПП различаются между собой по скорости и продолжительности кислотоблокирующего эффекта, а также по влиянию на метаболизм других препаратов, расщепляющихся с участием системы цитохрома Р450. Под действием ИПП протонная помпа инактивируется, однако затем ее активность вновь возвращается к прежнему уровню[5]. После приема лансопразола полупериод восстановления выработки кислоты составляет 12,9 часа; омепразола и рабепразола — 27,5 часа, а пантопразола — 45,9 часа[7]. Эти различия обусловлены продолжительностью сохранения связей ИПП с остатками цистеина АТФазы. Омепразол и остальные препараты взаимодействуют с остатками цистеина в положении 813, лансопразол — с цистеином 321, пантопразол — с цистеином 822. Цистеин 822 обеспечивает устойчивость связывания, поэтому продолжительность действия пантопразола больше по сравнению с другими ИПП[9].
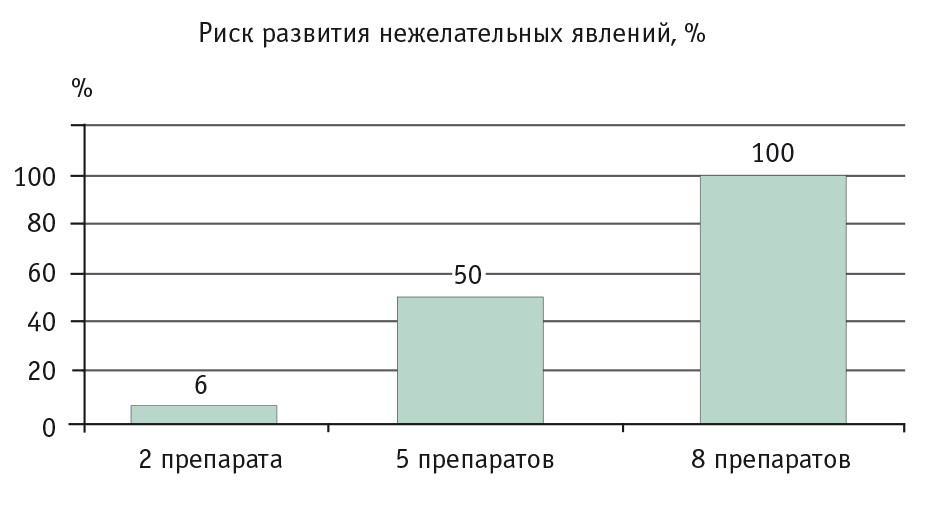
Метаболизм всех ИПП происходит в печени при участии цитохрома Р450. Большинство ИПП влияют на метаболизм многих лекарственных средств, таких как диазепам, фенитоин, варфарин, β-адреноблокаторы, дигоксин, теофиллин, диклофенак, кларитромицин, клопидогрел и др.[1]. При необходимости сочетанного приема нескольких препаратов целесообразно использовать пантопразол, который оказывает минимальное влияние на микросомальные ферменты гепатоцитов. Полипрагмазия достаточно часто встречается у больных хроническим панкреатитом, в лечении которых могут быть востребованы самые разные группы препаратов. С ростом числа принимаемых лекарств риск нежелательных последствий межлекарственного взаимодействия увеличивается (рис. 2)[6]. Для уменьшения этого риска предпочтение следует отдавать препарату с максимально низким потенциалом лекарственного взаимодействия — пантопразолу.
Рис. 2. Риск развития нежелательных явлений при одновременном приеме нескольких лекарственных препаратов, %
Полученные в настоящем исследовании данные свидетельствуют о том, что применение инъекционной формы препарата Панум® в течение первых 5 дней лечения больных острым панкреатитом и с обострением хронического панкреатита сопровождается более быстрым купированием болей, изжоги и чувства быстрого насыщения по сравнению с пероральным приемом препарата. Кроме того, использование инъекционной формы препарата оказывало статистически значимо более выраженное положительное влияние на отек и воспаление поджелудочной железы и на качество жизни по данным ВАШ.
ЗАКЛЮЧЕНИЕ
Препарат Панум® (как в инъекционной, так и в таблетированной форме) эффективен в лечении острого и обострения хронического панкреатита.
Использование инъекционной формы препарата Панум® в течение первых 5 дней лечения позволяет быстрее достичь блокирования секреции поджелудочной железы, уменьшения ее отека и воспаления и, соответственно, купирования болевого и диспептического синдромов по сравнению с пероральным приемом.
Включение в консервативную терапию больных острым панкреатитом и с обострением хронического панкреатита инъекционной формы препарата Панум® способствует статистически значимому улучшению качества жизни пациентов по данным ВАШ в более ранние сроки по сравнению с лечением таблетированной формой.
Препарат Панум® (как в инъекционной, так и в таблетированной форме) характеризуется преимущественно отличной и хорошей переносимостью.








