Солидная псевдопапиллярная неоплазия (СПН) поджелудочной железы (ПЖ) (опухоль Gruber — Frantz) представляет собой крайне редкую патологию, которая встречается менее чем в 0,1–2,7% случаев всех опухолей ПЖ и составляет 1–5% опухолей ее экзокринной части и 10% кистозных неоплазий[4].
Цель статьи: анализ литературных данных по изучению СПН ПЖ и собственных наблюдений.
Данный вид опухоли обладает низким потенциалом злокачественности и в 85–90% случаев имеет доброкачественный характер. Однако в 10–15% случаев малигнизации отмечают метастазирование в печень, регионарные лимфатические узлы, брыжейку кишки, сальник, брюшину. Кроме того, возможно прорастание опухоли в желудок, двенадцатиперстную кишку, селезенку и кровеносные сосуды[9].
Наиболее часто опухоль локализуется в хвосте или теле ПЖ. В литературе описано десять случаев внепанкреатической локализации СПН, чаще всего в брыжейке толстой кишки с эктопированной частью ПЖ и яичниках.
Этиология и патогенез данного заболевания в настоящее время не изучены. Известно, что клетки опухоли имеют эозинофильную цитоплазму и смешанные иммуногистохимические черты эндокринной, эпителиальной и мезенхимальной дифференцировки. Предположительно гистогенез опухоли происходит из дериватов ацинарных эндокринных клеток или колониеобразующих зародышевых клеток. Они содержат дикий тип гена k-ras, не экспрессируют р53, и, в отличие от протоковых аденокарцином, в них нет k-ras-мутаций. Вовлечение сигнальных путей Wnt/β-catenin и Notch в канцерогенез принципиально отличает СПН от протоковых аденокарцином и нейроэндокринных опухолей ПЖ.
По данным иммуногистохимических исследований клетки опухоли экспрессируют рецепторы к прогестерону, виментин, нейронспецифическую энолазу, ядерный β-катенин, α1-антитрипсин, α1-антихимотрипсин, CD10 и синаптофизин (в 20–30% случаев). В 80–100% случаев обнаруживают мутацию гена β-катенина, в результате которой в опухолевых клетках выявляется цитоплазматическая и ядерная экспрессия этого протеина[1].
И хотя наиболее часто заболевание встречается у лиц женского пола и в его патогенезе предполагается участие гормональной регуляции, иммунологические исследования не выявили различий в экспрессии рецепторов к половым гормонам и патологических характеристиках СПН у мужчин и женщин[10].
На начальных этапах развития опухоль имеет солидное строение, но в последующем в ее структуре появляются участки некроза и кровоизлияния, переходящие во вторичные кистозные полости. Причины некроза до конца не изучены. Опухоль имеет хорошо выраженную капсулу, хорошо васкуляризирована. На разрезе солидная ткань чередуется с участками некроза, кровоизлияний и кистозными полостями, по внешнему виду солидная ткань напоминает папиллярные разрастания. Микроскопически опухоль двухкомпонентная, состоит из папиллярных разрастаний и солидных полей из мелких мономорфных эпителиальных клеток с эозинофильной цитоплазмой. Встречаются пенистые макрофаги, гранулемы холестерина, кальцификаты. В строме опухоли отмечают многоядерные клетки инородных тел, кристаллы холестерина, кальцификаты и даже оссификаты. Однако в настоящее время четкие критерии злокачественности для данного типа опухолей еще не определены. Единственным значимым доказательством наличия солидной псевдопапиллярной карциномы являются метастазы.
Примерно в 89% случаев СПН встречается у женщин молодого возраста, средний возраст начала заболевания составляет 28 лет[3]. По данным ряда авторов, существуют различия в протекании заболевания у мужчин и женщин: у мужчин преобладает солидный компонент без дегенеративных изменений, в то время как у женщин при таких же размерах опухоли встречаются толстая фиброзная капсула и выраженные дегенеративные изменения, что свидетельствует о прогрессии опухоли. По результатам анализа историй болезней, проведенного с участием 1014 больных, у 137 (13,5%) лиц мужского пола частота метастазирования была в 2 раза выше и смертность в 3 раза превышала таковую у женщин. Так было продемонстрировано более агрессивное течение заболевания у мужчин[8].
Клиническая симптоматика заболевания приблизительно в 30% случаев отсутствует, клиническая картина зависит как от размера (средний размер — 5,5 см), так и от локализации опухоли. В большинстве случаев отмечают боль или дискомфорт в верхних отделах живота, пальпируемое образование в брюшной полости, а в случае разрыва капсулы и внутрибрюшного кровотечения — картину «острого живота».
Диагностировать СПН затруднительно. Как правило, опухоль случайно выявляют при проведении лучевых исследований. Данные УЗИ органов брюшной полости не являются существенными при постановке диагноза, большинство авторов основываются лишь на результатах КТ и МРТ. СПН при УЗИ визуализируется как неоднородное образование с наличием кистозных полостей и иногда кальцинатов по периферии[7]. Дополнительную информацию для постановки диагноза исследователи получают только при эндоскопической ультрасонографии (ЭУС)[2]. Этот метод диагностики, по данным M. Müller и соавт., обладает большей чувствительностью при выявлении опухолей ПЖ, особенно при их диаметре менее 3 см (94%), по сравнению с КТ (69%) и МРТ (83%)[5].
Сонографическими признаками образования являются четкая граница с окружающей тканью, солидный или смешанный солидно-кистозный компонент с наличием или отсутствием перегородок; возможно формирование кальцифицированной псевдокапсулы. Содержимое геморрагическое или некротическое. Окончательная постановка диагноза возможна при взятии и дальнейшей цитологической оценке материала, полученного во время тонкоигольной пункции под контролем ЭУС (ЭУС-ТИП).
На КТ эта опухоль имеет вид четко очерченного округлого гиподенсного образования, представленного солидным и кистозным компонентами в различных соотношениях без внутренних перегородок. Солидная часть располагается преимущественно по периферии. При контрастном усилении отмечают повышение эхогенности солидного компонента[5]. Плотность жидкостного компонента примерно соответствует плотности старых гематом. При МРТ повышается вероятность визуализации «папиллярных» структур в центре опухоли. Повышенная интенсивность сигнала на Т1-взвешенных изображениях и пониженная на Т2-взвешенных изображениях указывает на геморрагический характер содержимого.
В настоящее время радикальное лечение СПН осуществляют хирургическим путем даже при больших размерах опухоли и наличии метастазов. При ее малых размерах проводят локальную резекцию, при поражении тела и/или хвоста ПЖ — дистальную резекцию в сочетании со спленэктомией или без нее, при локализации опухоли в головке ПЖ — панкреатодуоденальую резекцию. Прогноз заболевания после оперативного лечения благоприятный[6].
Ниже приведено клиническое наблюдение, демонстрирующее трудности дифференциальной диагностики данного заболевания ПЖ.
Больная К. 49 лет поступила в отделение хирургии Московского клинического научно-практического центра с жалобами на боли в эпигастральной области. Из анамнеза известно, что боли беспокоили пациентку в течение 6 месяцев, предшествовавших моменту госпитализации.
При поступлении состояние удовлетворительное. Кожные покровы и видимые слизистые обычной окраски, чистые. При аускультации дыхание везикулярное, проводилось во все отделы. Частота дыхательных движений — 17 в минуту. Тоны сердца звучные, ритмичные. Частота сердечных сокращений — 76 уд/мин, АД — 130/90 мм рт. ст. Язык влажный, обложен белым налетом у корня. Живот не вздут, симметричный, участвовал в акте дыхания, при пальпации мягкий, умеренно болезненный в эпигастральной области. Симптомов раздражения брюшины не выявлено. Печень у края реберной дуги. Селезенка не пальпировалась.
В общем анализе крови отмечали снижение гемоглобина до 110 г/л, остальные показатели лабораторных методов исследования в пределах нормальных значений.
По данным УЗИ органов брюшной полости ПЖ увеличена за счет головки, где определялось гипоэхогенное образование с неровным нечетким контуром и размерами 30 × 40 × 29 мм. Объемное образование не было связано с сосудами. Парапанкреатические лимфатические узлы не визуализировались. Заключение: солидное образование головки поджелудочной железы.
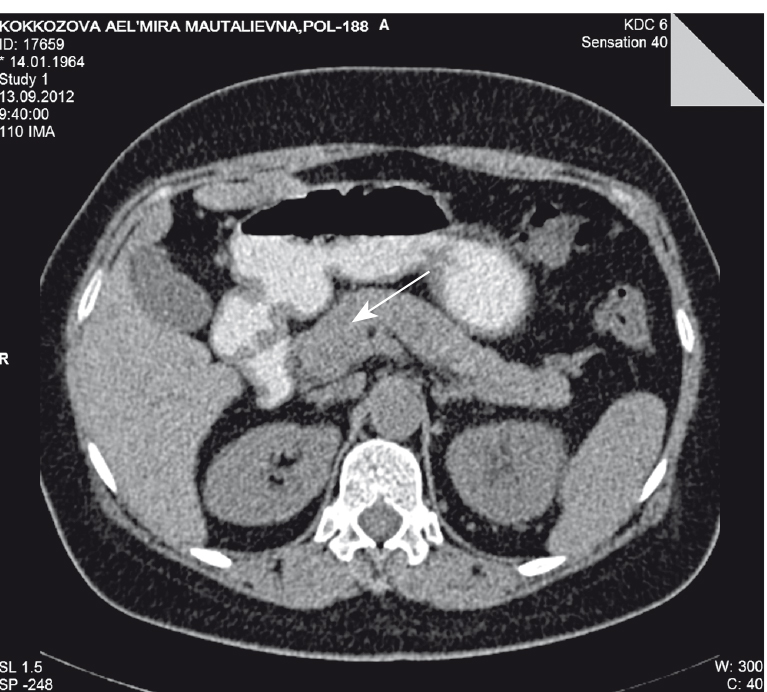
КТ выявила в проекции головки ПЖ объемное гиподенсное образование размерами 29 × 38 × 30 мм, прилежавшее к двенадцатиперстной кишке. Контрастный препарат не накапливает. Заключение: объемное образование головки поджелудочной железы (рис. 1).
Рис. 1. Компьютерная томограмма органов брюшной полости. Фото авторов
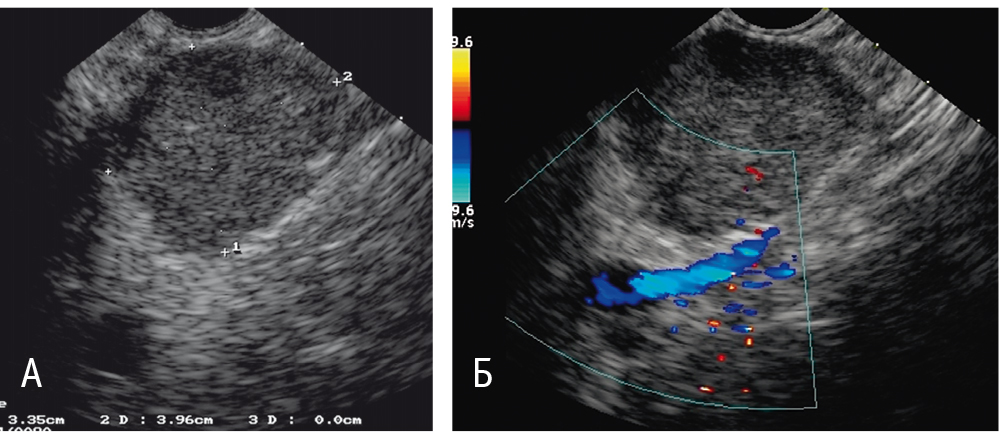
ЭУС: в проекции головки с распространением на перешеек ПЖ определялось кистозное образование овально-шаровидной формы, состоявшее из множества мелких кист 1–3 мм. Общий размер образования 34 × 40 мм. Контуры неровные, нечеткие. Главный панкреатический проток не расширен, составлял 2 мм в диаметре. Образование не связано с сосудами (рис. 2).
Рис. 2 (А, Б). Эндоскопическая ультрасонограмма. Фото авторов
Учитывая неоднозначные данные инструментальных методов исследования, для верификации диагноза было решено провести ЭУС-ТИП с последующей цитологической оценкой. Цитологическое исследование материала позволило диагностировать солидную псевдопапиллярную неоплазию (рис. 3).
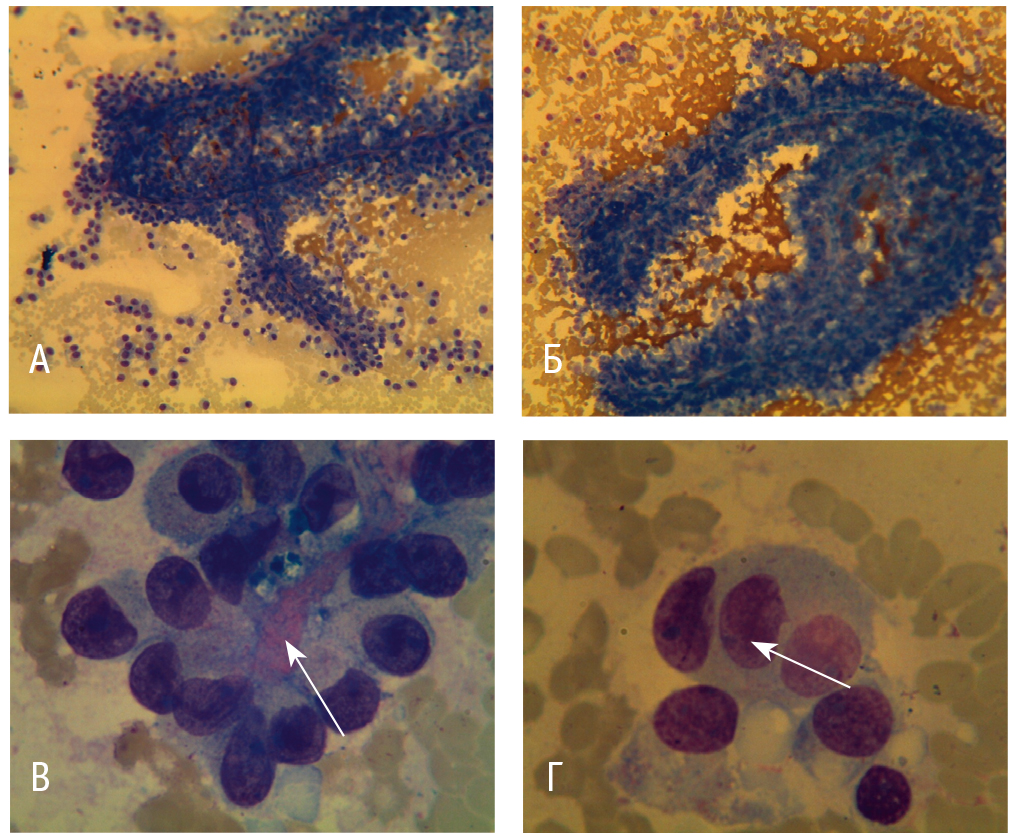
Рис. 3. Цитологическая картина. Фото авторов.
Примечание. А, Б — ветвящиеся псевдопапиллярные структуры (листовидные) с фиброваскулярными стержнями, выстланные несколькими слоями однотипных эпителиальных клеток с ядрами, ориентированными от стержня; В — клетки с ядрами округлой и слегка вытянутой формы с равномерной зернистой структурой хроматина, расположенные вокруг тонкого оксифильного стержня; Г — характерные борозды в ядрах по типу «кофейных зерен»
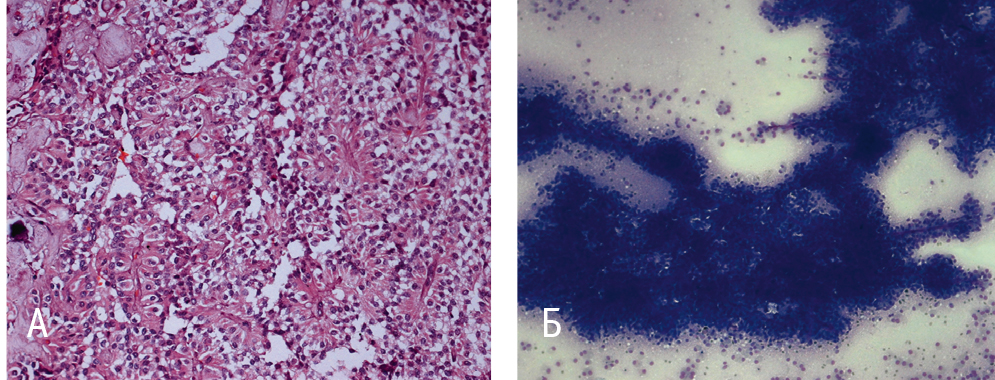
Учитывая характер и локализацию образования, больной провели панкреатодуоденальную резекцию (рис. 4). При гистологическом исследовании удаленной опухоли обнаружено, что она состояла из мелких мономорфных клеток, образовывавших солидные и папиллярные (сосочковые) структуры (рис. 5).
Рис. 4. Макропрепарат. Фото авторов
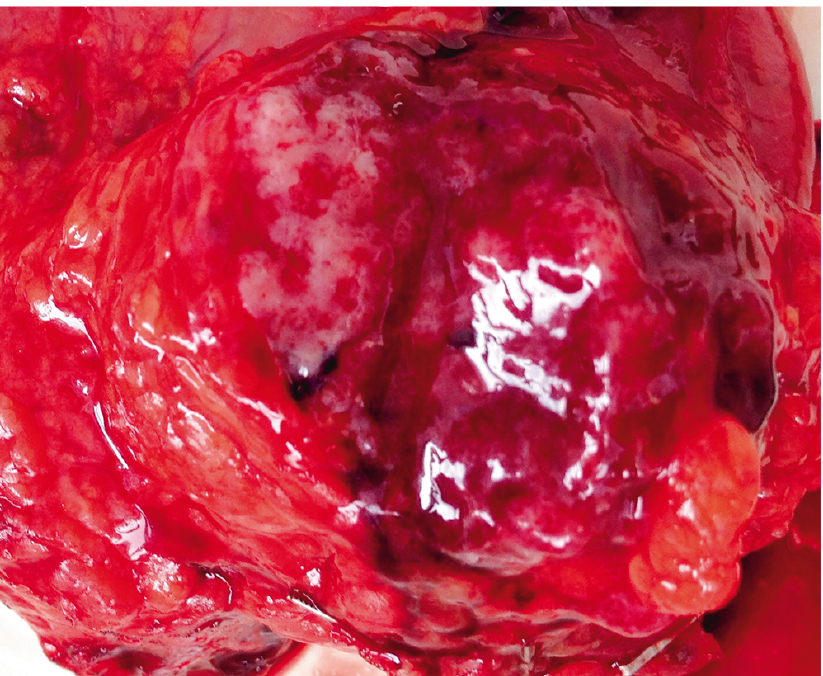
Рис. 5 (А, Б). Морфологическая картина (увеличение × 200, окраска гематоксилином и эозином). Фото авторов.
Примечание. Участок солидного строения
В течение 12 месяцев после оперативного вмешательства состояние больной удовлетворительное, при повторной КТ органов брюшной полости признаков рецидива и метастазирования не выявлено.
ЗАКЛЮЧЕНИЕ
Солидная псевдопапиллярная неоплазия является редким и загадочным заболеванием, диагностика которого крайне затруднительна даже при сопоставлении данных таких высокоинформативных методов, как КТ, МРТ и УЗИ.
Собственный клинический опыт позволяет продемонстрировать возможности применения тонкоигольной пункции под контролем эндоскопической ультрасонографии в дифференциальной диагностике объемных образований поджелудочной железы.








