Комплексная интенсивная терапия острого панкреатита остается одной из сложнейших задач современной медицины из-за высоких показателей летальности[1, 3]. Основные принципы интенсивной терапии включают подавление секреторной активности поджелудочной железы, антибактериальную терапию, нутриционную поддержку, адекватное хирургическое лечение с целью предотвращения развития гнойных осложнений[1–5].
Цель исследования: оптимизация тактики проведения нутриционной поддержки в комплексной терапии острого панкреатита.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включили 67 пациентов с диагнозом «острый панкреатит», поступивших в хирургическое отделение клинической больницы НУЗ «Медико-санитарная часть» (г. Астрахань) в 2014–2015 гг. У всех больных имелись строгие показания к хирургическому лечению: неэффективность консервативной терапии, ферментативный перитонит, выявленный при проведении УЗИ и КТ брюшной полости, нарастание симптомов системного воспалительного ответа. Возраст пациентов составил от 48 до 72 лет (в среднем 59,3 ± 2,9 года). В экстренном порядке им выполняли лапароскопическую санацию и дренирование сальниковой сумки, холецистостомию.
В зависимости от варианта лечебной тактики больные были рандомизированы на две группы: I группа — 33 пациентa, которые получали патогенетическое лечение с включением нутриционной поддержки в послеоперационном периоде, через 2 суток (48 часов) после оперативного вмешательства; II группа — 34 пациентa, которым на фоне основной патогенетической и симптоматической терапии проводилось раннее (интраоперационное) введение нутрицевтиков. На этапе дренирования сальниковой сумки и перед выполнением холецистостомии для энтерального питания в желудок пациента под контролем ФГДС интраназально вводили тонкий зонд. Интраоперационное питание осуществляли введением жидкого стерильного клинического питания «Нутризон Эдванст Диазон» по следующей схеме:
- в 1-е и 2-е сутки послеоперационного периода со скоростью 30 мл/ч в количестве 450–500 мл/сут;
- на 3-и сутки — 45–60 мл/ч в количестве 700–750 мл;
- на 4-е и 5-е сутки — 80–90 мл/ч в количестве 950–1000 мл/сут;
- на 6–9-е сутки — 125–150 мл/ч в количестве 1500–2000 мл/сут.
На 10-й день после операции удаляли зонд энтерального питания и переходили на сипинговый тип питания, в процессе которого пациенты принимали «Суппортан напиток» либо «Нутридринк» по 200 мл 3–4 раза в сутки до полного восстановления трофологического статуса. Соматометрические показатели и результаты лабораторных исследований (основные показатели клинического, биохимического и электролитного состава сыворотки крови) изучали при поступлении, на 5-е и 9-е сутки после оперативного вмешательства.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
У пациентов I группы на фоне острого панкреатита постепенно развивались трофологические нарушения с изменением соматометрических показателей и результатов лабораторного анализа. Cоматометрические нарушения заключались в уменьшении окружности мышц плеча и толщины кожно-жировой складки над трицепсом и были более выраженными у пациентов I группы (табл. 1).
Таблица 1
Динамика нутритивной недостаточности по основным соматометрическим показателям
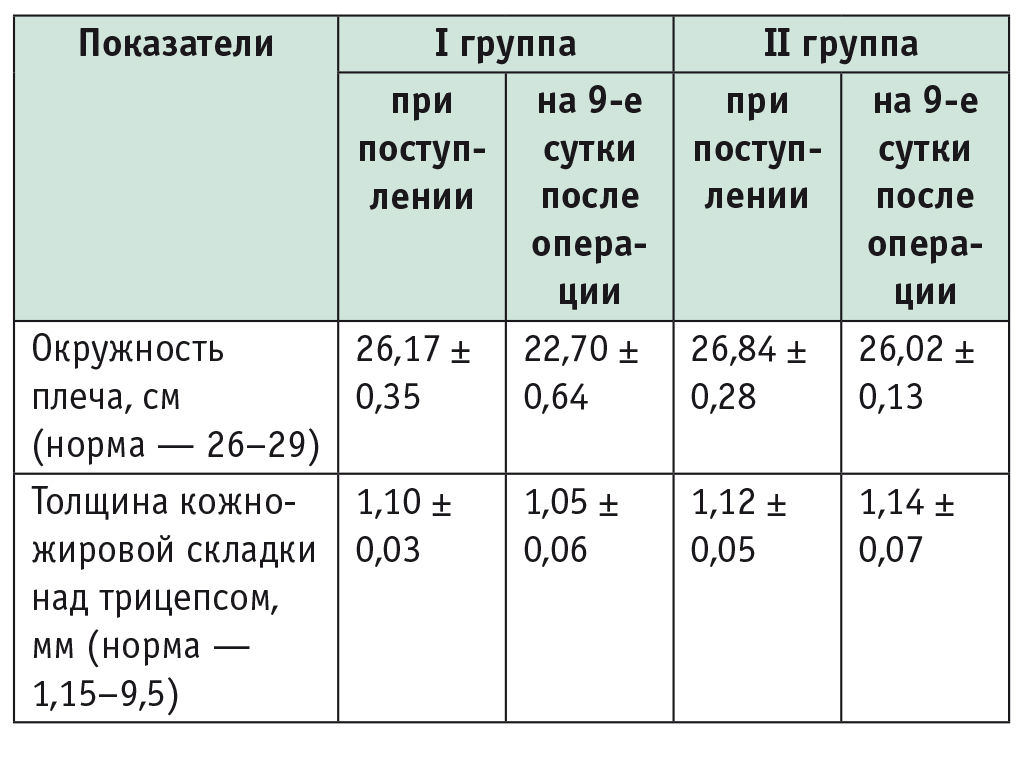
На 9-е сутки послеоперационного периода у всех пациентов определяли процент потери массы тела. Этот показатель у пациентов I и II групп существенно различался: потеря массы тела в диапазоне 5–10% в I группе отмечена у 25 (75,8%) человек, а в II-й группе — у 16 (47%).
Динамика лабораторных показателей. На 9-е сутки после операции у пациентов I группы наблюдалась отрицательная динамика гематологических показателей: количество эритроцитов уменьшилось на 7,04%, уровень гемоглобина — на 17,9%, показатель гематокрита снизился на 19,1% (p < 0,05 во всех случаях). Во II группе на 9-е сутки имело место увеличение количества эритроцитов на 4,7%, содержания гемоглобина на 6,2%, показатель гематокрита снизился на 10,5% (p < 0,05 во всех случаях) (табл. 2).
Таблица 2
Динамика гематологических, биохимических и электролитных показателей сыворотки крови у обследованных больных
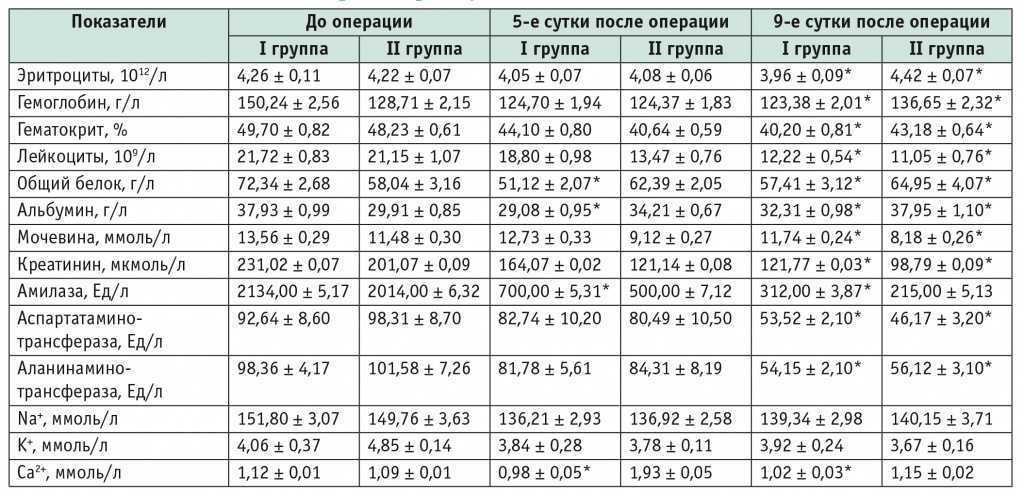
* Отличие от исходного показателя статистически значимо (p < 0,05).
Количество лейкоцитов крови в исследуемых группах статистически значимо снизилось на 9-е сутки после операции: у пациентов II группы на 47,8%, а в I группе — на 43,7% (p < 0,05 для обеих групп).
В I группе на 5-е сутки уровень общего белка снизился на 29,3% (p < 0,05), на 9-е сутки он был на 20,6% меньше исходного показателя (р < 0,05), но увеличился на 12,3% по сравнению со таковым на 5-е сутки. Количество общего белка плазмы крови у пациентов II группы на 5-е сутки увеличилось на 7,5% (p > 0,05), к 9-м суткам — на 11,9% по сравнению с исходным уровнем (p < 0,05).
Уровень альбумина плазмы крови в I группе на 5-е сутки был на 23,3% ниже исходного значения, к 9-м суткам его снижение по сравнению с исходным значением составляло 14,8% (в обоих случаях р < 0,05). Во II группе к 5-м суткам уровень альбумина в плазме крови увеличился на 14,4% по сравнению с исходным значением (p > 0,05), к 9-м суткам— на 26,9% (p < 0,05).
Для выявления повреждающего действия эндотоксикоза у пациентов определяли активность АСТ и АЛТ. У больных II группы уровень АСТ на 5-е сутки был на 18,13% (p > 0,05), а к 9-м суткам на 53,03% ниже исходного (p < 0,05). У пациентов I группы к 5-м суткам происходило статистически незначимое снижение показателя на 10,7%, к 9-м суткам он снизился уже на 42,2% по сравнению с исходным (p < 0,05), но не достиг пределов физиологической нормы.
Аналогичные результаты были получены при исследовании АЛТ: во II группе к 5-м суткам показатель снизился на 17,0% (p > 0,05), к 9-м суткам — на 44,7% (p < 0,05). У пациентов I группы к 5-м суткам показатель АЛТ уменьшился на 16,9% (p > 0,05), к 9-м суткам — на 44,9% (p < 0,05) (см. табл. 2).
Снижение уровня калия сыворотки крови было более выражено при паралитическом парезе кишечника. У пациентов I группы содержание К+ на 5-е сутки снизилось на 5,4%, на 9-е отмечен его прирост на 2,1% (p > 0,05). У 9% пациентов I группы изменения концентрации калия сыворотки крови приводили к нарушениям сердечной деятельности, часто проявлявшимся на ЭКГ снижением сегмента SТ и зубца Т. На фоне коррекции гипокалиемии у больных отмечена положительная клиническая динамика.
Таким образом, выявлена закономерная динамика соматометрических, гематологических, биохимических показателей, а также электролитного баланса сыворотки крови, убедительно свидетельствующая об эффективности интраоперационной нутриционной поддержки больных острым панкреатитом.
ЗАКЛЮЧЕНИЕ
Осуществление интраоперационной энтеральной нутриционной поддержки в комплексе лечения позволяет значительно быстрее нормализовать основные соматометрические, гематологические, биохимические и электролитные показатели у пациентов с острым панкреатитом.








