ВВЕДЕНИЕ
За последние 40 лет неалкогольная жировая болезнь печени (НАЖБП) прошла путь от одного из неясных гепатологических заболеваний, гистологически сходного с алкогольной болезнью печени (АБП), до одной из наиболее признанных причин патологии печени в мире [1, 2]. После первого описания высказывался определенный скептицизм по поводу того, что НАЖБП представляет собой реальное заболевание, но в 1990-е гг. было показано, что неалкогольный стеатогепатит (НАСГ) — часть спектра НАЖБП — обладает потенциалом для прогрессирования [3]. В последние 10 лет стало очевидно, что НАЖБП является печеночной манифестацией метаболического синдрома и превалирует у пациентов с ожирением и больных диабетом [4]. Признано, что НАСГ принадлежит к наиболее значимым причинам гепатоцеллюлярной карциномы и трансплантации печени [5]. По прогнозам, в ближайшие 20–30 лет НАЖБП займет лидирующие позиции в мире среди причин цирроза печени [6]. Социальная значимость НАЖБП не вызывает сомнений, но до настоящего времени, несмотря на ряд крупных международных консенсусов [4, 7, 8], не существует рекомендаций по терапии НАСГ, официально одобренных Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (англ. Food and Drug Administration) или Европейским агентством лекарственных средств (англ. European Medicines Agency) [9]. Все это обусловливает огромное внимание к проблеме НАЖБП.
Целью обзора явился анализ современных данных, посвященных различным аспектам НАЖБП.
ОПРЕДЕЛЕНИЕ ПАТОЛОГИИ
В 2020 г. в Journal of Hepatology, являющемся официальным органом Европейской ассоциации по изучению болезней печени (англ. European Association for the Study of the Liver), была опубликована статья международных экспертов из 22 стран, которые проанализировали перспективы изучения НАЖБП [10]. Международные эксперты пришли к заключению, что термин «метаболически ассоциированная жировая болезнь печени» (МАЖБП) более адекватно отражает сущность заболевания, чем НАЖБП. Предложение изменить название болезни связано с тем, что она сопровождается мультисистемными расстройствами и является гетерогенной патологией с различными причинами, проявлениями и течением [11]. Эксперты отметили, что в перспективе надо стремиться к выработке позитивных критериев диагностики МАЖБП, а не критериев исключения. Это, в свою очередь, сделает вероятным сочетание МАЖБП с другой патологией печени.
Предыдущее определение НАЖБП базировалось на выводах ведущих международных консенсусов и предусматривало наличие стеатоза более чем в 5% гепатоцитов при отсутствии злоупотребления алкоголем и других известных причин патологии печени [4, 7, 12, 13]. Новые критерии, предлагаемые для диагностики МАЖБП, включают в себя аккумуляцию жира в печени, подтвержденную данными гистологического исследования, лучевой диагностики или биомаркерами крови и дополненную одним из трех признаков: избыточной массой тела / ожирением, сахарным диабетом 2 типа или верифицированной метаболической дисрегуляцией (рис. 1) [10]. Следует обратить внимание, что диагноз МАЖБП может устанавливаться и у пациентов с нормальной массой тела при наличии двух нарушений метаболизма, приведенных на рисунке 1. Этот подход верифицирован в клинических исследованиях [14].
Рис. 1. Критерии диагностики метаболически ассоциированной жировой болезни печени [10]
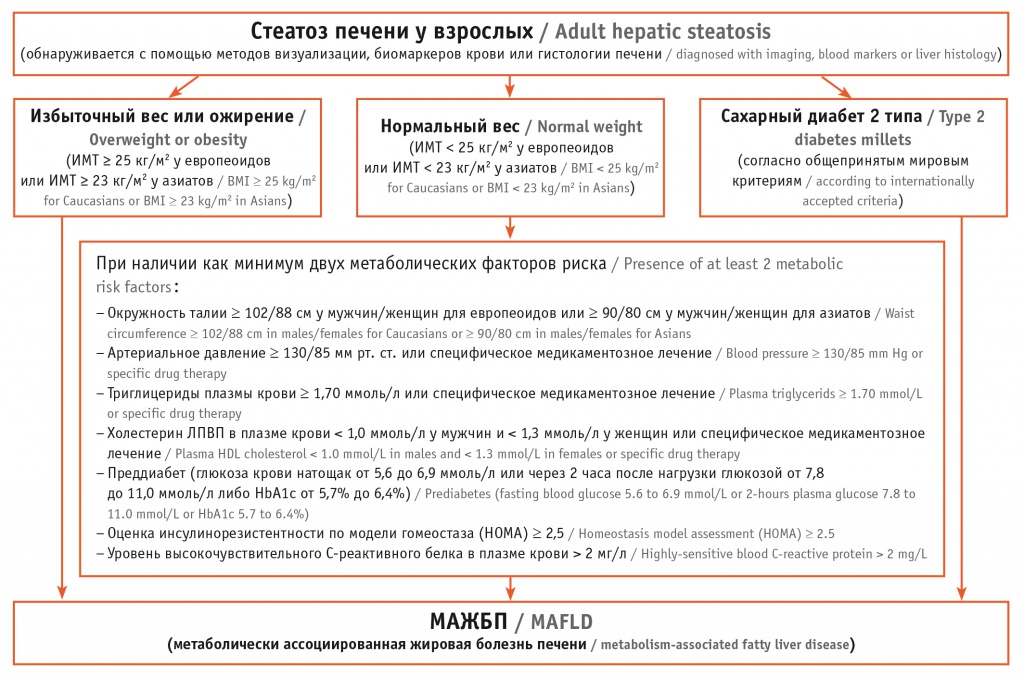
Для выявления стеатоза печени в рутинной практике широко используется УЗИ, но эта процедура имеет ограниченную чувствительность. Транзиентная эластография с определением управляемого параметра затухания (англ. controlled attenuation parameter, CAP) обладает более высокой точностью [15]. КТ и магнитно-резонансное исследование дают хорошие результаты при диагностике среднего или выраженного стеатоза. Магнитно-резонансная спектроскопия позволяет определить количество жира в печени, но является дорогим исследованием, что ограничивает ее практическое применение [16].
По экспертному мнению, при формировании диагноза термин МАЖБП должен быть единым всеобъемлющим термином, описывающим заболевание. Выраженность клинических проявлений должна характеризоваться степенью активности и стадией фиброза [17]. Эксперты полагают, что применение единого термина МАЖБП с указанием активности и стадии фиброза позволяет более эффективно и точно определить характер патологии, чем использование дихотомии на стеатогепатит и стеатоз [10].
Экспертами подчеркнуто, что у пациентов с циррозом печени и низким уровнем стеатоза печени, имеющих два метаболических расстройства и более (см. рис. 1), должен диагностироваться МАЖБП-ассоциированный цирроз. Термина «криптогенный цирроз» у этой группы больных необходимо избегать [10].
Поистине революционной является точка зрения экспертов, согласно которой возможно определение двойной этиологии заболевания печени. Эксперты отмечают, что у одного пациента может быть сочетание диагнозов МАЖБП и АБП или МАЖБП и гепатита другой этиологии. Согласно новым рекомендациям, МАЖБП не является диагнозом исключения. Обосновывая свое мнение, эксперты ссылаются на частое сочетание МАЖБП с указанными болезнями. У пациентов с сочетанием нескольких этиологических факторов заболевания печени и лиц с одним этиологическим фактором естественный анамнез и реакция на терапию различаются [18].
Эксперты указывают, что в ближайшем будущем возможна субклассификация МАЖБП с выделением доминирующих патофизиологических путей и определением преобладающего фенотипа. Это связано с выраженной гетерогенностью заболевания [19].
Необходимо заметить, что в майском номере за 2020 г. журнала Gastroenterology, являющегося официальным органом Американской гастроэнтерологической ассоциации (англ. American Gastroenterological Association), опубликована статья аналогичной тематики. В сравнении с работой в Journal of Hepatology, авторский состав этой публикации дополнен известными учеными из США. В статье высказывается однозначная позиция о целесообразности использования термина МАЖБП при дальнейшем изучении жировой болезни печени [20]. С учетом этого переименование НАЖБП в МАЖБП можно считать свершившимся фактом.
РАСПРОСТРАНЕННОСТЬ И ФАКТОРЫ РИСКА ЗАБОЛЕВАНИЯ
По различным оценкам, в США от 75 до 100 млн человек страдают НАЖБП, ежегодные затраты на лечение этой патологии составляют 103 млрд долларов [21]. В четырех европейских странах (Франция, Германия, Италия, Великобритания) НАЖБП больны 35 млн человек, ежегодные затраты на лечение равны 35 млрд евро [22].
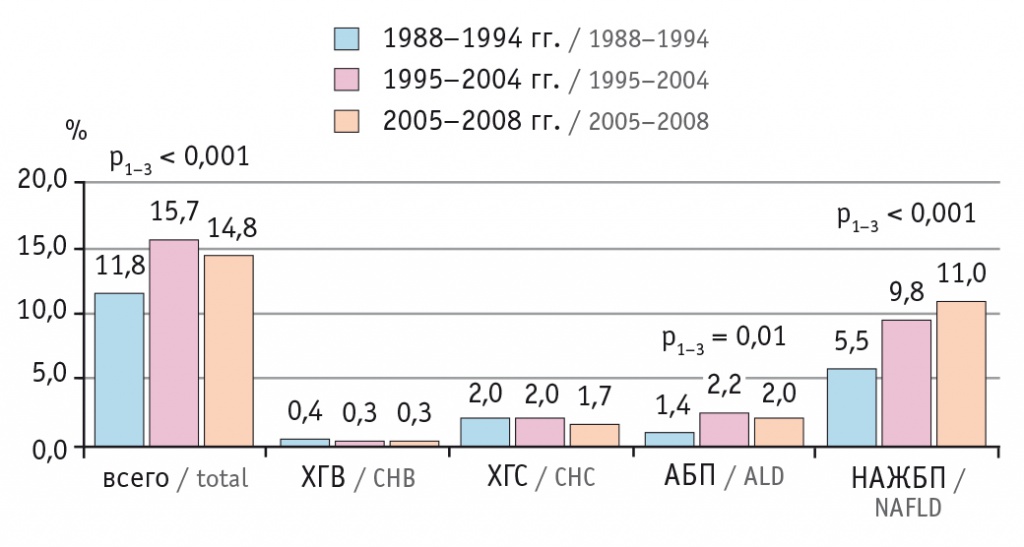
Распространенность НАЖБП в популяции Северной Америки составляет около 24% [23]. В одном из американских исследований проанализирована информация о 39 500 пациентах в период с 1988 по 2008 г. Авторы показали, что распространенность НАЖБП за это время выросла в 2 раза и болезнь заняла ведущие позиции в структуре заболеваний печени в США (рис. 2). При этом частота факторов риска НАЖБП — ожирения, сахарного диабета 2 типа и компонентов метаболического синдрома — за указанный период возросла в 1,5 раза [24].
Рис. 2. Динамика распространенности заболеваний печени в США [24].
Примечание: АБП — алкогольная болезнь печени; НАЖБП — неалкогольная жировая болезнь печени; ХГВ — хронический гепатит В; ХГС — хронический гепатит С
В Европе распространенность НАЖБП колеблется от 20% до 30% [25]. В Азии этот показатель возрос в последние годы и соответствует уровню Северной Америки и Европы [26]. Современные исследования показывают, что в связи со снижением значимости вирусных гепатитов в ближайшие годы на первое место среди причин цирроза печени выйдет НАЖБП [6].
В нашей стране в 2007–2008 гг. под руководством академика РАН В.Т. Ивашкина проводилось мультицентровое исследование НАЖБП в 16 городах, получившее наименование по протоколу DIREG_L_01903. Было обследовано 30 417 человек (17 208 женщин и 13 209 мужчин) в возрасте от 18 до 80 лет. Распространенность НАЖБП составила 27% (стеатоза — 21,7%, НАСГ — 4,5%, цирроза печени — 0,8%) и варьировалась в различных регионах: самый высокий показатель отмечен в Сибири и самый низкий — на юге европейской части России [27]. В 2015 г. было осуществлено исследование DIREG 2, включавшее 50 145 пациентов в 16 городах Российской Федерации. В работе применялась методика изучения частоты патологии по обращаемости. Распространенность НАЖБП составила 37,3%, ведущими факторами риска патологии были метаболический синдром, ожирение и сахарный диабет 2 типа [28].
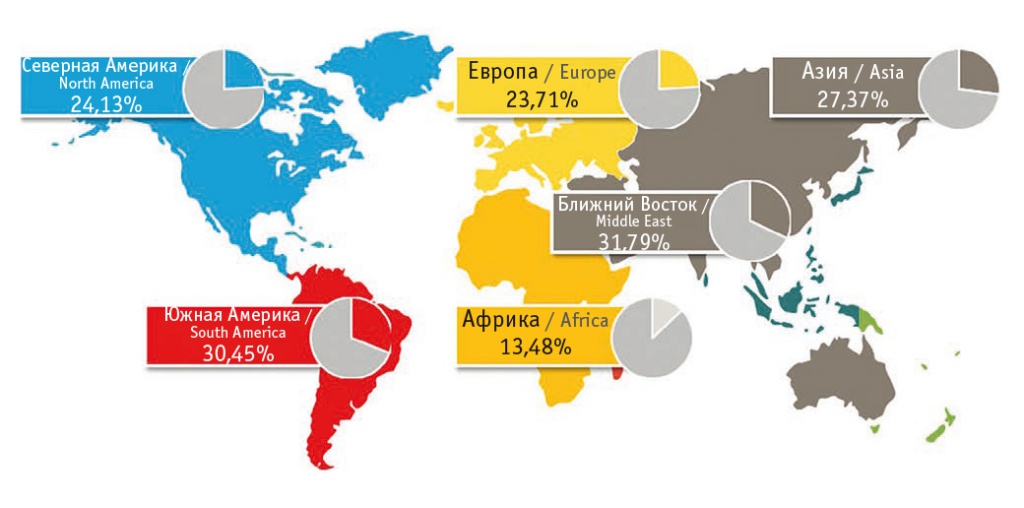
В целом в настоящее время общепризнано, что распространенность НАЖБП в различных регионах мира составляет около 25% (рис. 3). При этом распространенность НАСГ изменяется в диапазоне 3–5%, цирроза печени — 0,3–0,5%, стеатоза печени — 20–21%. Ведущие факторы риска НАЖБП не имеют этнических и географических различий — это метаболический синдром, ожирение и сахарный диабет 2 типа [29].
Рис. 3. Глобальная распространенность неалкогольной жировой болезни печени [29]
ДИАГНОСТИКА
И в прежних, и в новых представлениях о НАЖБП большое значение имеет признание отсутствия «золотого стандарта» диагностики этой патологии [29]. Согласно консенсусу Американской ассоциации по изучению заболеваний печени (англ. American Association for the Study of Liver Diseases), опубликованному в 2018 г., диагноз НАЖБП базируется на доказательстве наличия стеатоза печени при помощи лучевых методов диагностики или гистологического исследования и отсутствии других этиологических факторов накопления жира в печени (злоупотребление алкоголем, длительное применение стеатогенных препаратов, вирусный гепатит С, выраженная мальнутриция, болезнь Вильсона — Коновалова, аутоиммунный гепатит) [4]. Но в соответствии с новыми критериями (см. раздел «Определение патологии») МАЖБП будет диагностироваться на основании доказательства стеатоза печени и наличия одного из трех критериев: избыточной массы тела / ожирения, сахарного диабета 2 типа или верифицированной метаболической дисрегуляции. Новыми критериями предусматривается отсутствие необходимости исключать другие этиологические факторы, то есть у одного больного можно будет диагностировать одновременно МАЖБП и АБП или МАЖБП и хронический вирусный гепатит С [10, 20].
Известно, что наличие НАСГ и выраженного фиброза печени (≥ F2 по METAVIR) значительно повышает риск печеночных событий: цирроза печени; гепатоцеллюлярной карциномы; смерти, ассоциированной с заболеванием печени [30]. Аналогичным неблагоприятным действием на течение НАЖБП характеризуются метаболический синдром и сахарный диабет 2 типа [31].
Для диагностики фиброза печени в настоящее время разрешено применять серологические тесты NAFLD Fibrosis Score (NFS, шкала оценки стадии фиброза при НАЖБП) и Fibrosis-4 (FIB-4) [32].
Тест FIB-4 предназначен для определения фиброза печени у пациентов, инфицированных ВИЧ или ВГC, и учитывает возраст пациента и результаты анализов крови (тромбоциты, АсАТ, АлАТ). Формула расчета:
FIB-4 = возраст (лет) × АсАТ / (тромбоциты (109/л) × √АлАТ).
В интернете можно найти автоматический калькулятор теста FIB-4. Интерпретация результатов: если FIB-4 меньше 1,45, то с достоверностью около 90% может быть констатировано отсутствие значимого фиброза печени; если FIB-4 больше 3,25, то высока вероятность наличия выраженного фиброза печени [33].
Наиболее точными неинвазивными методами определения фиброза печени являются транзиентная эластометрия и магнитно-резонансная эластография. Интерпретируя результаты исследований, необходимо учитывать, что на них влияют избыточная масса тела пациента и наличие воспаления в печени [33, 34]. Подробное изложение большинства описанных диагностических подходов содержится в Клинических рекомендациях по диагностике и лечению неалкогольной жировой болезни печени Российского общества по изучению печени (РОПИП) и Российской гастроэнтерологической ассоциации (РГА) [35].
ЛЕЧЕНИЕ
Современные европейские [7], американские [4], азиатские [8] и российские [35] гайдлайны содержат рекомендации по модификации образа жизни, повышению физической активности и снижению веса в качестве терапии первой линии у пациентов с НАЖБП. Рекомендации включают сокращение калорийности диеты (снижение на 500–1000 ккал/день в сравнении с привычным режимом), увеличение в пище доли продуктов, содержащих ω3-полиненасыщенные жирные кислоты (морепродукты), уменьшение доли рафинированных углеводов, систематическое применение физических упражнений средней интенсивности и общее повышение физической активности, снижение веса, в случае его избыточности, на 7–10% от начальных величин [36].
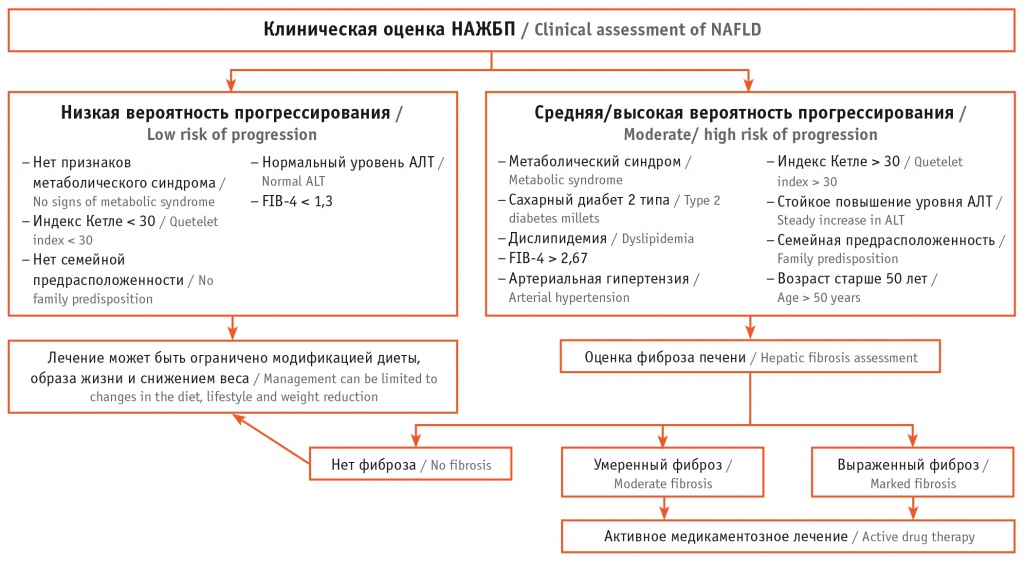
К показаниям для медикаментозного лечения НАЖБП в настоящее время принято относить НАСГ, сочетание с фиброзом печени и/или наличием нескольких компонентов метаболического синдрома [37, 38]. Алгоритм ведения пациентов в зависимости от стадии фиброза и других факторов приведен на рисунке 4 [34].
Рис. 4. Алгоритм ведения пациентов с неалкогольной жировой болезнью печени [34]
В международных рекомендациях для лечения НАЖБП одобрены витамин Е, инсулиновые сенситайзеры, статины (при наличии гиперлипидемии) [4, 7, 8, 38]. В рекомендациях РОПИП и РГА для лечения НАЖБП из препаратов с цитопротективной активностью допускается использовать урсодезоксихолевую кислоту, адеметионин, глицирризиновую кислоту, препараты, содержащие силибинин и эссенциальные фосфолипиды [35].
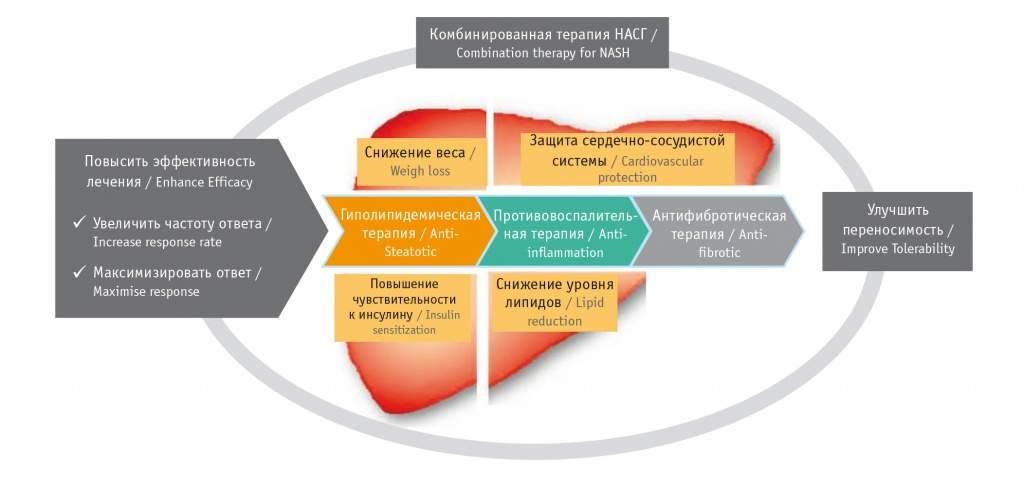
В последнее время активно обсуждается выраженная ассоциация НАЖБП с сердечно-сосудистыми заболеваниями. Наиболее частой причиной смерти пациентов с НАЖБП являются кардиоваскулярные события [39]. В этой связи предложено активно использовать комбинированную терапию НАСГ, которая должна включать защиту сердечно-сосудистой системы и, при необходимости, гиполипидемические средства (рис. 5) [9]. Этот подход поддерживают ведущие российские гепатологи — академик РАН В.Т. Ивашкин, М.В. Маевская и соавт. [40].
Рис. 5. Комбинированная терапия неалкогольного стеатогепатита [9]
Большое внимание сейчас уделяется новым методам лечения НАЖБП [41]. Агонист фарнезоидных рецепторов обетихолевая кислота (ОХК) регулирует обмен желчных кислот и липидный метаболизм. В плацебо-контролируемом трайле FLINT 283 пациента с морфологически подтвержденным диагнозом НАСГ без цирроза печени были рандомизированы на две группы: одна из них в течение 72 недель получала ОХК в дозе 25 мг/день, другая — плацебо. В конце исследования положительная морфологическая динамика была достигнута у 45% лиц, получавших ОХК, и только у 21% пациентов группы плацебо (р = 0,0002). У 23% пациентов, принимавших ОХК, регистрировались зуд и неблагоприятные изменения липидного профиля крови [42].
В другом плацебо-контролируемом исследовании с участием 931 пациента с НАСГ и фиброзом печени (F2–F3 по METAVIR) больных рандомизировали на три группы, которые в течение 18 месяцев получали плацебо, ОХК в дозе 10 мг/сут и ОХК в дозе 25 мг/сут. Выраженность фиброза печени снизилась у 12% лиц группы плацебо и у 23% пациентов, принимавших 25 мг ОХК в сутки (p < 0,001). Зуд регистрировался у 51% больных, получавших ОХК в дозе 25 мг/сут. Было сделано заключение о статистически значимом снижении выраженности фиброза печени и ключевых компонентов воспалительной активности НАСГ при применении 25 мг ОХК в сутки [43].
Элафибранор (elafibranor) является агонистом PPAR-α/δ-рецепторов и оказывает регулирующее действие на метаболический гомеостаз, воспаление и β-оксидацию жирных кислот. В плацебо-контролируемом исследовании 276 пациентов с морфологически подтвержденным НАСГ и без цирроза печени были рандомизированы на три группы: в течение 52 недель в одной группе применяли 80 мг элафибранора в сутки (группа 1), в другой — 120 мг препарата в сутки (группа 2), в третьей группе — плацебо (группа 3). После введения строгих дефиниций конечная точка морфологического ответа была достигнута у 13% лиц первой группы, 19% пациентов второй группы и 12% больных, получавших плацебо (р2–3 = 0,045) [44].
Вместе с тем новые препараты не всегда показывают необходимую эффективность. В плацебо-контролируемых исследованиях ингибиторов апоптоза селонсертиба (selonsertib) и эмрикасана (emricasan) существенного ответа у пациентов с НАСГ и выраженным фиброзом печени получить не удалось [45, 46].
ЗАКЛЮЧЕНИЕ
Следует ожидать, что предложение международных экспертов переименовать неалкогольную жировую болезнь печени в метаболически ассоциированную жировую болезнь печени (МАЖБП) будет официально одобрено в ближайшее время.
Точка зрения, согласно которой возможно сочетание МАЖБП с гепатитами, вызванными другими этиологическими факторами, является по-настоящему революционной. Несомненно, такой подход позволит получить новую информацию, но, по всей видимости, только время позволит оценить все его плюсы и минусы.
Проводится огромная работа по развитию методов диагностики и лечения жировой болезни печени, и это позволяет надеяться на их оптимизацию в ближайшее время.
Поступила: 13.01.2021
Принята к публикации: 31.01.2021








