Функциональная диспепсия (ФД) — одно из наиболее часто встречающихся функциональных нарушений органов пищеварения в большинстве стран мира[4, 14]. В общей популяции распространенность симптомов ФД колеблется от 11% до 29%[11]. Данные эпидемиологических исследований свидетельствуют о неуклонной тенденции к росту частоты встречаемости ее проявлений среди населения[11]. У большинства пациентов заболевание протекает длительно, с чередованием периодов обострения и ремиссии. Симптомы заболевания оказывают существенное влияние на качество жизни больных, что сопряжено с экономическими потерями в результате утраты трудоспособности, затратами на диагностику и лечение. Среди больных ФД 25% обращаются к врачу более 4 раз в год[10], суммарная временная нетрудоспособность этой группы пациентов на 3–4 недели больше средней длительности нетрудоспособности населения[13]. Особую трудность представляет оптимизация лечения болевого синдрома при ФД. В базовую терапию ФД входят ИПП и прокинетики. В последнее время апробируются и другие методы лечения: агонисты рецепторов мотилина и мускариновых М1- и M2-рецепторов, — однако потребность в безопасных и эффективных методах лечения остается в значительной степени неудовлетворенной[17].
В соответствии с рекомендациями согласительного совещания Международной рабочей группы по совершенствованию диагностических критериев функциональных заболеваний ЖКТ (Римские критерии III, 2006), термин «функциональная диспепсия» характеризуются четырьмя основными признаками (табл. 1).
Таблица 1
Характеристика симптомов функциональной диспепсии (Римские критерии Ш, 2006)

Для постановки диагноза ФД необходимо, чтобы указанные симптомы наблюдались у больного последние 3 месяца и рецидивировали по крайней мере несколько раз в неделю, а первые признаки заболевания появились как минимум за 6 месяцев до постановки диагноза и чтобы при этом не было обнаружено никакой органической причины диспепсии.
Диагноз ФД устанавливается на основании анализа клинических симптомов, анамнеза заболевания, результатов физикального осмотра больных, а также данных лабораторно-инструментального обследования с обязательным эндоскопическим исследованием верхних отделов ЖКТ и УЗИ органов брюшной полости — по существу, посредством исключения органических заболеваний, при которых могли бы возникать подобные симптомы. Следовательно, диагноз ФД выставляется методом исключения.
Римский консенсус III предлагает выделять два основных клинических варианта ФД: эпигастральную боль и постпрандиальный дистресс-синдром, — которые, впрочем, могут существовать одновременно, а также сочетаться с функциональной тошнотой/рвотой или отрыжкой.
- Эпигастральный болевой синдром (ЭБС). О синдроме боли в эпигастрии принято говорить в тех случаях, когда у больного по меньшей мере один раз в неделю отмечаются умеренные или выраженные боли или чувство жжения в эпигастральной области. При этом боли не носят постоянного характера, связаны с приемом пищи или возникают натощак, не иррадиируют в другие отделы живота, не уменьшаются после дефекации или отхождения газов и не сопровождаются признаками дисфункции желчного пузыря или сфинктера Одди.
- Постпрандиальный дистресс-синдром (ППДС). Об этой форме ФД следует вести речь в тех ситуациях, когда у больного по меньшей мере несколько раз в неделю после приема обычного объема пищи возникает чувство переполнения в эпигастрии или раннее насыщение. ППДС может сочетаться с тошнотой и ЭБС.
Существенным отличием Римских критериев III от предыдущих редакций стало признание комитетом экспертов того факта, что у пациентов с симптомами, соответствующими диагностическим критериям ФД (ЭБС и ППДС), могут отмечаться изжога или клинические признаки синдрома раздраженного кишечника (СРК). Наличие изжоги не исключает диагноза ФД, если симптомы диспепсии персистируют несмотря на попытки проведения адекватной кислотоснижающей терапии. Установлено, что сочетание ФД с СРК не оказывает значительного влияния на патофизиологические механизмы развития ФД[6].
По данным классических исследований, патогенетические звенья ФД включают в себя нарушения секреции соляной кислоты, расстройства гастродуоденальной моторики и изменение висцеральной чувствительности[1]. Большинство исследователей связывают патогенез ФД с повышенной висцеральной чувствительностью (гиперсенситивностью) слизистой оболочки желудка и двенадцатиперстной кишки к обычным пищевым раздражителям и соляной кислоте, а также со снижением порога чувствительности к растяжению[15]. Избыточная чувствительность слизистой оболочки приводит к нарушению рефлекторной регуляции нервно-мышечного аппарата гастродуоденальной зоны на различных уровнях: местном, сегментарном, центральном, — а также вызывает сдвиги в серотонинергической сигнальной системе и гормональном профиле больных (соматостатин, мотилин и др.)[2]. По существу, развитие ФД, подобно формированию других функциональных расстройств, обусловлено дискоординацией работы регуляторных звеньев различного уровня, что приводит к дискинезии подчиненных органов[3].
Что касается собственно моторных нарушений, а именно нарушений моторики желудка и двенадцатиперстной кишки, то их роль в патогенезе ФД сводится к:
- расстройствам аккомодации желудка (40%);
- нарушениям миоэлектрической активности (ритма перистальтики) в виде тахи- и брадигастрии (33–66%);
- замедлению эвакуации из желудка (30–40%);
- ослаблению моторики антрального отдела желудка и нарушениям антродуоденальной координации.
Исследования последних лет подтвердили наличие выраженной корреляции между моторно-тонической дисфункцией желудка и развитием ППДС, тогда как у больных с ЭБС такой корреляции не прослеживается[1, 7].
Роль кислотно-пептического фактора в развитии функционального гастродуоденального расстройства определяется тем, что: 1) у части (30–40%) больных повышены уровни базальной и стимулированной секреции соляной кислоты и нарушено ощелачивание в антральном отделе желудка[8]; 2) у пациентов с ФД может иметься повышенная чувствительность слизистой оболочки желудка и двенадцатиперстной кишки к соляной кислоте, особенно при увеличении времени пребывания последней в двенадцатиперстной кишке; 3) ИПП эффективны у больных с язвенноподобным вариантом ФД; 4) у больных с синдромом эпигастральной боли снижены уровни интрагастрального и интрадуоденального рН (особенно в ночное время) и отмечаются субкомпенсированные нарушения ощелачивающей функции антрального отдела желудка; 5) гипо- и анацидный типы рН-граммы у больных с дискинетическим вариантом ФД могут быть отражением эпизодов дуоденогастрального рефлюкса.
Первичная гиперчувствительность к кислоте через нервные и гуморальные механизмы может обуславливать задержку эвакуации содержимого из желудка. В эксперименте доказано, что введение слабого раствора соляной кислоты через эндоскоп в двенадцатиперстную кишку у больных ФД чаще приводит к возникновению болей, чувства жжения в эпигастрии и тошноты, чем у здоровых людей, и сопровождается снижением двигательной функции антрального отдела желудка и повышением моторики тощей кишки[6]. Висцеральная гиперчувствительность выявляется у 34–65% пациентов с ФД, коррелирует с выраженностью признаков как ЭБС, так и ППДС и может играть главную роль в возникновении основного клинического симптома — болей в эпигастральной области.
Таким образом, у многих больных с болевым вариантом ФД основным фактором, вызывающим клинические проявления заболевания, правомерно считать гиперсекрецию соляной кислоты и/или гиперчувствительность слизистой оболочки гастродуоденальной области.
Лечение ФД представляет трудную задачу, особенно при рефрактерном и рецидивирующем характере симптомов. Оно включает в себя общие мероприятия по нормализации образа жизни и питания, исключение вредных привычек, применение антисекреторных лекарственных препаратов и прокинетиков, а в ряде случаев — и психотерапевтических методов.
Несмотря на то что значение алиментарных погрешностей и вредных привычек в развитии ФД остается недоказанным, больным (особенно с ППДС) рекомендуется частое (6 раз в сутки) питание небольшими порциями с исключением продуктов, раздражающих слизистую оболочку желудка: горячих блюд, алкоголя (особенно натощак), газированных напитков, острых, копченых, жареных блюд, свежей выпечки, блинов, крепкого кофе, редиса, острых приправ. В рацион могут входить нежирное мясо (рубленое, отварное, тушеное или жареное без панировки в муке или сухарях), различные каши, пудинги, яйца всмятку, фруктовые и ягодные протертые компоты, фруктовые и овощные пюре, кисели, желе, муссы. Больным следует включать в меню блюда, обладающие обволакивающим эффектом: молочный или молочно-овсяный кисель, жидкие каши (манную, рисовую, гречневую, овсяную) с добавлением молока или сливок, овощные супы-пюре, рубленые отварные мясные и рыбные блюда с молочным и сливочным соусами, омлет, пюре из картофеля или тыквы с добавлением сливок, яичного желтка. Если пациент любит кофе, крепкий чай, не следует категорически требовать от него отказа от любимых напитков, но больному следует рекомендовать добавлять в кофе молоко или сливки и пить чай и кофе после основных блюд. При обострении заболевания в рационе должны преобладать супы на мясном, курином и рыбном бульонах, овощных отварах с крупой, макаронными изделиями, с мелко нарубленными или протертыми овощами.
Главным направлением в медикаментозной терапии ФД с позиций доказательной медицины является использование лекарственных средств с антисекреторным эффектом и прокинетиков. Часто больные с диспепсией используют антациды, однако результаты большинства двойных слепых контролируемых исследований свидетельствуют об отсутствии их преимуществ перед плацебо.
Результаты многочисленных исследований по оценке применения антисекреторных препаратов в лечении больных ФД свидетельствуют о статистически значимо более высокой эффективности ИПП по сравнению с блокаторами H2-рецепторов. Канадское многоцентровое рандомизированное сравнительное исследование эффективности применения омепразола (20 мг/сут), ранитидина (150 мг 2 раза в сутки), цизаприда (20 мг 2 раза в сутки) и плацебо в течение четырех недель в лечении H. pylori-отрицательных больных с синдромом диспепсии (исследование CADET-HN) показало, что эффективность омепразола (51%) существенно превосходит таковую при применении ранитидина (36%), цизаприда (31%) и плацебо (23%)[16]. Метаанализ семи работ, включавших в общей сложности 3421 больного ФД, выявил существенные преимущества ИПП над плацебо, при этом стойкое купирование болевого синдрома (в частности, при назначении рабепразола) достигалось уже на первой неделе лечения[12, 16].
ИПП наиболее эффективны у пациентов с ЭБС. При доминировании признаков дискинетических расстройств (ППДС) дополнительно показан прием прокинетиков.
По данным большинства исследователей, продолжительность основного курса лечения ФД должна составлять около четырех недель. При обострении симптомов диспепсии ИПП применяют в стандартных суточных дозах (эзомепразол — 40 мг, лансопразол — 30 мг, омепразол — 20 мг, рабепразол — 20 мг, пантопразол — 40 мг). В последующем, в зависимости от самочувствия пациентов, наличия или отсутствия рецидивов симптомов диспепсии, выбирается индивидуальная схема поддерживающей терапии.
Главная цель поддерживающей терапии при ФД — сохранение клинической ремиссии и качества жизни пациентов. Для ее проведения необходимо, во-первых, выбрать базисное лекарственное средство, оказывающее стабильное антисекреторное действие и безопасное при длительном приеме, а во-вторых, определить тактику лечения — установить оптимальную дозу, режим и сроки приема препарата.
Если при анализе результатов лечения ФД большинство исследователей сходятся во мнении, что симптомы заболевания эффективно купируются ИПП[9], то в отношении поддерживающей терапии единого мнения нет, рекомендации носят общий характер и имеют низкий уровень доказательности. Предлагаются различные варианты: постоянный прием ИПП в стандартной или половинной дозе ежедневно или через день; прием ИПП в режиме «по требованию»; интермиттирующая терапия (полные курсы при рецидиве симптомов); терапия при усилении психосоциальных стрессовых факторов; поэтапно снижающаяся базисная терапия (переход от ИПП к регулярному приему блокаторов Н2-рецепторов гистамина или антацидов).
Вероятно, выбор поддерживающего лечения должен определяться такими критериями, как объем начальной терапии, необходимой для купирования симптомов (прежде всего болевого синдрома в эпигастральной области), и индивидуальные факторы — как способствующие, так и препятствующие возникновению рецидива заболевания.
Целью проведенного нами рандомизированного исследования была оценка эффективности трех режимов поддерживающей терапии препаратом Хайрабезол (рабепразол) у пациентов с ФД по достижении ими клинической ремиссии.
Задачи исследования:
- определить количество больных с рецидивами болезни в группах пациентов, получавших поддерживающую терапию Хайрабезолом, и в контрольной группе с другими методами лечения;
- изучить частоту и интенсивность симптомов диспепсии при различных схемах поддерживающей терапии;
- оценить качество жизни пациентов на фоне поддерживающей терапии;
- исследовать безопасность длительного приема Хайрабезола.
МАТЕРИАЛЫ И МЕТОДЫ
В исследовании, выполненном на базе городских поликлиник № 52 и № 195 Департамента здравоохранения города Москвы, участвовали 80 больных — 45 женщин и 35 мужчин; средний возраст — 37 ± 11,5 года. Диагноз ФД был поставлен в соответствии с Римскими критериями III, у всех пациентов на момент включения в исследование отмечалась клиническая ремиссия заболевания, а в анамнезе имелось рецидивирование симптомов диспепсии (более 3 раз за последние 6 месяцев). У 37 (46,25%) пациентов клиническая ремиссия была достигнута на фоне монотерапии Хайрабезолом в суточной дозе 20 мг, у 34 (42,50%) — на фоне применения Хайрабезола в комбинации с прокинетиками (итоприд или домперидон), и у 9 (11,25%) человек симптомы заболевания купировались в результате лечения прокинетиками (итоприд) в комбинации с антацидами по требованию.
В зависимости от метода и схемы лечения больные были разделены на четыре равные группы:
- прием Хайрабезола в дозе 10 мг/сут ежедневно (первая группа, n = 20);
- прием Хайрабезола в дозе 20 мг/сут ежедневно (вторая группа, n = 20);
- прием Хайрабезола в дозе 20 мг/сут по требованию (третья группа, n = 20);
- применение антацидов и прокинетиков по требованию (четвертая, контрольная, группа, n = 20).
Распределение по группам поддерживающей терапии было случайным. Больные каждой группы были сопоставимы по возрасту, длительности болезни и другим существенным признакам (табл. 2).
Таблица 2
Характеристика больных обследуемых групп
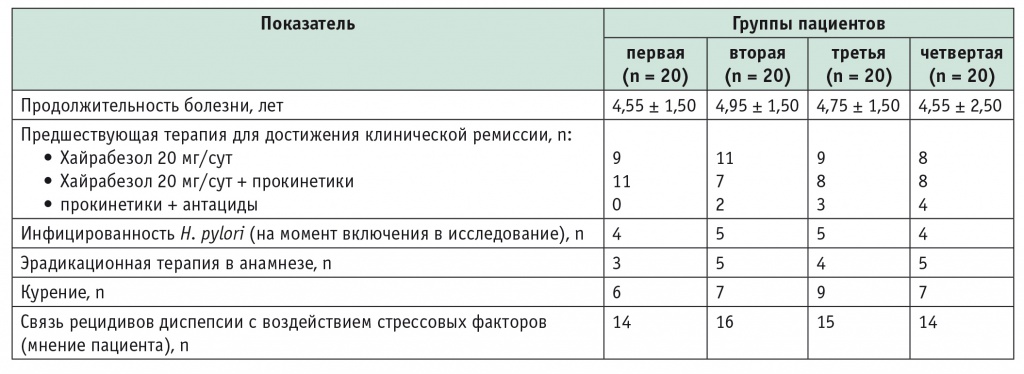
Перед включением в исследование всем пациентам назначали ЭГДC с проведением быстрого уреазного теста на H. pylori, УЗИ органов брюшной полости, клинический и биохимический анализы крови.
Пациенты вели ежедневный дневник, в котором фиксировали время возникновения рецидивов заболевания и выраженность симптомов диспепсии по шкале Лайкерта: 1 — симптомы отсутствуют; 2 — выраженность симптомов слабая (можно не замечать, если не думать); 3 — умеренная (симптомы не удается не замечать, но они не нарушают дневную активность или сон); 4 — сильная (симптомы нарушают дневную активность и сон); 5 — очень сильная (симптомы значительно нарушают дневную активность или сон, требуется отдых). При рецидиве диспепсии больным разрешалось дополнительно принимать Хайрабезол (в первой группе — 10 мг, во второй и третьей — 20 мг) или антациды и прокинетики (в контрольной группе). Сопутствующая патология в момент исследования ни в одном случае не требовала медикаментозной коррекции.
Динамику состояния больных оценивали ежемесячно на протяжении трех месяцев. Оценку переносимости терапии выполняли на основании дневниковых записей в конце каждого месяца наблюдения. Для определения качества жизни использовали визуальную аналоговую шкалу (ВАШ) в сантиметрах. По завершении наблюдения всем пациентам проводили повторную ЭГДС, общеклиническое и биохимическое исследование крови.
При обработке материала определяли средние значения, ошибку, доверительный интервал. При сравнении средних показателей различных групп использовали t-критерий Стьюдента. Полученные данные обрабатывали в программе Statistica 7.0, результаты считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
Частота рецидивов на фоне поддерживающей терапии в разных группах представлена в таблице 3. У пациентов первой и второй групп рецидивы симптомов диспепсии происходили статистически значимо реже (p < 0,05). На фоне постоянного приема Хайрабезола их отметили только 25% пациентов, при этом пациенты, ежедневно принимавшие 20 мг Хайрабезола, зафиксировали появление диспепсии только на третий месяц поддерживающей терапии. Возврат клинических симптомов выявлен у 65% больных, принимавших Хайрабезол в режиме «по требованию», и у 70% пациентов контрольной группы (с применением антацидов и прокинетиков по требованию).
Таблица 3
Количество пациентов с рецидивами диспепсии на фоне различных схем поддерживающей терапии
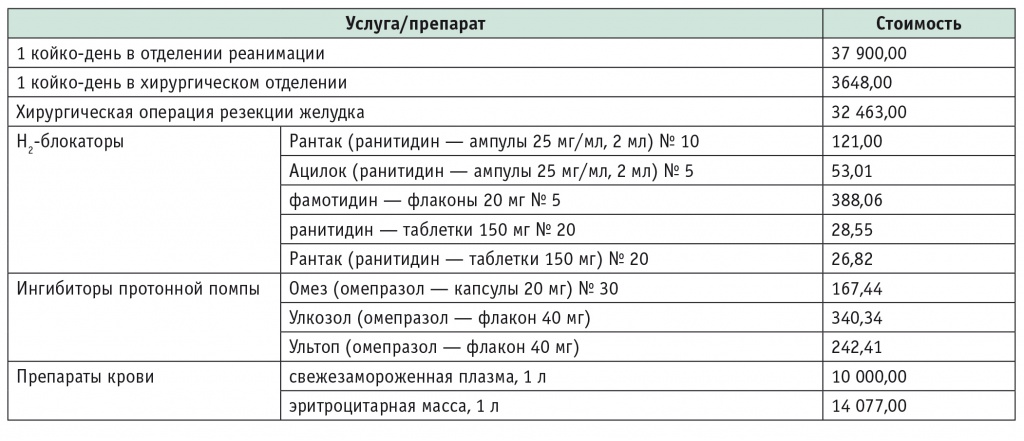
* P < 0,05 (в сравнении с третьей и четвертой группами).
При оценке выраженности рецидивирующих симптомов диспепсии все пациенты первой и второй групп определяли эпигастральную боль или сочетание боли с тяжестью в подложечной области после еды как слабые либо умеренные ощущения; большинство пациентов третьей группы — как умеренные (45%) либо сильные (10%). Сходное распределение больных отмечено и в контрольной группе: с умеренной выраженностью симптомов диспепсии — 50%, с сильной — 5% больных (табл. 4).
Таблица 4
Оценка выраженности симптомов диспепсии на фоне поддерживающей терапии, n (%)
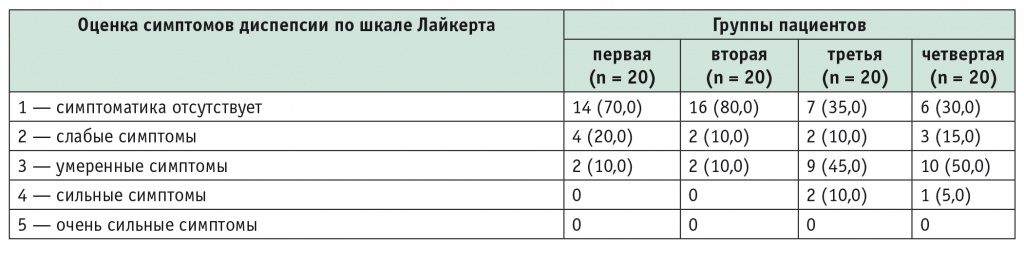
При определении количества дней с симптомами диспепсии различной степени выраженности за все время наблюдения установлено, что у большинства пациентов трех первых групп симптомы обострения заболевания продолжались не более 7 дней, а у 45% пациентов контрольной группы длительность диспепсических симптомов превышала 7 дней (табл. 5).
Таблица 5
Длительность симптомов диспепсии при различных режимах поддерживающей терапии, n (%)
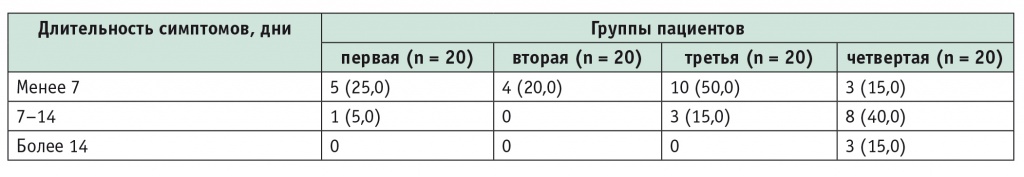
По данным ВАШ поддерживающая терапия позволяла сохранять качество жизни, достигнутое в ходе курсового лечения, при использовании всех трех режимов поддерживающей терапии рабепразолом, при этом статистически значимого различия между первой и второй группами, ежедневно применявшими Хайрабезол в суточных дозах 10 и 20 мг соответственно, не обнаружено. Прием Хайрабезола в каждом режиме позволял обеспечивать более высокий уровень качества жизни, чем у пациентов контрольной группы (табл. 6).
Таблица 6
Динамика данных визуальной аналоговой шкалы оценки качества жизниу больных разных групп, см (х ± m-х)
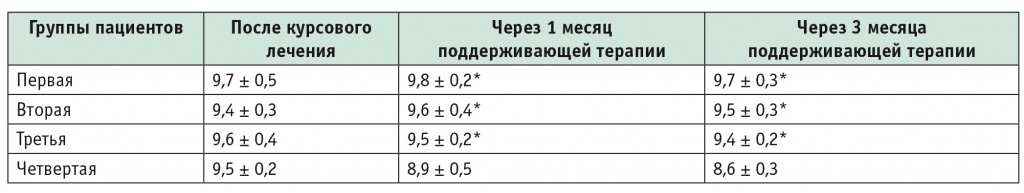
* P < 0,05 (в сравнении с четвертой группой).
В ходе анализа дневниковых записей пациентов очень хорошая переносимость лечения Хайрабезолом выявлена у 51 (85%), хорошая — у 5 (8,3%), удовлетворительная — у 4 (6,7%) больных. Нежелательное явление (легкая головная боль, не требовавшая прекращения приема препарата и терапии для купирования) отмечена у 2 (3,3%) пациентов. Остальные больные (58 человек, или 96,7%) перенесли курс поддерживающего лечения без нежелательных явлений.
ОБСУЖДЕНИЕ
У большинства больных ФД заболевание протекает длительно, с чередованием периодов обострения и ремиссии. При назначении лекарственных препаратов на основной и поддерживающий курсы лечения следует исходить из варианта ФД. При ЭБС целесообразно назначение антисекреторных препаратов, прежде всего ИПП, в стандартных дозах. Больным с ППДС показан прием прокинетиков.
Выбор препарата Хайрабезол (рабепразол) в качестве поддерживающей терапии у пациентов с ФД обоснован следующими фактами:
- доказана высокая клиническая эффективность рабепразола в лечении кислотозависимых заболеваний, подтвержденная клиническими исследованиями. Особая структура таблеток, покрытых кишечнорастворимой оболочкой, которая предотвращает разрушение активного вещества соляной кислотой и позволяет создавать его максимальную концентрацию непосредственно в слизистой оболочке желудка, обеспечивает эффективное долговременное снижение кислотности желудочного сока;
- более длительный период полувыведения рабепразола, в сравнении с другими ИПП, предопределяет продолжительность антисекреторного действия в течение 24 часов при приеме 1 раз в сутки[9]. Антисекреторный эффект после перорального приема 20 мг препарата наступает в течение 1 часа и достигает максимума через 2–4 часа; угнетение базальной и стимулированной пищей секреции кислоты через 23 часа после приема первой дозы составляет 62% и 82% соответственно;
- известно, что все ИПП подвергаются биотрансформации в печени. Этот метаболизм включает в себя окисление системой ферментов цитохрома Р450 (CYP2C19 и CYP3A4). Указанные ферменты встречаются у человека в виде различных изоформ, которые метаболизируют ИПП с различной скоростью[13]. Поэтому у разных людей, имеющих быстрый или медленный тип метаболизма, обусловленный данными ферментами, эффективность препаратов существенно различается: пациент — быстрый метаболизатор может быть нечувствительным к лекарственным средствам, и доза ИПП у него должна быть повышена. Ввиду того что в повседневной клинической практике методы определения скорости метаболизма ИПП отсутствуют, клинически выгоднее применять препараты, эффективность которых меньше зависит от цитохромов печени. Рабепразол в значительной степени подвергается неферментному превращению, его выведение в меньшей степени определяется печеночным метаболизмом, что обеспечивает предсказуемую антисекреторную эффективность у всех пациентов;
- Хайрабезол безопасен при длительном использовании и может применяться совместно с другими лекарственными средствами, в том числе с антацидами;
- Хайрабезол имеет разные дозировки в таблетированной форме выпуска (10, 20 мг) и отличается от аналогичных средств более низкой стоимостью;
- Хайрабезол разрешен к применению у детей с 12 лет.
Результаты исследования показали значительное снижение частоты рецидивирования и выраженности симптомов диспепсии (как ЭБС, так и ППДС), а также обеспечение хорошего качества жизни пациентов с ФД на фоне трехмесячной поддерживающей терапии препаратом Хайрабезол. Использование Хайрабезола в дозе 10 мг ежедневно позволяло сохранять клиническую ремиссию заболевания в 70% случаев, а в дозе 20 мг — у 80% больных. Практически одинаковая эффективность поддерживающей терапии у пациентов первой и второй групп является основанием для того, чтобы в равной степени рекомендовать прием Хайрабезола в стандартной или половинной дозе. У 70% пациентов, не получавших поддерживающую терапию ИПП, отмечены рецидивы диспепсических симптомов.
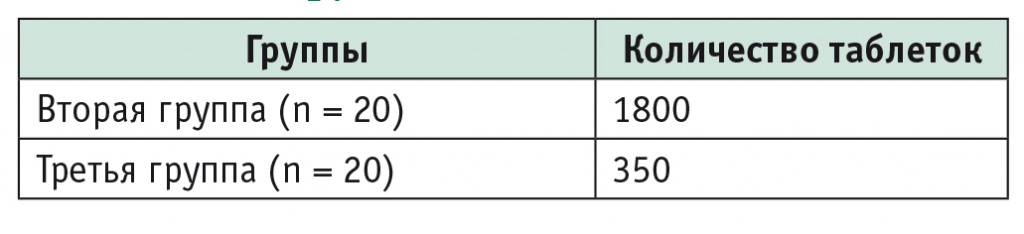
При сопоставлении клинической эффективности различных режимов поддерживающей терапии Хайрабезолом по формальным показателям, т. е. по частоте рецидивирования симптомов, выявлено, что режим «по требованию» наименее эффективен: рецидивы эпигастральной боли отмечались у 65% больных третьей группы. При детальном изучении количества дней с симптомами диспепсии и ее интенсивности также оказалось, что режимы лечения, использовавшиеся в первой и второй группах, статистически значимо превосходят режимы, применявшиеся в третьей и тем более в четвертой группе. Однако сохранение хорошего качества жизни, достигнутого в ходе курсового лечения, а также факты быстрого купирования симптомов диспепсии приемом 20 мг Хайрабезола у пациентов третьей группы позволяют в некоторых случаях рекомендовать и такой вариант поддерживающей терапии. Он может быть рекомендован, в частности, пациентам, которые с предубеждением относятся к регулярному применению лекарств либо в силу различных обстоятельств не имеют возможности соблюдать режим ежедневного приема препарата. Поддерживающая терапия по требованию может быть обоснованной также в фармакоэкономическом аспекте, который имеет важное значение для многих пациентов. Как следует из таблицы 7, количество принятых таблеток у больных третьей группы более чем в 5 раз меньше, чем во второй группе.
Таблица 7
Количество таблеток Хайрабезола 20 мг, необходимых для поддерживающей терапии пациентам с функциональной диспепсией, шт.
Выводы
- Проведение трехмесячного курса поддерживающей терапии препаратом Хайрабезол (рабепразол) в суточной дозе 10 или 20 мг пациентам с ФД существенно снижает частоту рецидивирования и выраженность симптомов диспепсии по сравнению с результатами применения прокинетиков и антацидов.
- Использование Хайрабезола в дозе 20 мг ежедневно в нашем исследовании позволяло поддерживать клиническую ремиссию заболевания у 80% пациентов с ФД, а в дозе 10 мг — у 70%.
- Быстрое купирование симптомов диспепсии при применении 20 мг Хайрабезола дает основания в отдельных случаях рекомендовать поддерживающее лечение этим препаратом в режиме «по требованию».
- Установлена хорошая переносимость трехмесячного курса поддерживающей терапии Хайрабезолом. Побочные явления были отмечены у 2 из 60 пациентов и выражались в легкой головной боли, не требовавшей отмены препараты или применения дополнительных лекарственных средств.
- Препарат Хайрабезол может быть успешно использован для поддержания клинической ремиссии заболевания у пациентов с ФД.
ЗАКЛЮЧЕНИЕ
Трехмесячный курс препарата Хайрабезол (рабепразол) в суточной дозе 10 или 20 мг у пациентов с функциональной диспепсией позволяет статистически значимо снизить частоту рецидивирования и выраженность симптомов заболевания по сравнению с результатами лечения прокинетиками и антацидами.








