ВВЕДЕНИЕ
Рак желудка (РЖ) является актуальной проблемой современной медицины, занимая пятое место в мире среди всех форм рака по частоте и распространенности и третье место среди причин смерти от злокачественных новообразований1 [1]. Канцерогенез в желудке рассматривается как мультистадийный и многофакторный процесс от нормального состояния слизистой оболочки желудка через последовательность предраковых состояний, известных как каскад Корреа (атрофия, кишечная метаплазия и дисплазия)1 [1-7].
Наиболее эффективные мероприятия по снижению распространенности РЖ и улучшению прогноза — своевременная диагностика и адекватная терапия предопухолевой патологии (хронического атрофического гастрита, кишечной метаплазии, дисплазии)1 [1-9]. В соответствии с этим принципом в некоторых странах с высокой распространенностью РЖ, таких как Япония и Южная Корея, введены программы скрининга, позволяющие значительно улучшить диагностику заболевания на ранних стадиях и увеличить выживаемость пациентов [4-12]. Так, проведение скрининга в Японии позволило снизить смертность от РЖ в течение 30 лет в 3 раза [7].
В настоящее время в качестве методов скрининга используют рентгенологический метод, эндоскопическое исследование и серологические исследования сыворотки крови на уровни пепсиногенов (ПГ). Эндоскопический скрининг наиболее чувствителен, однако имеет такие недостатки, как высокая стоимость, инвазивный характер, делающий процедуру непривлекательной для пациента, возможность развития осложнений, ограниченная доступность [5-7, 12].
Поскольку 5-летняя выживаемость пациентов с установленным РЖ чрезвычайно низка, ведется обсуждение возможности предварительного определения группы высокого риска для последующего направления на эндоскопическое исследование. Необходимо разработать усовершенствованные инструменты скрининга для ранней диагностики и выявления людей с высоким риском развития РЖ.
В последнее время широко обсуждаются возможности диагностики атрофических гастритов и предопухолевых изменений с применением сывороточных биомаркеров: пепсиногена 1 (ПГ-1), пепсиногена 2 (ПГ-2) и их соотношения (ПГ-1/2). Атрофия слизистой оболочки желудка приводит к прогрессивному снижению в сыворотке крови как уровня ПГ-1, так и ПГ-1/2. Низкое содержание сывороточных ПГ (уровень ПГ-1 ≤ 70 нг/мл и ПГ-1/2 ≤ 3,0) может служить предиктором предраковых состояний и РЖ [5, 6, 8-11, 13-15].
Тем не менее данные различаются по странам и расам, существуют противоречия в отношении достоверности этого теста для идентификации пациентов со средним и низким риском развития РЖ.
Поскольку чувствительность (65–85%) и специфичность (20–98%) теста ПГ различны в каждой стране, необходима дальнейшая работа для повышения эффективности серологического исследования при практическом использовании для скрининга предопухолевых состояний и РЖ [8, 10, 11]. Это предполагает последовательное исследование: серологическую диагностику с дальнейшим отбором для проведения ЭГДС.
Мы предположили, что, поскольку наследственность является признанным фактором риска возникновения РЖ, отягощенный наследственный анамнез может рассматриваться как потенциальный критерий стратификации популяции при формировании групп для прицельного скрининга. С позиции оценки целесообразности такого подхода представляют интерес данные о состоянии слизистой оболочки желудка у пациентов с отягощенным по раку желудка наследственным анамнезом.
Цель данного исследования: изучить возможности серологических маркеров ПГ-1, ПГ-2 и их соотношения для скрининга предраковых состояний с учетом наследственности, отягощенной по РЖ, — у родственников лиц, страдающих РЖ (РЛРЖ).
МАТЕРИАЛЫ И МЕТОДЫ
Для формирования основной группы, включавшей РЛРЖ, в период с августа 2013 г. по июль 2018 г. проводили анкетирование 107 пациентов с установленным диагнозом РЖ, проходивших лечение в учреждениях здравоохранения УЗ «Гомельский областной клинический онкологический диспансер» и УЗ «Минский городской клинический онкологический диспансер». Все взрослые родственники первой и второй степени родства (братья, сестры, родители, дети, внуки), указанные пациентами в анкете, рассматривались как потенциальные участники основной группы. Из них 114 человек выразили согласие на включение в исследование и были обследованы на базе поликлинического отделения ГУ «Республиканский научно-практический центр радиационной медицины и экологии человека» (ГУ РНПЦ РМиЭЧ) г. Гомеля (n = 54) и УЗ «Минский клинический консультативно-диагностический центр» (УЗ МККДЦ) (n = 60).
Группа сравнения состояла из 117 пациентов с симптомами диспепсии, не имевших в анамнезе ни онкологических либо предопухолевых заболеваний желудка, ни указаний на отягощенный по РЖ наследственный анамнез.
В обе группы включались лица в возрасте от 18 до 75 лет. Критериями исключения являлись отказ пациента от участия или наличие противопоказаний для проведения плановой ЭГДС (тяжелая коморбидная патология: АГ 3-й стадии, ХСН (стадия IIb по New York Heart Association), дыхательная недостаточность 2–3 ст., инфаркт миокарда или ОНМК, перенесенные менее года назад, аневризма аорты, судорожный симптом в анамнезе и др.).
Все участники исследования подписали форму информированного согласия, одобренную комитетами по этике ГУ РНПЦ РМиЭЧ г. Гомеля и УЗ МККДЦ.
Все больные прошли клиническое собеседование на основе структурированной анкеты. Анкета включала вопросы, касающиеся демографических данных, наличия и характеристики симптомов диспепсии, сопутствующих заболеваний, анамнеза эрадикации Helicobacter pylori, особенностей образа жизни, предположительно влияющих на риск развития РЖ (употребление алкоголя, курение, потребление фруктов/овощей и соли), а также наследственного анамнеза (наличие родственников с установленным РЖ).
Всем участникам исследования назначалась ЭГДС, проводившаяся по стандартной методике аппаратом Olympus GIF-XQ40. ЭГДС сопровождалась биопсией слизистой оболочки из пяти точек желудка:
1) антрального отдела по малой кривизне в 2 см от пилоруса;
2) антрального отдела по большой кривизне в 2 см от пилоруса;
3) угла желудка;
4) тела желудка по малой кривизне примерно в 8 см от кардии;
5) тела желудка по большой кривизне области, противоположной точке 4.
Кроме того, при обнаружении очаговых изменений проводилась биопсия из измененных участков.
Биоптаты из каждого отдела желудка помещались в отдельные флаконы. Биопсийный материал сопровождался разработанной биопсийной картой, содержащей краткие клинико-анамнестические сведения о пациенте и формализованное описание эндоскопической картины слизистой оболочки желудка.
Состояние слизистой оболочки желудка оценивалось по модифицированной Сиднейской системе, а также по системам гистопатологического стадирования OLGA (Operative Link for Gastritis Assessment — оперативная система оценки гастрита) и OLGIM (Operative Link on Gastric Intestinal Metaplasia Assessment — оперативная система оценки гастрита, основанная на кишечной метаплазии) [13].
Гистологические исследования проводились на базе группы патолого-анатомических исследований лаборатории клеточных технологий ГУ РНПЦ РМиЭЧ и лаборатории клинической патогистологии УЗ МККДЦ и выполнялись опытными патологоанатомами. Образцы для гистологического исследования фиксировали в 10%-ном формалине и заливали в парафин. Из блоков изготавливались гистологические срезы толщиной 4 мкм, которые окрашивались гематоксилином и эозином, а для определения H. pylori — также и по методу Гимзы (с последующей микроскопией препаратов под иммерсионным 1000-кратным увеличением).
Гастрит оценивали в соответствии с модифицированной Сиднейской системой по шкале от 0 (отсутствует/нормальный) до 3 (максимальная интенсивность) баллов. Определялись следующие характеристики слизистой оболочки желудка: активность воспаления (инфильтрация нейтрофилами), выраженность воспаления (инфильтрация лимфоцитами и плазматическими клетками), атрофия (потеря нормальных желез), кишечная метаплазия, дисплазия, наличие H. pylori. Стадию гастрита, характеризующую риск развития РЖ, оценивали по системам OLGA и OLGIM от 0 до IV.
Образцы крови брали непосредственно перед эндоскопией. Сыворотку немедленно отделяли центрифугированием и хранили при –80 °С до проведения серологического анализа на ПГ-1 и ПГ-2 и расчета соотношения ПГ-1/2. Концентрации ПГ-1 и ПГ-2 в сыворотке крови измеряли с помощью иммуноферментного определения методом твердофазного анализа («Вектор-Бест», РФ) в соответствии с инструкциями производителя.
Мы использовали значения отсечения ПГ-1 ≤ 70 нг/мл и ПГ-1/2 ≤ 3,0 [3-6, 8, 10, 15].
На основании результатов теста на сывороточные ПГ исследуемые были разделены на три группы: группа отрицательного пепсиногенового теста (ОПТ): уровень ПГ-1 > 70 нг/мл и ПГ-1/2 > 3,0; группа сомнительного пепсиногенового теста (СПТ): концентрация ПГ-1 ≤ 70 нг/мл или ПГ-1/2 ≤ 3,0; группа положительного пепсиногенового теста (ППТ): уровень ПГ-1 ≤ 70 нг/мл и ПГ-1/2 ≤ 3,0.
Возраст пациентов в исследовании представлен медианой и квартилями. Сравнение возраста в группах осуществлялось с помощью критерия Краскела — Уоллиса. Все остальные факторы представлены частотами и процентами в группе. При исследовании таблиц сопряженности использовался критерий χ2, а в случае нарушения предположений, лежащих в основе критерия χ2, — точный критерий Фишера.
При исследовании факторов, ассоциированных с возрастанием вероятности ППТ, при однофакторном анализе применялся критерий трендов, а после — многофакторная порядковая регрессия с логистической функцией связи. В качестве зависимой переменной выступала порядковая переменная, характеризующая результаты ПТ, в качестве независимых переменных — факторы, которые проявили статистическую значимость при однофакторном анализе.
Далее модель редуцировалась с помощью алгоритма пошагового исключения на базе критерия AIC [16]. Для окончательной модели рассчитывалось ОШ как экспоненциальное преобразование соответствующих коэффициентов регрессии. ДИ для ОШ рассчитывались также как экспоненциальное преобразование соответствующих доверительных интервалов коэффициентов регрессии.
Все расчеты проводились в статистическом пакете R (версия 3.6) и Statisticа 8. Результаты анализа считались статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ
Средний возраст РЛРЖ — 40,5 (33,5–54,3) года, больных группы сравнения — 37,6 (31,6–49,7) года. В группе РЛРЖ было 38 (33,3%) мужчин и 76 (66,7%) женщин, в группе сравнения — 84 (71,8%) женщины и 33 (28,2%) мужчины.
Демографические и поведенческие факторы в исследуемых группах на момент постановки диагноза, такие как возраст, пол, образ жизни (курение и употребление алкоголя), значимо не различались (p > 0,05).
По основным изменениям, выявленным визуально в процессе ЭГДС, различий между группами также не было (p > 0,05). У всех пациентов при гистологическом исследовании установлено наличие хронического гастрита, выраженного в разной степени. В таблице 1 представлены изменения слизистой оболочки желудка, выявленные при ЭГДС у РЛРЖ и лиц группы сравнения.
Таблица 1
Гистологические изменения слизистой оболочки желудка, выявленные при эзофагогастродуоденоскопии у участников исследования, n (%)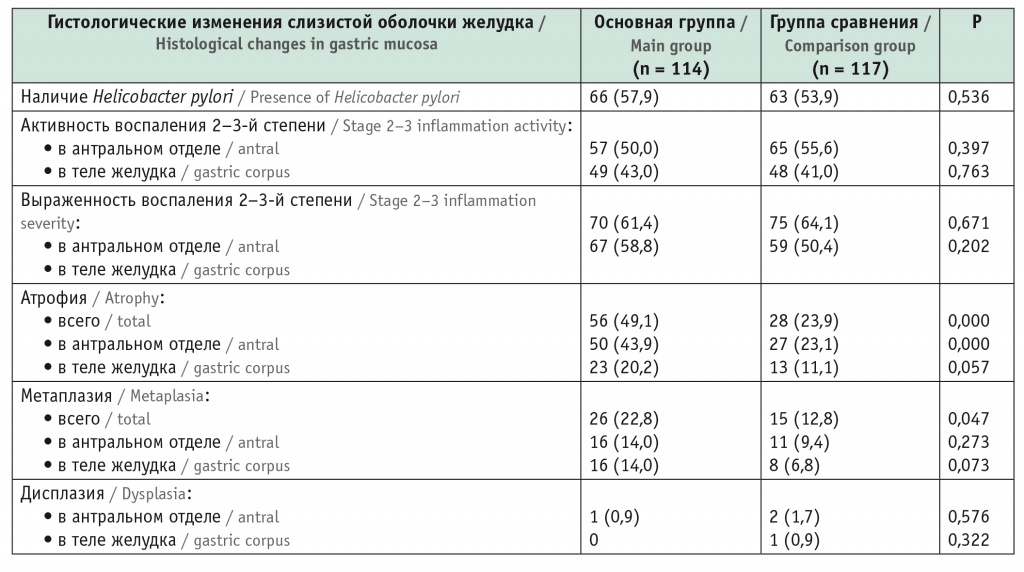
По степени активности и выраженности воспаления в антральном отделе и теле желудка значимые различия не выявлены. Распространенность инфекции H. pylori в основной группе составила 57,9% (95%-ный ДИ: 48,8–66,7%), в группе сравнения — 53,9% (95%-ный ДИ: 45,1–63,6%) (p = 0,536). Атрофия слизистой оболочки желудка любой локализации, а также атрофия антральной слизистой оболочки значимо чаще наблюдались в группе РЛРЖ (p = 0,000).
Метаплазия слизистой оболочки желудка любой локализации существенно чаще определялась у РЛРЖ (p = 0,047). Частота изолированной метаплазии в антральном отделе в группах не различалась (p > 0,05). Дисплазия была выявлена у 3 человек (1 из основной и 2 из группы сравнения) и во всех случаях имела легкий характер.
Средний возраст пациентов с атрофией слизистой оболочки желудка в группе РЛРЖ — 45,9 года (95%-ный ДИ: 44,8–52,2 года), в группе сравнения — 54,7 года (95%-ный ДИ: 48,5–57,6 года) (p < 0,001). Гастрит в стадиях низкого риска (I–II стадия) диагностировали в возрасте 44,1 года (95%-ный ДИ: 42,9–51,0 года) в основной группе и в 53,5 года (95%-ный ДИ: 48,2–57,7 года) в группе сравнения (p = 0,002), что отражает более раннее развитие атрофии у РЛРЖ. Пациентов с гастритом высокого риска (III–IV стадии) в группе РЛЖР было восемь, а в группе сравнения — только один, что не позволяет равнозначно оценить возраст лиц с данными изменениями.
У всех участников (n = 231) проводилось исследование на уровни ПГ, в результате которого были исключены 5 человек из-за отсутствия результатов (табл. 2).
Таблица 2
Уровни пепсиногенов (ПГ) у участников исследования, Ме (95%-ный доверительный интервал) 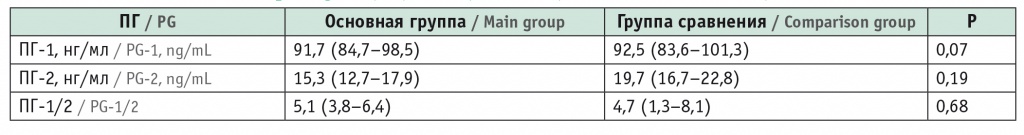
По концентрациям ПГ и их соотношению значимых различий между группами не было.
Затем пациенты (n = 226) были разделены на три группы по результатам ПТ: ОПТ, СПТ и ППТ. Распространенность ОПТ среди участников исследования составила 53,5% (121 из 226; 95%-ный ДИ: 46,6–60,0%), СПТ — 34,5% (78 из 226; 95%-ный ДИ: 28,4–41,0%), ППТ — 12,0% (27 из 226; 95%-ный ДИ: 7,7–16,3%).
Результаты ПТ в зависимости от наличия факторов риска, выявленных при однофакторном анализе, представлены в таблице 3. Они не зависели от пола (p = 0,73), курения (p = 0,646), факта употребления крепких алкогольных напитков и частоты употребления любого алкоголя (p = 0,925 и p = 0,862 соответственно), ограничения соли в рационе (p = 0,350), частоты употребления овощей и фруктов (p = 0,636), эрадикации H. pylori в анамнезе (p = 0,730), наличия гиперхолестеринемии (p = 0,870) или гипергликемии (p = 0,351). Во всех группах большинство участников ранее проходили ЭГДС.
Таблица 3
Результаты пепсиногенового теста (ПТ) в зависимости от наличия факторов риска, выявленных при однофакторном анализе 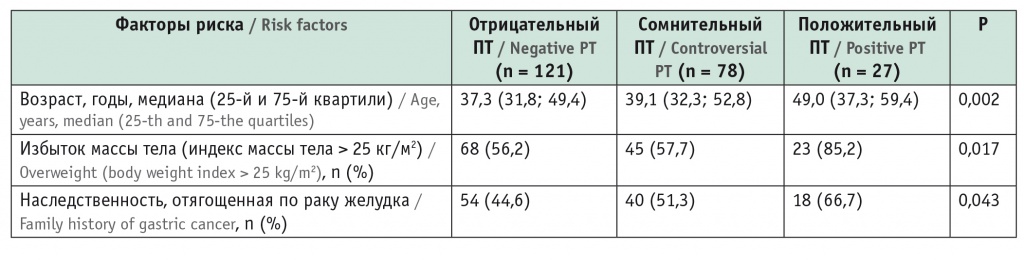
Найдена связь результатов ПТ с возрастом (p = 0,002) и избыточной массой тела (p = 0,024), наследственностью, отягощенной по РЖ (p = 0,043).
У всех пациентов проводилось исследование ЭГДС с биопсией. Визуально установлено наличие гастропатии разной степени выраженности без значимого различия по частоте встречаемости между группами.
У всех больных независимо от результатов ПТ при гистологическом исследовании диагностирован хронический гастрит, выраженный в различной степени (табл. 4). По наличию на момент обследования H. pylori и по эрадикации в анамнезе группы существенно не отличались (p > 0,05). Сравнение групп по степени активности воспаления показало, что активность в теле желудка значимо выше при СПТ и ППТ (p = 0,031 при 0–1 ст. и p = 0,025 при 2–3 ст.).
Таблица 4
Результаты пепсиногенового теста (ПТ) в зависимости от гистологических параметров, выявленных при эзофагогастродуоденоскопии, n (%) 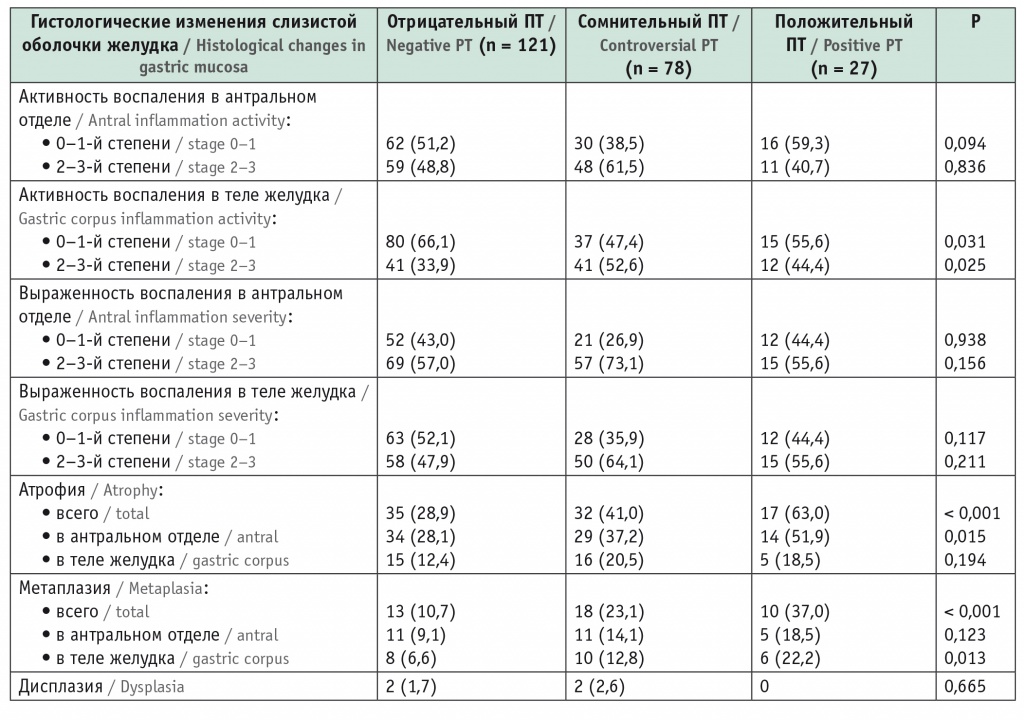
Атрофию, кишечную метаплазию и дисплазию рассматривают как предраковые изменения желудка [3-9].
Атрофия слизистой оболочки желудка любой локализации существенно чаще определялась в группе ППТ (p < 0,001), преимущественно за счет атрофии в антруме (p = 0,015).
Частота выявления метаплазии в целом также значительно различалась между группами (p < 0,001). Показана значимая связь результатов ПТ с локализацией метаплазии в теле желудка (p = 0,013), но не в антральном отделе (p = 0,123), несмотря на тенденцию к увеличению ее распространенности в антральном отделе в группе ППТ.
Эти данные позволяют говорить о взаимосвязи ППТ и наличия атрофии, в частности в антральном отделе, и метаплазии, особенно локализованной в теле желудка. В нашем исследовании не выявлена связь дисплазии и ППТ (p = 0,665).
Результаты стадирования гастрита по системам OLGA и OLGIM представлены в таблице 5. Стадии I–IV по OLGA определялись у 28,9% пациентов в группе ОПТ, у 41,0% участников группы СПТ и у 63,0% в группе ППТ, что соответствует частоте выявления атрофии слизистой оболочки желудка. Стадии низкого риска (I–II) в группе ОПТ выявлялись значимо реже (25,6%), чем при СПТ (37,2%) и ППТ (59,3%). Распространенность стадий высокого (III–IV) риска имела тенденцию к повышению в группах СПТ и ППТ.
Таблица 5
Результаты пепсиногенового теста (ПТ) в зависимости от стадирования гастрита по OLGA и OLGIM, n (%)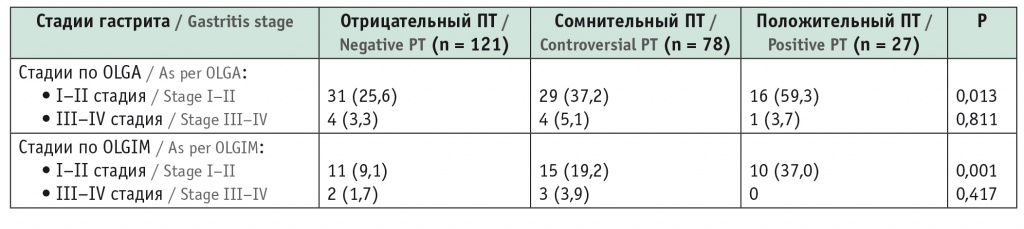
При оценке гастрита по тяжести развития метаплазии по OLGIM наблюдалось значимое увеличение количества больных с I–II стадией в группах СПТ (19,2%) и ППТ (37,0%) по сравнению с таковым в группе ОПТ (9,1%) (p = 0,001).
Для проведения многофакторного анализа использованы факторы риска, установленные в ходе однофакторного анализа. По данным многофакторного анализа, значимыми независимыми факторами риска ППТ оказались наследственность, отягощенная по РЖ (p = 0,037), избыток массы тела (ИМТ > 25 кг/м2) (p = 0,003), выраженная активность в теле желудка (2–3-я степени) (p = 0,018), а также наличие метаплазии (вне зависимости от локализации) (p = 0,008) (табл. 6).
Таблица 6
Значимые независимые факторы риска, влияющие на результаты пепсиногенового теста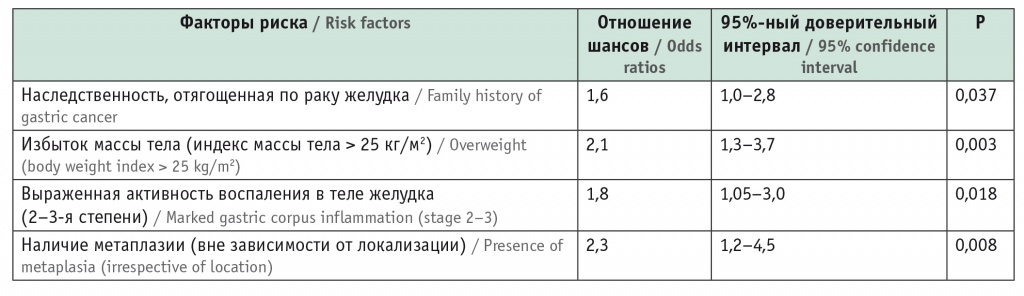
ОБСУЖДЕНИЕ
В данном исследовании мы оценивали результаты ПТ в зависимости от состояния слизистой оболочки желудка у РЛРЖ и лиц группы сравнения, не имевших отягощенного по РЖ наследственного анамнеза.
По результатам макроскопической оценки слизистой оболочки верхних отделов ЖКТ (наличие гастропатии, полипов, язв, эрозивной гастроэзофагеальной рефлюксной болезни) значимых различий между группами не было.
В нашем исследовании не обнаружено влияние колонизации слизистой оболочки желудка H. pylori на результаты ПТ. H. pylori выявлен у 62 человек (51,2%; 95%-ный ДИ: 44,3–57,7%) в группе ОПТ, у 13 (48,1%; 95%-ный ДИ: 41,3–54,7%) в группе ППТ и у 49 (62,8%; 95%-ный ДИ: 55,5–68,5%) в группе СПТ. Возможно, установленная в нашем исследовании частота инфицированности относительно невелика, поскольку более 25% участников уже подвергались эррадикационной терапии.
Сходные данные о том, что ППТ может служить предиктором РЖ и предопухолевой патологии желудка независимо от наличия инфекции H. рylori, получены и другими авторами [16]. По результатам ряда исследований, H. pylori влияет на уровни ПГ, а также на желудочную секрецию, преимущественно за счет действия на концентрацию ПГ-2 [5, 6, 8-11].
В нашем исследовании результаты ПТ ассоциированы с активностью воспаления умеренной и выраженной степени в теле желудка: 33,9% (95%-ный ДИ: 27,2–39,8%) в группе ОПТ против 52,6% (95%-ный ДИ: 45,9–59,3%) в группе СПТ и 44,4% (95%-ный ДИ: 37,8–51,0%) в группе ППТ.
Мы обнаружили, что у РЛРЖ чаще, чем в группе сравнения, наблюдается атрофия слизистой оболочки желудка любой локализации (49,1% против 23,9%), а также атрофия слизистой оболочки антрального отдела желудка (43,9% против 23,1%).
При проведении серологического исследования у всех участников наличиие атрофии значимо взаимосвязано с результатами ПТ (28,9% при ОПТ, 41,0% при СПТ и 63,0% при ППТ) (p < 0,001). По локализации атрофия в антральном отделе взаимосвязана с уровнями ПГ, а для атрофии в теле желудка такая связь не выявлена. Эти данные дают основание предполагать, что атрофия встречается у РЛРЖ значимо чаще, а результаты ПТ являются неинвазивным биомаркером для диагностики и прогнозирования течения хронического атрофического гастрита, преимущественно локализованного в антральном отделе.
Сходные данные получены и другими авторами. В португальском исследовании хронический атрофический гастрит у РЛРЖ был диагностирован в 70% случаев и у 32% участников группы сравнения (p < 0,001) [17-19].
Существуют сведения о том, что уровень сывороточного ПГ отражает морфологический и функциональный статус слизистой оболочки желудка и служит маркером хронического атрофического гастрита и кишечной метаплазии [8, 9, 11, 16].
В нашем исследовании кишечная метаплазия слизистой оболочки желудка любой локализации значительно чаще определялась в группе РЛРЖ (p = 0,047). Однако по локализации метаплазии в антральном отделе и теле желудка различий между группами исследования не было. Эти данные позволяют думать о возможной тенценции к более частому и выраженному развитию метаплазии у лиц с отягощенной наследственностью по РЖ.
По результатам однофакторного анализа частота метаплазии значимо коррелировала с ППТ (37,0% против 23,1% в группе СПТ и 10,7% в группе ОПТ) (p < 0,001). Найдена взаимосвязь между ППТ и ее локализацией в теле желудка (p = 0,013), но не в антральном отделе (p = 0,123).
Существуют работы, в которых показана связь наследственного анамнеза РЖ и развития кишечной метаплазии. Имеются также данные о том, что уровень сывороточного ПГ отражает морфологический и функциональный статус слизистой оболочки желудка и служит маркером метаплазии [9].
Для стадирования гастрита мы использовали классификационную систему OLGA, предназначенную для оценки риска возникновения РЖ. Мы выявили, что у лиц с ППТ чаще, чем при ОПТ и СПТ, имел место гастрит (p < 0,001), в частности I–II стадии (p = 0,013).
При использовании системы OLGIM отмечалась значимая взаимосвязь наличия I–II стадии с серологическими маркерами: 9,1% при ОПТ против 19,2% при СПТ и 37,0% при ППТ (p = 0,003).
В отношении применения классификаций OLGA и OLGIM при проведении ПТ существуют лишь единичные исследования. Например, по данным M. Rugge и соавт., установлена значительная обратная корреляция соотношения ПГ-1/2 и стадии гастрита по OLGA (p < 0,001) [13]. Анализ связи стадии гастрита по OLGIM с уровнем ПГ-1 в сыворотке продемонстрировал существенное его снижение с увеличением стадии по OLGIM (p < 0,001) [20].
В нашем исследовании число лиц со стадией высокого риска незначительно, и необходимо дополнительно изучить влияние указанной патологии на результаты ПТ. Но можно предположить взаимосвязь результатов ПТ и наличия рисков развития атрофии и метаплазии еще на стадии гастрита низкого риска (I–II), но мы не можем уточнить степень указанных рисков у конкретного пациента.
По нашим данным, результаты ПТ не зависели от пола, курения, факта и частоты употребления крепких алкогольных напитков, ограничения соли в рационе, частоты употребления овощей и фруктов, эрадикации H. pylori в анамнезе, наличия гиперхолестеринемии или гипергликемии. При однофакторном анализе нами выявлена взаимосвязь ППТ с возрастом, избыточной массой тела и наследственностью, отягощенной по РЖ.
ЗАКЛЮЧЕНИЕ
Наши данные еще раз подтверждают известную связь между возрастом и риском развития предопухолевых изменений слизистой оболочки желудка, а также наличие неблагоприятного влияния избыточной массы тела на риск рака желудка (РЖ).
Неинвазивный метод оценки изменений слизистой оболочки желудка с помощью определения антител к Helicobacter pylori и уровня пепсиногена 1 в крови считается в настоящее время перспективным. Однако применение серологических пепсиногеновых тестов (ПТ) должно быть изучено в разных популяциях и регионах. В исследованиях, проводимых в Азии и Европе, используются разные тест-системы и методы. В большинстве азиатских исследований применяется метод агглютинации латекса, в то время как в Европе в основном пользуются тестами ELISA, поэтому результаты не могут быть сопоставимы.
Таким образом, необходимо проведение региональных исследований для дальнейшего изучения использования уровней пепсиногенов для скрининга предраковых состояний. В то же время чувствительность и специфичность ПТ значительно выше для обнаружения атрофии, чем РЖ: 66,7–84,6% и 73,5–87,1% против 36,8% и 62,3% соответственно [2].
_______________
1 New Global Cancer Data: GLOBOCAN 2018. Paris; 2018. URL: https://www.uicc. org/new-global-cancer-data-globocan-2018 (дата обращения — 15.09.2020).
Поступила: 15.05.2020
Принята к публикации: 19.06.2020








