В настоящее время отмечается неуклонный рост числа пациентов с диффузными заболеваниями печени[1, 2]. При этом серьезной проблемой для здравоохранения остается терминальная стадия поражения печени — цирроз[1, 3]. Основным этиологическим фактором цирроза печени являются хронические вирусные инфекции, вызванные гепатотропными вирусами В и С[1, 3, 4].
Высокий уровень заболеваемости и смертности от цирроза печени и его осложнений требует ранней, точной постановки диагноза, а также уточнения степени фиброза для дальнейшего прогноза и выбора лечебной тактики[2, 5]. На сегодняшний день «золотой стандарт» диагностики фиброза печени у больных с хроническими вирусными гепатитами (ХВГ) — биопсия печени, которая является инвазивным методом, а значит, несет определенные риски для здоровья пациента (кровотечение, инфекции и т. д.). Кроме этого, оценка гистологического материала имеет ряд недостатков, снижающих диагностическую ценность биопсии[2, 4, 5]. Поэтому остается актуальным вопрос о внедрении в клиническую практику неинвазивного и высокоинформативного метода диагностики степени поражения паренхимы печени.
На сегодняшний день в гепатологии широко используется такой метод медицинской визуализации, как контраст-усиленное УЗИ (КУУЗИ), для диагностики очаговой патологии[6, 7]. Для уточнения локализации очагового образования и определения степени фиброза печень рассматривается как мультисегментарный орган, так как процесс фиброзной трансформации протекает в ней неравномерно[5, 8].
Современные ультразвуковые препараты — внутрисосудистые агенты, а размер микропузырьков не превышает 6–7 нм, что позволяет визуализировать не только крупные сосуды печени, но и микроциркуляторное русло всей паренхимы. Это делает КУУЗИ перспективным методом комплексной оценки степени фиброза или стадии цирроза печени[6, 7, 9–11].
Цель исследования: оценить возможности использования качественных параметров КУУЗИ для ранней неинвазивной диагностики у пациентов с ХВГ.
МАТЕРИАЛЫ И МЕТОДЫ
В 2019 году на базе проблемной научно-исследовательской лаборатории «Диагностические исследования и малоинвазивные технологии» были обследованы 54 пациента с ХВГ: 29 (53,7%) мужчин и 25 (46,3%) женщин (табл. 1). Группы были рандомизированы по полу, возрасту и тяжести клинического течения. Пациенты с выраженным клиническим течением (виремия > 105 МЕ/мл; АЛТ, АСТ > 5 норм) составили первую группу (n = 33), c минимальными клиническими проявлениями (виремия < 105 МЕ/мл; АЛТ, АСТ < 2 норм) — вторую группу (n = 21).
Таблица 1
Общая характеристика обследованных пациентов
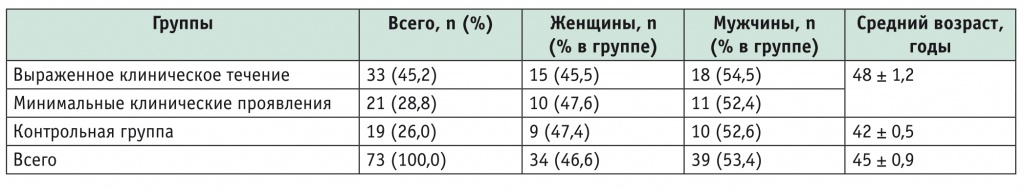
Больные с умеренно выраженной активностью ХВГ не включены в настоящее исследование, что сделано для проверки работоспособности предлагаемой модели полуколичественной оценки КУУЗИ.
Для оценки неизмененной паренхимы печени была набрана контрольная группа, в которую вошли 19 человек без ХВГ.
Исследование выполнено в соответствии с Хельсинкской декларацией и одобрено этическим комитетом Смоленского государственного медицинского университета (протокол № 9 от 23.11.2018 г.).
Статистически значимых различий по гендерному составу между группами пациентов с различным клиническим течением ХВГ не было (p ≥ 0,05). Медиана возраста в основной группе — 48 (31–65) лет, в контрольной — 42 (28–56) года.
УЗИ печени проведено по мультипараметрическому протоколу: В-режим + цветовое допплеровское картирование сосудов печени + эластография сдвиговой волны (2DSWE). Проведено также КУУЗИ всех участников на УЗ-аппарате Hitachi Preirus (Hitachi, Япония) в специализированном режиме Contrast с использованием конвексного датчика 3–6 МГц. При этом были установлены следующие значения механического индекса: для В-режима — 0,04, для режима Contrast — 0,06, что способствует более длительной циркуляции ультразвукового контрастного препарата и предотвращает его быстрое разрушение[10].
Для контрастирования использовался контрастный препарат 2-го поколения, разрешенный на территории РФ, — SonoVue (Bracco, Италия), представляющий собой лиофилизированный порошок гексафторида серы SF6. Для проведения КУУЗИ печени применялся 1,0 мл SonoVue, который вводился внутривенно струйно с последующим введением 5 мл физиологического раствора для усиления болюсного эффекта. Для внутривенного введения контрастного агента использовался двухпортовый периферический катетер G19 (диаметр — 0,9 мм), что также предотвращало разрушение микропузырьков.
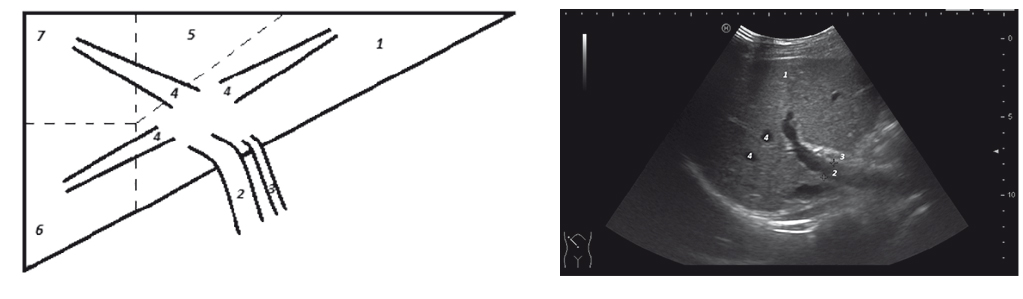
Одновременно с введением контрастного препарата проводилась запись видеопетли длительностью не менее 6 минут для оценки всех фаз контрастирования: артериальной, портальной и поздней венозной, — поскольку контрастирование печени сохраняется от 6 до 8 минут[6, 7, 9]. Перед началом контрастирования добивались такой визуализации в В-режиме, чтобы на монитор УЗ-аппарата попали воротная вена, печеночная артерия и печеночные вены (рис. 1).
Рис. 1. Ультразвуковое исследование печени в В-режиме: 1 — печень, 2 — воротная вена, 3 — печеночная артерия, 4 — печеночные вены, 5 — 5-й сегмент печени, 6 — 6-й сегмент печени, 7 — 7-й сегмент печени. Здесь и далее в статье иллюстрации авторов
Качественные параметры контрастирования оценивали в IV, V, VI, VII сегментах печени по двум методикам: стандартной качественной[6, 7, 10, 11] и предложенной нами полуколичественной.
Референтным методом служила биопсия печени, которую осуществили у 25 (46,3%) больных после предварительного подписания информированного согласия. При отказе от биопсии в качестве референтного метода применялась только эластография печени (53,7% участников). Эластография сдвиговых волн проведена у 100% пациентов.
Для подтверждения клинического диагноза ХВГ анализу подвергались данные лабораторных (вирусная нагрузка, биохимический анализ крови) и инструментальных исследований (УЗИ органов брюшной полости в В-режиме, эластография печени).
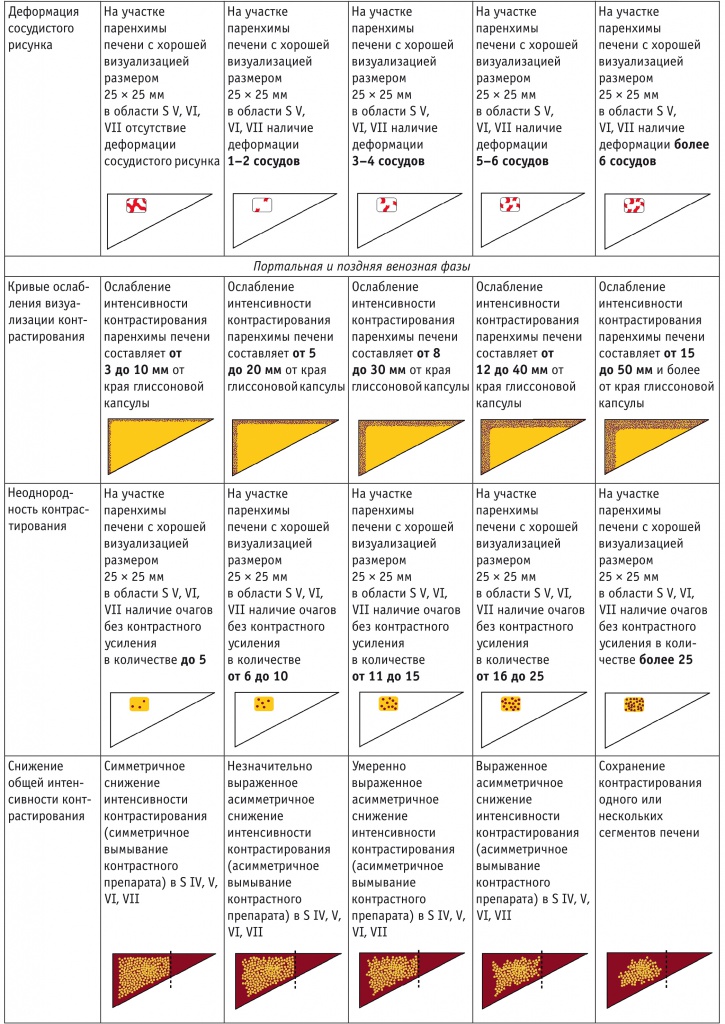
В соответствии с Европейскими методическими рекомендациями по КУУЗИ печени 2012 г.[10] и валидированным переводом для отечественных специалистов[11], выделены следующие качественные параметры: в артериальную фазу — симметричность накопления контрастного препарата и деформация сосудистого рисунка; в портальную и позднюю венозную фазы — кривые ослабления визуализации контрастирования, неоднородность контрастирования, снижение общей интенсивности контрастирования и задержка вымывания контрастного препарата (сладж-синдром). Для уменьшения субъективности оценки КУУЗИ нами предложена полуколичественная стандартизированная оценка качественных параметров КУУЗИ в баллах.
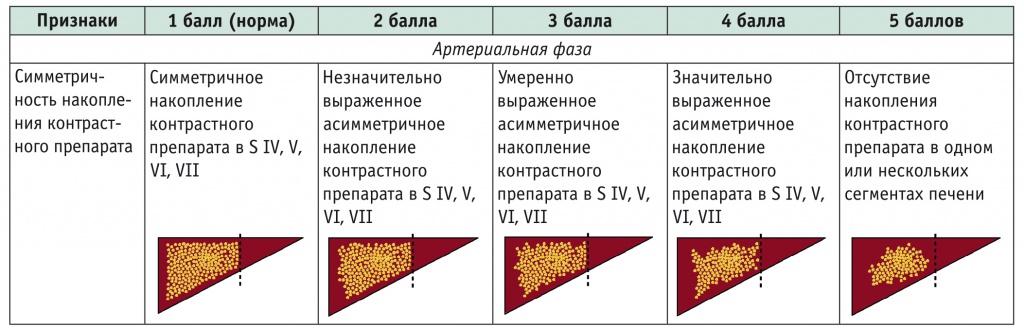
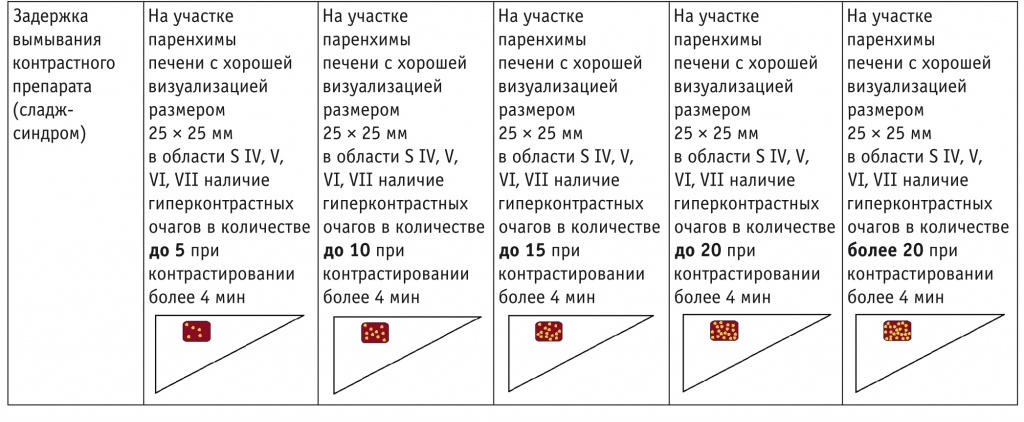
Согласно предложенной системе оценки качественных параметров КУУЗИ (полуколичественной), каждому признаку присваивается значение от 1 до 5 баллов (табл. 2). За основу были приняты работы M. Bertolotto и соавт. и А.В. Борсукова и соавт. по оценке степени васкуляризации паренхимы почек в режиме энергетического допплера по 5-балльной шкале и по стандартизированной качественной оценке допплерографии почек соответственно[12, 13].
Таблица 2
Полуколичественная оценка контраст-усиленного ультразвукового исследования печени
РЕЗУЛЬТАТЫ
Распределение баллов оценки КУУЗИ по каждому признаку в различных группах представлено в таблице 3.
Таблица 3
Распределение качественных признаков контраст-усиленного ультразвукового исследования в обследуемых группах, баллы (процент участников с данным числом баллов)
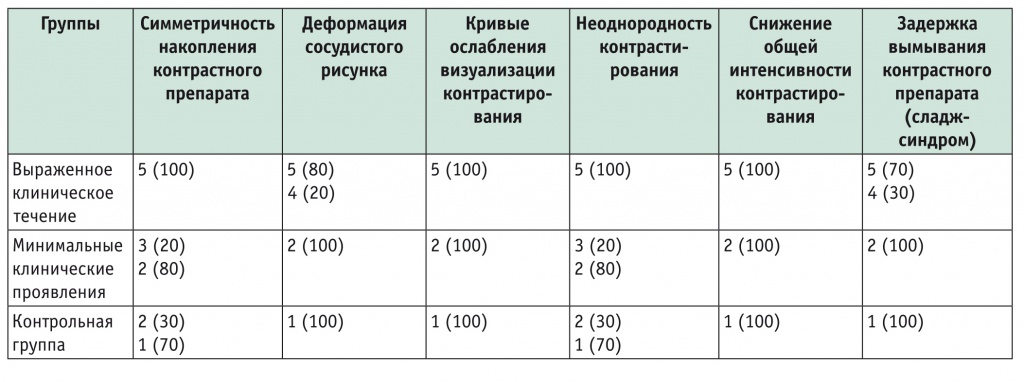
Как следует из таблицы 3, значение таких признаков, как симметричность накопления контрастного препарата и неоднородность контрастирования, в первой группе составило 5 баллов у 100% пациентов, во второй группе — 2 и 3 балла у 80% и 20% больных соответственно, в контрольной группе — 1 и 2 балла у 70% и 30% соответственно. Распределение таких признаков, как кривые ослабления визуализации контрастирования и снижение общей интенсивности контрастирования, было одинаковым у всех участников в каждой группе: 5, 2 и 1 балл соответственно.
Анализируя полученные данные, можно сделать вывод, что максимальное число баллов получено в первой группе (от 28 до 30), а минимальное количество — в контрольной (от 6 до 8), что подтверждает работоспособность предложенной модели.
Полуколичественная оценка по предлагаемой системе проводилась специалистом сразу во время исследования, а затем повторный анализ видеопетель осуществлялся другим специалистом по стандартному методу субъективной оценки КУУЗИ[6, 7, 10, 11]. При этом повторный просмотр видеопетель повышал качество оценки на 25% и в том, и в другом случае, так как в течение самого исследования оценить качественные параметры во время таких фаз, как артериальная и портальная, достаточно затруднительно в силу их небольшой продолжительности — около 15 и 90 секунд соответственно.
При сравнении методов диагностики состояния паренхимы печени сделан вывод, что предложенная система полуколичественной оценки КУУЗИ уступает таким методам, как биопсия и эластография, но превосходит оценку качественных параметров по стандартной методике (табл. 4).
Таблица 4
Сравнительная характеристика диагностической точности методов оценки состояния паренхимы печени (с расчетом r — коэффициента корреляции Пирсона[14])
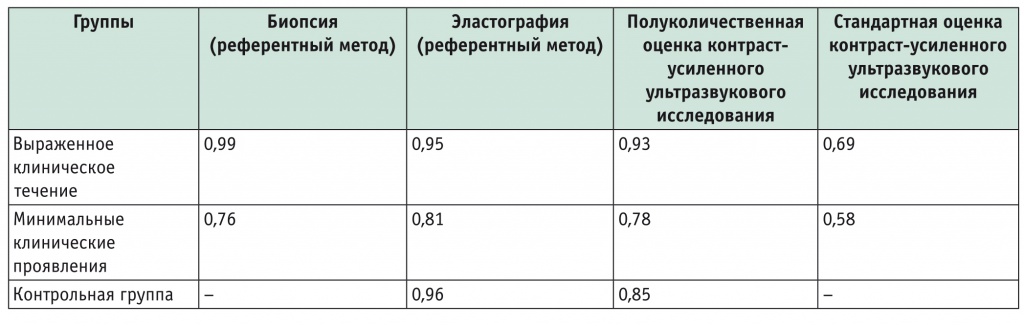
Предложенная в настоящем исследовании полуколичественная оценка качественных параметров КУУЗИ является перспективным методом диагностики патологии печени, поскольку процесс фиброзной трансформации протекает неравномерно в силу неоднородного строения печени и проходит несколько стадий до окончательного перехода в цирроз[5, 8], а процесс визуализации при КУУЗИ охватывает все микроциркуляторное русло[6, 7, 9–11] и позволяет сделать вывод о состоянии паренхимы печени в целом, именно поэтому в группе пациентов с минимальной степенью активности данная система оценки несколько превосходила по эффективности биопсию.
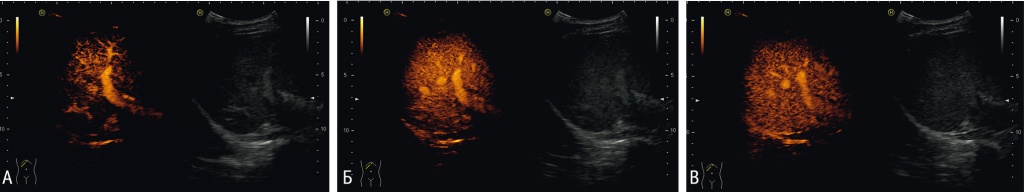
Клинический пример 1. Больная И., 31 год. В 2015 г. установлен диагноз ХВГ С минимальной степени активности, генотип 1b. АЛТ — 28,6 Ед/л; АСТ — 33,5 Ед/л. Сумма баллов полуколичественной оценки — 6 (рис. 2).
Рис. 2. Больная И., 31 год. Хронический вирусный гепатит С минимальной степени активности. Артериальная фаза (А) — симметричное накопление контрастного препарата, отсутствие деформации сосудистого рисунка. Портальная (Б) и поздняя венозная (В) фазы — ослабление интенсивности контрастирования паренхимы не превышает 10 мм от края глиссоновой капсулы, симметричное снижение интенсивности контрастирования, отсутствие очагов неоднородного вымывания и задержки контрастного препарата
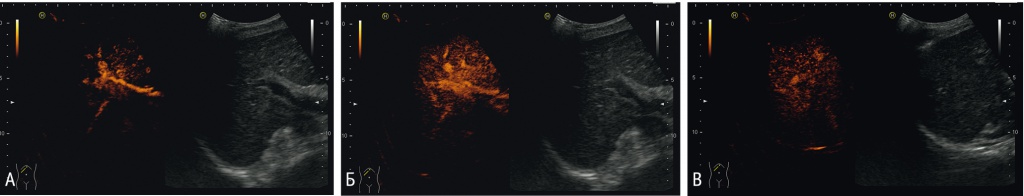
Клинический пример 2. Больной О., 56 лет. В 2013 году установлен диагноз ХВГ С выраженной степени активности, генотип 1b. АЛТ — 115,1 Ед/л, АСТ — 80 Ед/л. Сумма баллов полуколичественной оценки — 29 (рис. 3).
Рис. 3. Больной О., 56 лет. Хронический вирусный гепатит С выраженной степени активности. Артериальная фаза (А) — асимметричное накопление контрастного препарата, деформация 4 сосудов. Портальная (Б) и поздняя венозная (В) фазы — ослабление интенсивности контрастирования паренхимы составляет от 15 до 20 мм от края глиссоновой капсулы, асимметричное снижение интенсивности контрастирования, наличие очагов неоднородного вымывания и очагов задержки контрастного препарата в количестве более 20
ЗАКЛЮЧЕНИЕ
Предложенная система полуколичественной оценки контраст-усиленного УЗИ (КУУЗИ) предназначена для диагностики состояния паренхимы печени при диффузных заболеваниях, в том числе и при хронических вирусных гепатитах.
Стандартная качественная оценка параметров КУУЗИ по стадиям менее эффективна (r = 0,58–0,69), чем предложенная полуколичественная балльная оценка этих же параметров (r = 0,78–0,93).
Применение КУУЗИ для постановки заключительного клинического диагноза диффузных заболеваний печени необходимо в составе комплексного лабораторно-инструментального обследования, включающего в себя эластографию, ПЦР и, при возможности, биопсию.








