Гастроэнтерологические заболевания и во взрослой, и в детской врачебной практике относятся к наиболее частым1 [1]. Кислотозависимые заболевания в силу ключевой роли желудка в ранней фазе пищеварения охватывают патологию многих смежных органов, включая гастроэзофагеальную рефлюксную болезнь, язвенные поражения двенадцатиперстной кишки, панкреатиты и многое другое [2, 3].
Блокаторы Н+/К+-аденозинтрифосфатазы (Н+/К+-АТФазы) — ключевого фермента образования водородных ионов, необходимых для секреции соляной кислоты, —получившие название ингибиторов протонных помп (ИПП), относятся к антисекреторным лекарственным препаратам. Они широко применяются при различных кислотозависимых заболеваниях желудка, двенадцатиперстной кишки и пищевода [2–6].
Всплеск популярности у педиатров пришелся на начало XXI века, когда анализ назначений в разных странах (около 12,9 млн взрослых и 1,3 млн детей в возрасте до 12 месяцев) выявил увеличение частоты выписки ИПП в педиатрической практике более чем в 7 раз с 1999 г. по 2004 г. [7].
Популярность ИПП связана с тем, что они ингибируют финальную стадию секреции соляной кислоты, при этом эффективное подавление кислотообразования достигается при приеме один раз в сутки, к ИПП не развивается толерантность, не возникает синдром «рикошета» после отмены, нет существенных побочных эффектов [4, 8, 9]. Крупные метаанализы не выявили значимые различия по эффективности кислотоподавления между отдельными представителями класса ИПП [10].
ФАРМАКОЛОГИЧЕСКИЕ АСПЕКТЫ
Фармакодинамика и фармакокинетика ИПП связаны с функцией фермента, обеспечивающего секрецию соляной кислоты в париетальных клетках, — Н+/К+-АТФазы. Стимуляция выработки соляной кислоты в желудке происходит под воздействием различных лигандов — ацетилхолина, гастрина и гистамина, что приводит к конформационным изменениям в H+/K+-АТФазе [11, 12]. АТФаза транспортирует ион водорода из цитоплазмы париетальной клетки через апикальную мембрану в просвет желудка, обменивая его на ион калия, который переносится внутрь клетки [13].
Механизм действия всех ИПП связан с блокированием функции H+/K+-АТФазы [11, 13]. АТФаза содержит 28 молекул цистеина (Цис), десять из которых доступны для связывания ИПП. Активированные молекулы ИПП связываются с остатком Цис АТФазы с образованием дисульфидных связей, вызывая их блокировку. ИПП связываются с несколькими остатками Цис протонной помпы.
Скорость блокирования образования кислоты зависит от количества блокированных Цис в протонных помпах париетальной клетки [4, 12, 13]. Дисульфидные связи, создаваемые ИПП, постоянно инактивируют протонную помпу [14].
Активация — важный этап фармакодинамики ИПП. Являясь слабыми основаниями, они могут быть максимально протонированы лишь в кислой среде протоков париетальных клеток, потому в кровотоке они находятся в виде неактивных пролекарств [8]. В канальцах париетальных клеток рН может достигать 1,0–0,8. Этот факт в значительной степени обусловливает селективное накопление препаратов. Концентрация бензимидазолов в секреторных канальцах париетальных клеток почти в 1000 раз больше, чем в крови [12]. Образующийся сульфенамид плохо проходит через мембраны, поскольку является катионом. Это обеспечивает селективное накопление активной формы ИПП в секреторных канальцах париетальных клеток.
После активации протонированием молекулы ИПП связываются с одним или несколькими Цис в канале протонной помпы, приводя его в неактивное состояние [15, 16]. Восстановление кислотопродуцирующего потенциала париетальной клетки возможно за счет синтеза новых молекул протонных помп.
T1/2 протонных помп составляет от 54 до 96 часов, это объясняет надежное ингибирование выработки кислоты, притом что сами ИПП имеют короткий период полужизни (от 1,5 до 3 ч).
Оптимальная активность ИПП обеспечивается при приеме натощак за 30–60 мин до еды (лучше до первого приема пищи, активирующего наибольшее число протонных помп). Прием в такое время не только улучшает всасывание, но и синхронизирует пиковые уровни ИПП в плазме с наличием большого количества активированных приемом пищи протонных помп [8, 12, 17].
ОСОБЕННОСТИ ФАРМАКОДИНАМИКИ ИНГИБИТОРОВ ПРОТОННЫХ ПОМП В ДЕТСКОМ ВОЗРАСТЕ
Долгое время считалось, что у новорожденных и детей первых месяцев жизни соляная кислота не вырабатывается или вырабатывается в незначительном количестве. Связано это с тем, что материнское молоко успешно створаживается под воздействием амилазы и других ферментов и не требует участия соляной кислоты. Но исследования показали, что желудочные железы младенцев способны вырабатывать достаточное количество кислоты для поддержания базальной кислотности желудка на уровне рН < 4 [18]. Относительный объем секретируемой соляной кислоты достигает уровня взрослых примерно через 5–6 месяцев после рождения [19].
Кажется, что для ингибирования продукции относительно небольшого количества соляной кислоты в желудке младенца требуется меньшая доза ИПП. Однако назначаемые младенцам дозы в 7–9 раз превышают те, которые обычно применяются у взрослых [4, 19]. Таким образом, использование различных ИПП для лечения новорожденных и детей первых месяцев жизни требует дальнейшего изучения. Назначение ИПП детям старше 2 лет регламентировано действующими инструкциями по медицинскому применению препаратов.
Ключевую роль в метаболизме ИПП, как и других лекарственных препаратов, играют цитохромы Р450 в печени [20, 21]. У взрослых вариации в конститутивной экспрессии ферментов, ответственных за биотрансформацию ИПП, существенно влияют на скорость метаболизма, что продемонстрировано на примере омепразола [22] и лансопразола [23]. Исследования фармакокинетики ИПП у новорожденных [24, 25], детей младшего возраста (до 2 лет) [26, 27] и в возрасте от года до 16 лет [28–30] показали, что фармакокинетика ИПП в детском возрасте не зависит от дозы и генетических особенностей цитохромов. Связано это с невысокой активностью ферментов биотрансформации в организме ребенка [31–33].
НЮАНСЫ ПРИМЕНЕНИЯ ИНГИБИТОРОВ ПРОТОННЫХ ПОМП В ДЕТСКОЙ ГАСТРОЭНТЕРОЛОГИИ
Показана эффективность ИПП в лечении кислотозависимых заболеваний у детей, в том числе ассоциированных с инфекцией Helicobacter pylori. Детальное исследование результатов длительного лечения кислотозависимых заболеваний с использованием ИПП в течение 32–47 месяцев у 133 детей в возрасте от 0,1 до 17,6 года доказало безопасность столь длительного использования ИПП [34]. Так, гиперплазия париетальных клеток выявлена не более чем у 16% пациентов в течение всего периода наблюдения. При гистологическом исследовании нормальная слизистая оболочка желудка обнаруживалась чаще при длительности лечения более 48 месяцев и/или приеме высоких доз препаратов. Отмечалась некритичная гипергастринемия, концентрация витамина B12 оставалась в норме. Наилучшие показатели у детей до одного года зафиксированы при использовании омепразола и эзомепразола [6].
Эффективность омепразола подтверждена во многих исследованиях с участием детей в возрасте старше одного года [6, 27, 28, 35]. Он широко применяется в педиатрической практике и в нашей стране [4, 5]. Важно, что использование у детей прописано в инструкции, например Омез® (ООО «Др. Редди’с Лабораторис») разрешен в педиатрической практике. При этом не все ИПП имеют показания для применения у детей, например ряд омепразолов, а пантопразол, рабепразол, лансопразол и декслансопразол противопоказаны детям.
Омез® рекомендован для лечения гастроэзофагеальной рефлюксной болезни у детей в возрасте старше 2 лет с массой тела больше 20 кг в дозе 20 мг один раз в сутки 4–8 недель (рекомендованная доза омепразола для лечения гастроэзофагеальной рефлюксной болезни в педиатрической практике составляет 0,7–3,3 мг на килограмм массы тела ребенка в сутки); при язве двенадцатиперстной кишки, вызванной H. pylori, Омез® может назначаться детям старше 4 лет с массой тела больше 20 кг в комбинации с антибактериальными препаратами (рекомендованная доза омепразола в схемах эрадикации H. pylori в педиатрической практике составляет 1–2 мг на килограмм массы тела ребенка в сутки).
Еще одним аспектом выбора препаратов при лечении кислотозависимых заболеваний и гастроэзофагеальной рефлюксной болезни в частности является их патогенетическая, а не симптоматическая направленность. В этом плане показательно исследование компании Comcon: педиатры продолжают назначать антациды значительно чаще ИПП (табл.).
Таблица
Антисекреторные лекарственные препараты, назначенные детям в возрасте до 19 лет в 17 городах (данные от Q2 2021)
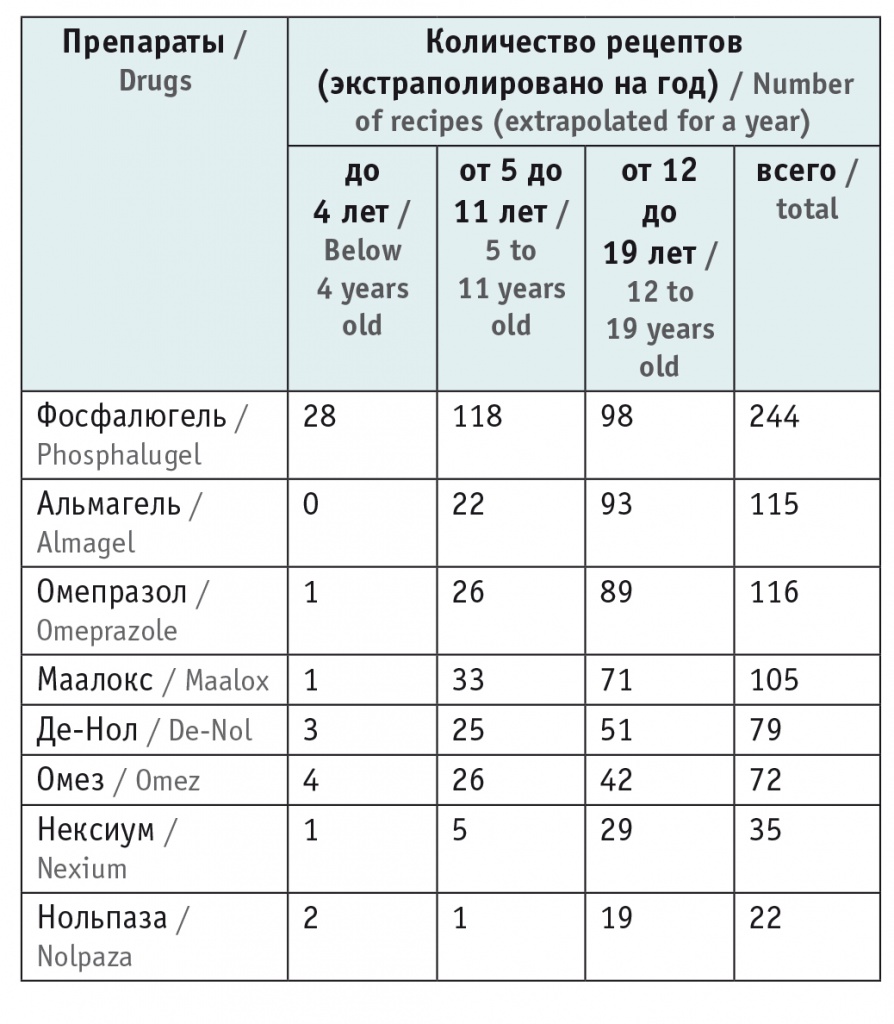
Очевидно, что использование антацидных препаратов при кислотозависимых заболеваниях не решает проблему. Антацидные препараты неплохо нейтрализуют кислоту, находящуюся в просвете желудка, но не контролируют выработку соляной кислоты. К недостаткам этой группы следует отнести и малую продолжительность действия: даже длительно действующие препараты эффективны в течение не более 1,5–2 часов. Для достижения эффекта лечение антацидами требует частого приема больших доз препаратов, что может приводить к развитию побочных и нежелательных эффектов. Побочные эффекты от приема антацидов могут проявляться нарушением стула с появлением запоров или диареи в зависимости от того, алюминий- или магний-содержащие препараты принимал больной. Кроме того, длительное использование антацидов может привести к нарушению минерального баланса в организме с развитием алкалоза. Поэтому антацидные препараты не могут использоваться как основные при лечении кислотозависимых состояний [36].
Немаловажный критерий выбора лекарственных средств — фармакоэкономический. Стоимость оригинальных препаратов до окончания срока действия патента высока, а среди дженерических препаратов одним из доступных является Омез®, выпускаемый по рецептуре оригинального производителя и обладающий несомненными преимуществами в фармакоэкономическом плане. Кроме того, Омез® включен в Оранжевую книгу Food and Drug Administration (FDA) (биоэквивалентность категории А), что дополнительно подтверждает его эффективность и безопасность.
Таким образом, Омез® можно считать «золотым стандартом» терапии, потому что это первый ИПП, появившийся в России, для него накопились обширная доказательная база, большой опыт применения у докторов различных специальностей. Полный цикл производства Омеза соответствует международным стандартам GMP, что доказывается включением его в Оранжевую книгу FDA США2.
ЗАКЛЮЧЕНИЕ
Антисекреторная терапия обоснована и доказанно эффективна при кислотозависимых заболеваниях ЖКТ в педиатрической практике. Ингибиторы протонных помп (ИПП) имеют ряд преимуществ перед антацидами. Выбор конкретного препарата ИПП в педиатрии должен учитывать, помимо клинических характеристик, еще и юридические моменты, а именно наличие показаний к применению при конкретном заболевании, так как врачи несут ответственность за назначение лекарственных препаратов не по показаниям (офф-лейбл).
Омепразол имеет убедительную доказательную базу в педиатрической гастроэнтерологии, однако при его назначении следует учитывать не только клинические особенности конкретного пациента, но и нормативные документы, например инструкции по медицинскому применению ИПП в детском возрасте по конкретным показаниям: многие омепразолы в нашей стране имеют противопоказания к применению в детском возрасте. При этом препарат Омез®, доказавший биоэквивалентность референтному препарату, обладающий экономическими преимуществами, включает внесенные в инструкцию показания для лечения у детей гастроэзофагеальной рефлюксной болезни и язвы двенадцатиперстной кишки, вызванной Helicobacter pylori.
Поступила: 13.10.2021
Принята к публикации: 10.11.2021
________
1 Россия в цифрах 2017. Краткий статистический сборник. М.: Росстат; 2017. 513 c.
2 Food and Drug Administration. URL: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=078490 (дата обращения — 06.09.2021).21).








