ВВЕДЕНИЕ
В современных условиях преобладают заболевания, отличающиеся системностью поражения, мультифакториальностью и развитием коморбидности. Актуальность проблемы коморбидных состояний обусловлена четко наметившейся тенденцией к дальнейшему росту их числа в популяции, что вызывает определенные трудности лечебно-диагностического процесса и снижение качества жизни пациентов [1].
Клиническое значение в медицинской практике этого понятия не может рассматриваться как результат суммации количества болезней и утяжеления состояния больного, оно определяется маркерностью отдельных сочетаний болезней. Согласно современным рекомендациям, коморбидность — сосуществование двух и более заболеваний у одного пациента, патогенетически и генетически связанных между собой [2].
Механизмы коморбидности многообразны, особое место среди них занимают висцеральные состояния с генетической детерминированностью и наследственными аномалиями [3, 4]. В формировании коморбидности важнейшую роль играют универсальные патофизиологические механизмы, имеющие общепатологическое значение, такие как хроническое системное воспаление, тканевая гипоксия, генотоксический эффект, развитие эндотелиальной дисфункции. В основе коморбидности лежит закономерно частое сочетание определенных болезней с общностью этиологических факторов или патогенетических механизмов — синтропия (вид полипатологии).
Гены, обусловливающие развитие синтропий, локализованные во всем пространстве генома человека, определяют биохимический метаболизм. В настоящее время установлено, что ассоциации болезней на уровне клинических фенотипов имеют молекулярно-генетическую основу — общие гены и перекрывающиеся метаболические пути [5, 6]. Следовательно, изучение патологического состояния на уровне генетических и фенотипических признаков имеет большое практическое значение для выявления болезней, имеющих определенные маркеры коморбидности.
В настоящее время для исследования связи всех заболеваний человека («феном» болезней) с полным списком генов, контролирующих заболевание («геном» болезней), разработана концептуальная основа, что создает картину известных ассоциаций «ген — болезнь» [7]. Фенотипическая информация о сочетании болезней человека по мере совершенствования технологий генотипирования дополняется построением генных сетей с последующим анализом «ген-феном» ассоциаций. Примером концептуальной основы ассоциации «феном» болезней и «ген — болезнь» являются целиакия и многочисленные дисплазии соединительной ткани, сопровождающиеся аномалиями желчного пузыря (ЖП). Наличие аномалий тканевой структуры ЖП становится базой для формирования клинико-функциональных нарушений органов пищеварения при целиакии [8].
На основе собственных клинических наблюдений нами ранее описана коморбидность целиакии с синдромом билиарной дисфункции, расцененная нами как природно-видовое сочетание патологических состояний [9]. В настоящее время, согласно новым Римским критериям IV (2016), функциональные билиарные расстройства диагностируются при наличии болей в правом подреберье, вызванных моторно-тонической дисфункцией ЖП и сфинктера Одди (СО) и отсутствием структурных и биохимических изменений билиарного тракта [10].
При целиакии в происхождении первичной билиарной дисфункции имеет значение патология гладкомышечных клеток ЖП, сопровождающаяся нарушением сократительной способности ЖП, реологических свойств желчи, изменением дуоденальной зоны и большого дуоденального сосочка (БДС). Речь идет об анатомических изменениях строения ЖП и его различных аномалиях, которые влияют на функцию ЖП преимущественно по гипотоническому типу и создают условия для развития билиарной недостаточности [11].
Как известно, важным модулем в процессе пищеварения считается двенадцатиперстная кишка (ДПК), где происходит переход от желудочного переваривания к кишечному и регулирование секреторной, моторной и эвакуаторной деятельности органов пищеварения. Главной мишенью при глютеновой энтеропатии является ДПК с характерными признаками хронического воспаления и атрофического процесса ультраструктуры микроворсинок и снижения синтеза гастроинтестинальных гормонов пептидной природы, в частности холецистокинина [12].
К физиологическим эффектам холецистокинина относят регуляцию дуоденальной фазы пищеварения, а также регулирование билиарной функции, касающееся опорожнения ЖП и расслабления СО [13].
Причиной билиарной дисфункции у больных целиакией может являться длительное существование хронического дуоденита, характеризующееся структурными изменениями слизистой оболочки ДПК воспалительно-дистрофического, дисрегенераторного характера, приводящими к атрофии слизистой оболочки и нарушению основных функций ДПК.
Предположения о связи воспалительного процесса ДПК и синдрома билиарной дисфункции изложены ранее в отечественных работах. Патология желчевыводящих путей в 80–85% случаев сопровождается дуоденитом, а в 70–85% случаев — дискинетическими расстройствами ДПК [14]. При целиакии хроническое воспаление и атрофические изменения слизистой оболочки ДПК могут выступать в качестве единого патогенетического фактора вторичной билиарной дисфункции. С другой стороны, имеющиеся аномалии ЖП как висцеральные признаки дисплазии соединительной ткани, сопровождающиеся снижением сократительной функции, можно рассматривать в качестве первичной причины билиарных нарушений при целиакии.
Итак, при целиакии билиарная дисфункция имеет смешанный этиопатогенез, а маркерами в формировании коморбидной патологии могут служить топические билиарные факторы: патоморфологические изменения ДПК и БДС, анатомические особенности строения ЖП, снижение сократительной функции < 40%.
С учетом вышеперечисленных аспектов коморбидности при целиакии в конечном механизме синдрома мальабсорбции решающее значение следует придавать билиарной дисфункции: аномалиям, застою желчи на фоне гипокинезии ЖП и нарушению реологии желчи, хроническому воспалению стенки при одновременном снижении поступления желчных кислот в ДПК.
Следовательно, развитие синдрома мальабсорбции у больных целиакией — полиэтиологический симптомокомплекс. Атрофические изменения слизистой оболочки ДПК не могут рассматриваться как единственная причина нарушенного всасывания, важным патогенетическим звеном в развитии мальабсорбции является также недостаточное поступление желчи в ДПК на фоне билиарной дисфункции. Поэтому улучшение реологии желчи играет существенную роль в коррекции билиарной дисфункции у больных целиакией на фоне исключения глютена.
В целом патогенетическая связь сосуществующих заболеваний билиарной системы и целиакии еще нуждается в дальнейшем изучении.
Цель настоящего исследования: определить ведущие клинико-диагностические маркеры коморбидности, отражающие риск развития билиарной патологии при целиакии.
МАТЕРИАЛЫ И МЕТОДЫ
Обследованы 133 больных целиакией с наличием боли или дискомфорта в правом верхнем квадранте живота, которые находились на амбулаторном и стационарном обследовании в гастроэнтерологическом отделении ФГБОУ ВО «СЗГМУ им. И.И. Мечникова» в период с 2016 по 2018 г. Средний возраст участников составил 31,6 ± 11,5 года (от 18 до 44 лет). Соотношение мужчин и женщин — 1 : 1,1 (62 (46,6%) и 71 (53,4%) соответственно).
Диагноз целиакии устанавливался на основании данных клинической картины, анамнеза, генетического профиля крови с выявлением HLA-DQ2 и HLA-DQ8 и антител к тканевой трансглутаминазе IgА и IgG, чьи уровни превышали 10 ед/мл, на основании результатов эндоскопического исследования и гистоморфологического исследования биопсии слизистой оболочки ДПК у пациентов, не соблюдавших безглютеновую диету [15].
Показатели субъективной клинической симптоматики оценивали по данным опроса и анкетирования пациентов, объективную клиническую симптоматику — по данным физикального обследования. При характеристике клинической симптоматики определяли наличие у пациентов субъективных клинических критериев синдрома функционального расстройства ЖП и CО (Римские критерии IV) при отсутствии данных о другой гепатобилиарной патологии [10].
Билиарную дисфункцию и желчнокаменную болезнь (ЖКБ) верифицировали на основании клинических данных, характерных изменений сократительной функции и выявления конкрементов в просвете ЖП по данным УЗИ. Дифференциальную диагностику патологии БДС осуществляли путем выполнения дуоденоскопии в НИИ скорой помощи им. И.И. Джанелидзе (Санкт-Петербург) в эндоскопическом отделении.
РЕЗУЛЬТАТЫ
Клиническая характеристика обследованных пациентов
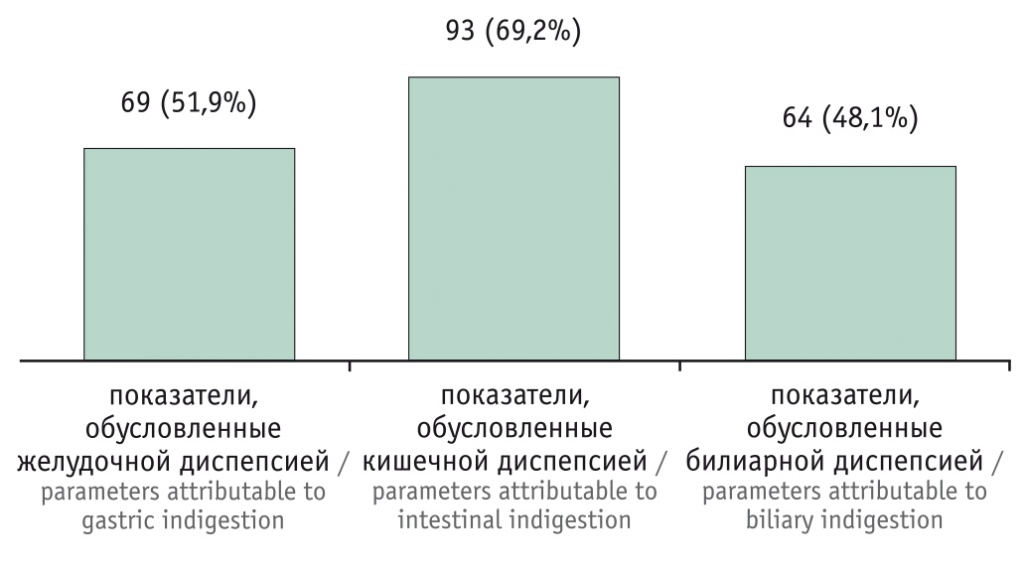
Анализ субъективных расстройств показал, что пациенты предъявляли разнообразные жалобы, обусловленные патологией верхних отделов пищеварительной и билиарной систем. Клиническая картина патологии верхних отделов органов пищеварения характеризовалась наличием боли в эпигастральной области — 68 (51,1%), отрыжки — 69 (51,9%), изжоги — 70 (52,6%).
Со стороны нижних отделов наблюдались следующие симптомы кишечной диспепсии: боль в левом подреберье — 24 (18,0%), абдоминальная боль — 48 (36,1%), вздутие, урчание в животе — 93 (69,9%), нарушение стула по типу запора — 52 (39,1%), диарея — 36 (27,1%), неустойчивый стул — 40 (30,1%). Проявлениями билиарной патологии были ощущение горечи — 48 (36,1%), боли в правом подреберье — 60 (45,1%), тошнота в утреннее время — 48 (36,1%). Кроме гастроэнтерологических симптомов пациенты отмечали различные внекишечные проявления — 35 (26,3%), слабость — 21 (15,8%).
Полученные данные (рис. 1) наглядно свидетельствуют о том, что наряду с синдромом желудочной и кишечной диспепсии у 48,1% пациентов обнаружен синдром билиарной боли, диспепсия.
Рис. 1. Клинические показатели больных целиакией
Анализ эндоскопических признаков
При эндоскопическом исследовании у всех пациентов с целиакией выявлены признаки воспалительных изменений пищевода, желудка и ДПК. Признаки неэрозивного поражения слизистой оболочки пищевода в виде катарального дистального эзофагита найдены у 62 (46,6%) обследованных, признаки эрозивного поражения слизистой оболочки пищевода — у 28 (21,0%). У 20 (15,1%) больных наблюдали степень А эрозивного эзофагита, у 8 (6,1%) — степень В, согласно Лос-Анджелесской классификации (1-я и 2-я степень Savary — Miller).
Признаки воспаления слизистой оболочки желудка были у 99 (74,4%) человек, эрозивные изменения антрального отдела желудка — у 48 (36,1%), отек и гиперемия слизистой оболочки луковицы ДПК — у 102 (76,7%). Эрозивный бульбит диагностирован у 25 (18,8%) обследованных, у 14 (10,5%) пациентов — парапапиллярный дивертикул, что стало впервые обнаруженной находкой.
Признаками функциональных нарушений в верхних отделах пищеварительного тракта и дискинезии желчевыводящих путей служили изменения в виде недостаточности кардии — 63 (47,4%), дуодено-гастрального рефлюкса — 55 (41,4%), отсутствие желчи в просвете ДПК — 32 (24,1%). Наличие вышеперечисленных признаков можно отнести к висцеральным стигмам дисплазии соединительной ткани.
Гистоморфологическое исследование пациентов
Как видно на рисунке 2, результаты гистоморфологического исследования свидетельствуют, что у больных наблюдались все стадии гистологических изменений слизистой оболочки ДПК по классификации М.N. Маrsh.
Рис. 2. Распределение активности дуоденита в зависимости от стадии целиакии, согласно классификации M.N. Marsh
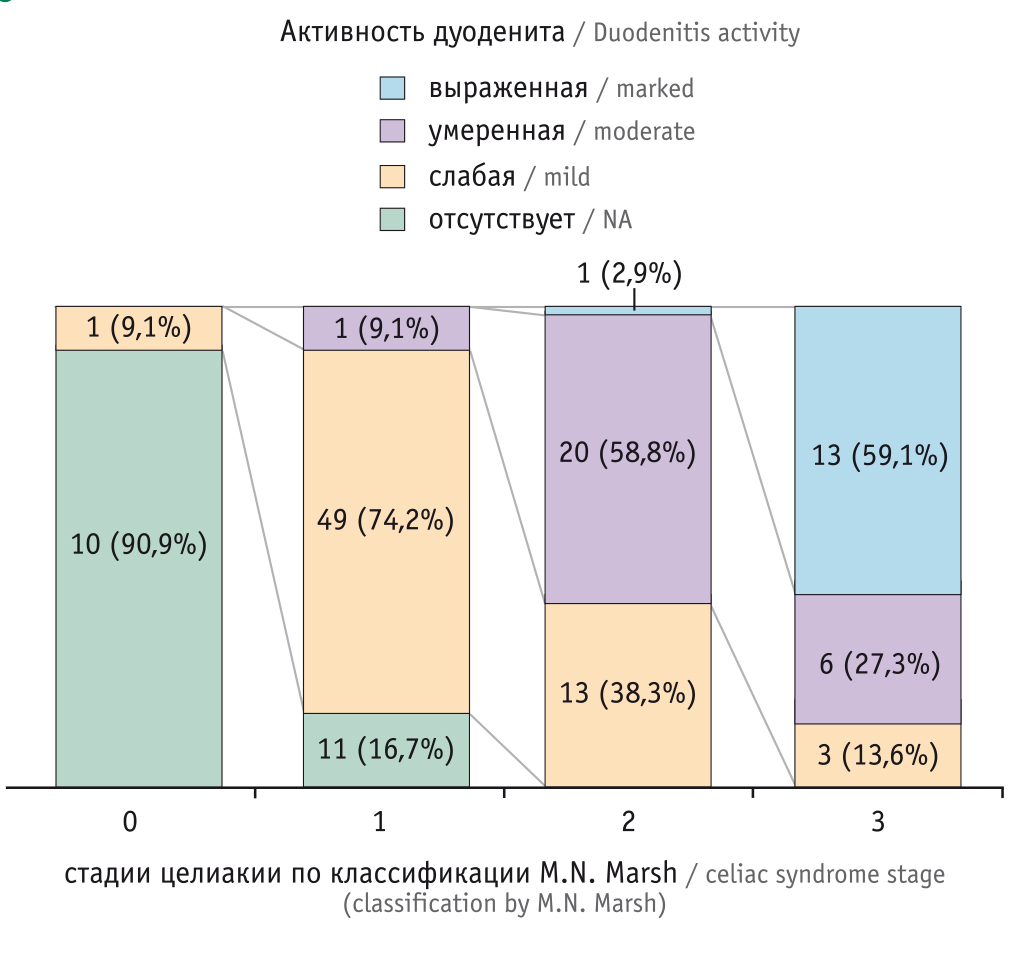
В соответствии с критериями классификации R. Whitehead, у больных целиакией определяли три степени выраженности хронического дуоденита. У лиц с хроническим дуоденитом разной степени были признаки воспаления (отек стромы и полнокровие сосудов), но при этом они различались по распространенности. У 21 (15,8%) человека отсутствовали признаки активности воспалительного процесса, среди них 10 пациентов имели нормальную гистологическую картину, у 11 гистологическая картина соответствовала 1-й стадии целиакии. У 66 (49,6%) больных диагностирован хронический дуоденит I степени, среди них у 74,2% гистологическая картина соответствовала 1-й стадии целиакии, у 38,3% — 2-й стадии.
У 32 (24,1%) участников определяли хронический дуоденит II степени, среди них преобладали лица с гистологической картиной 2-й (58,8%) и 3-й (27,3%) стадии. Хронический дуоденит III степени наблюдали у 14 (10,5%) пациентов, из них у 13 была гистологическая картина 3-й стадии целиакии (по M.N. Marsh).
Из вышеизложенного следует, что по мере нарастания выраженности гистологических изменений от 0 до 3-й стадии значимо снижалась доля пациентов с отсутствием активности дуоденита (от 90,9% до 0, р < 0,001), а доля больных с умеренной (от 0 до 58,8%, р < 0,001) и выраженной (от 0 до 59,1%, р < 0,001) активностью дуоденита, напротив, закономерно увеличивалась.
Эндоскопическое исследование большого дуоденального сосочка
С целью изучения характера морфологических изменений БДС и оценки степени воспаления у 32 пациентов с выраженным болевым синдромом проводилась биопсия для морфологического исследования. Забор материала из неизмененной слизистой БДС осуществлялся во время проведения дуоденоскопии для гистоморфологического исследования.
При изучении биоптатов, взятых из БДС, получены следующие варианты гистологической картины: у 22 (68,7%) пациентов встречалась гиперпластическая форма, у 7 (21,8%) — атрофическая и у 3 (9,5%) — аденоматозная форма БДС. На основании полученных результатов биопсии БДС выявлены нижеследующие изменения: лимфоплазмоцитарная инфильтрация (44,4%), лейкоцитарная инфильтрация (22,6%), дистрофические изменения железистого эпителия, гиперплазия желез (62,9%) (χ2(3) = 48,53; р < 0,001; С = 0,75), что позволяет рассматривать указанные изменения как одну из причин влияния на пассаж желчи.
Для уточнения влияния воспалительного процесса ДПК на морфологические изменения БДС оценивали активность дуоденита и характер клеточной инфильтрации слизистой оболочки БДС.
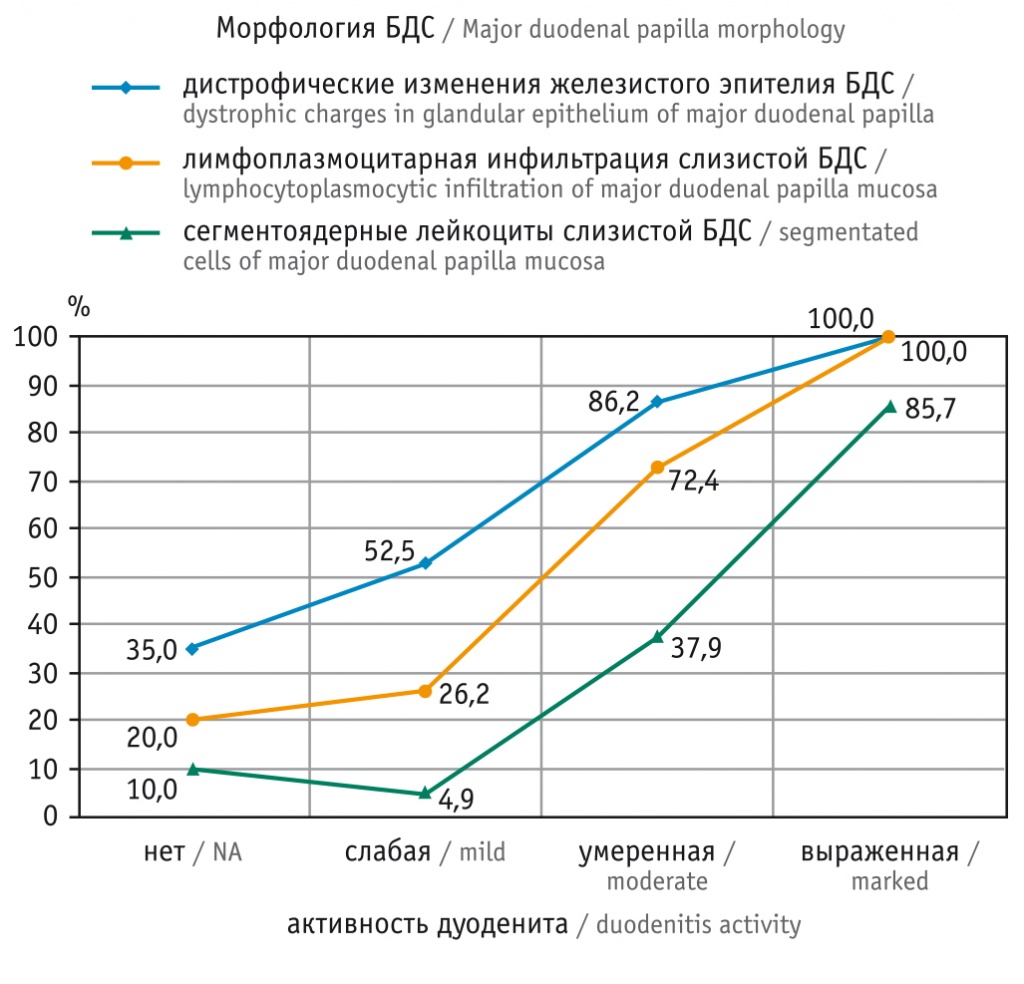
По результатам анализа активности дуоденита и морфологических изменений БДС установлена их высокозначимая сопряженность (коэффициент взаимной сопряженности С = 0,75; p < 0,001) (рис. 3).
Рис. 3. Взаимосвязь активности дуоденита и морфологических показателей большого дуоденального сосочка (БДС)
Ультрасонографическое исследование
По результатам инструментального исследования у больных целиакией диагностированы аномалии, связанные с изменением формы ЖП. У 44 (33,1%) пациентов выявлена S-образная форма ЖП, у 42 (31,6%) — перегиб в области тела ЖП и у 47 (35,3%) — перегиб в области шейки ЖП. Особый интерес представляет изучение взаимосвязи аномалий и сократительной функции ЖП.
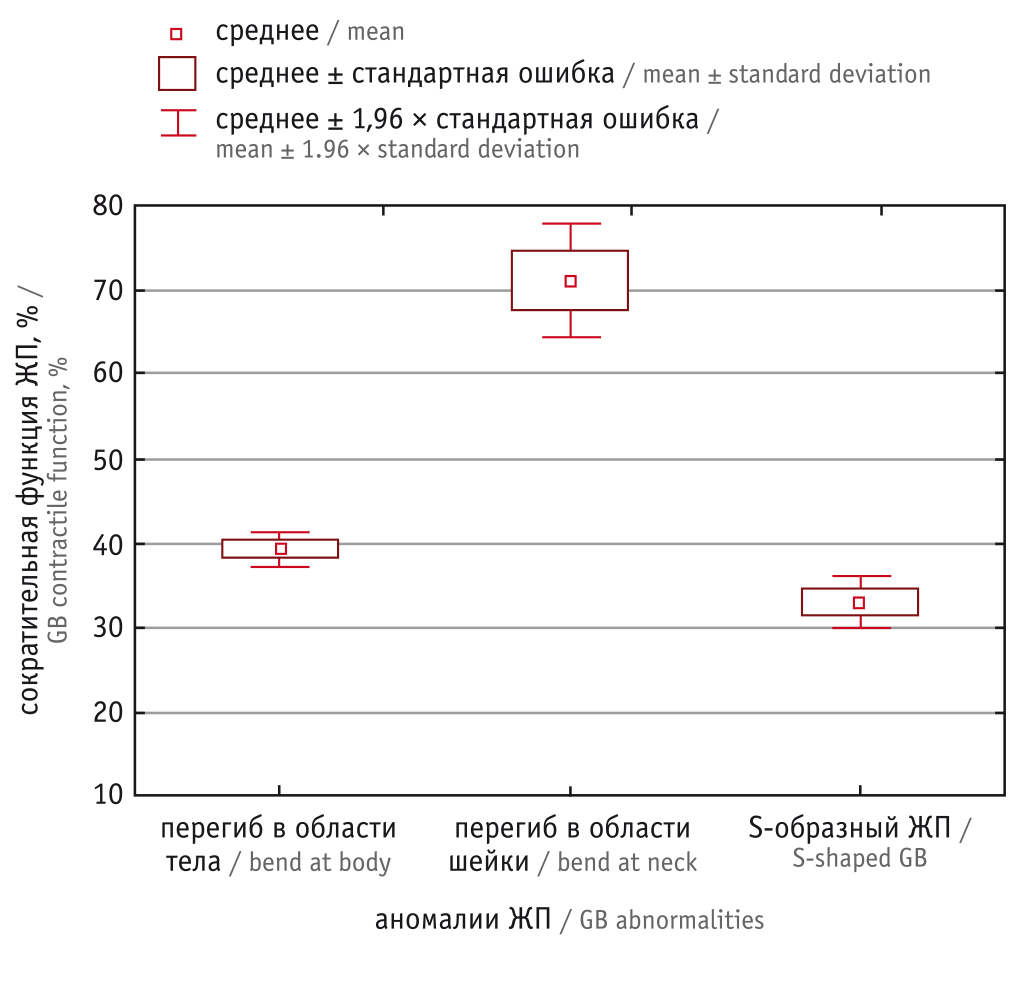
Установлено, что у пациентов с перегибом в области тела и S-образной формой сократительная функция ЖП понижена, а у больных с перегибом в области шейки — повышена. Таким образом, становится очевидным, что тип дискинетических расстройств у больных целиакией зависит от вида аномалий ЖП (рис. 4).
Рис. 4. Показатели сократительной функции желчного пузыря (ЖП) при различных аномалиях
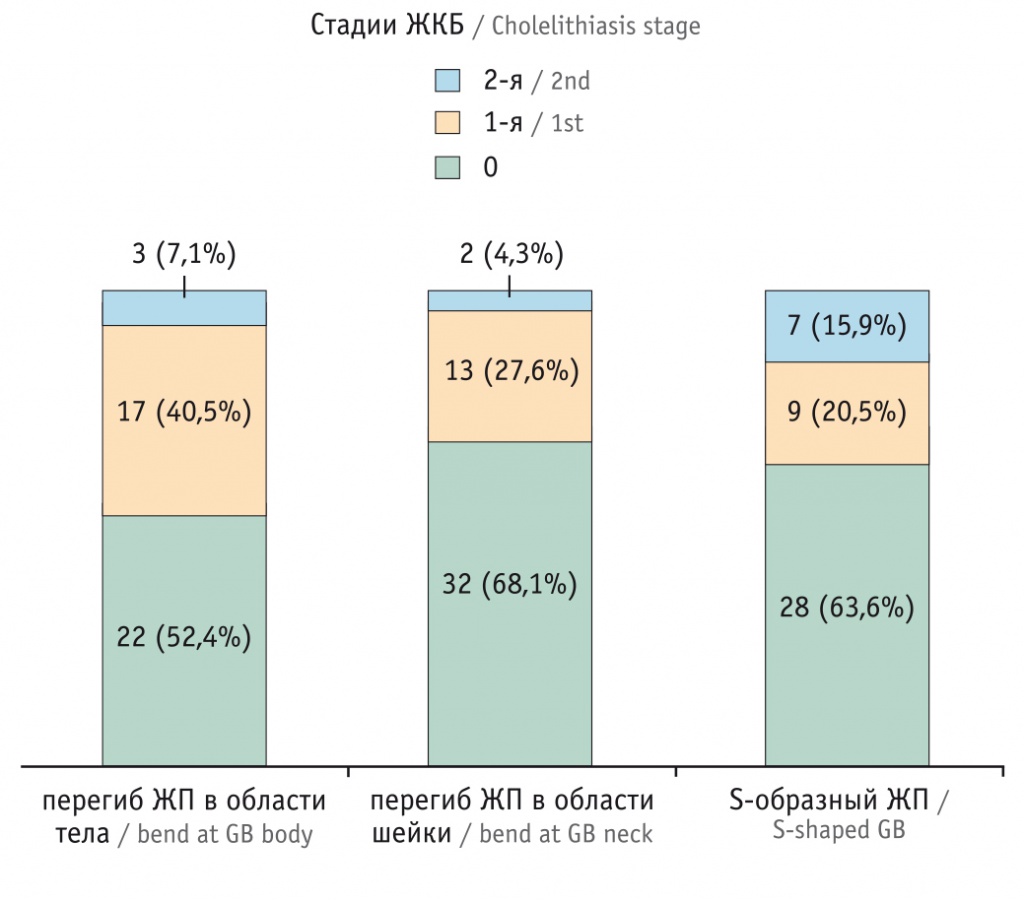
Для оценки влияния аномалий ЖП на реологию желчи изучалась их взаимосвязь со стадией ЖКБ. По результатам наблюдения у 51 пациента выявлена ЖКБ. Итак, среди участников с перегибом в области тела, сопровождающимся пониженной сократительной функцией, по данным УЗИ, нарушение реологии желчи в виде билиарного сладжа визуализируется у 17 (40,5%), в виде конкрементов — у 3 (7,1%). При перегибе в области шейки билиарный сладж и конкременты наблюдали у 13 (27,6%) и у 2 (4,3%) человек соответственно. Среди лиц с S-образным перегибом ЖП отмечено увеличение доли пациентов с конкрементами ЖП — 7 (15,9%), билиарный сладж был у 9 (20,5%) больных.
Наличие нарушения реологии желчи по типу билиарного сладжа и конкрементов в ЖП, согласно классификации, разработанной в Центральном научно-исследовательском институте гастроэнтерологии (г. Москва) и рекомендованой ІІІ съездом Научного общества гастроэнтерологов России (2003) [16], соответствует ЖКБ 1-й и 2-й стадии. Обращает на себя внимание, что наибольшая доля больных с ЖКБ 2-й стадии отмечена при S-образном перегибе ЖП (рис. 5).
Рис. 5. Взаимосвязь аномалий желчного пузыря (ЖП) и стадии желчнокаменной болезни (ЖКБ)
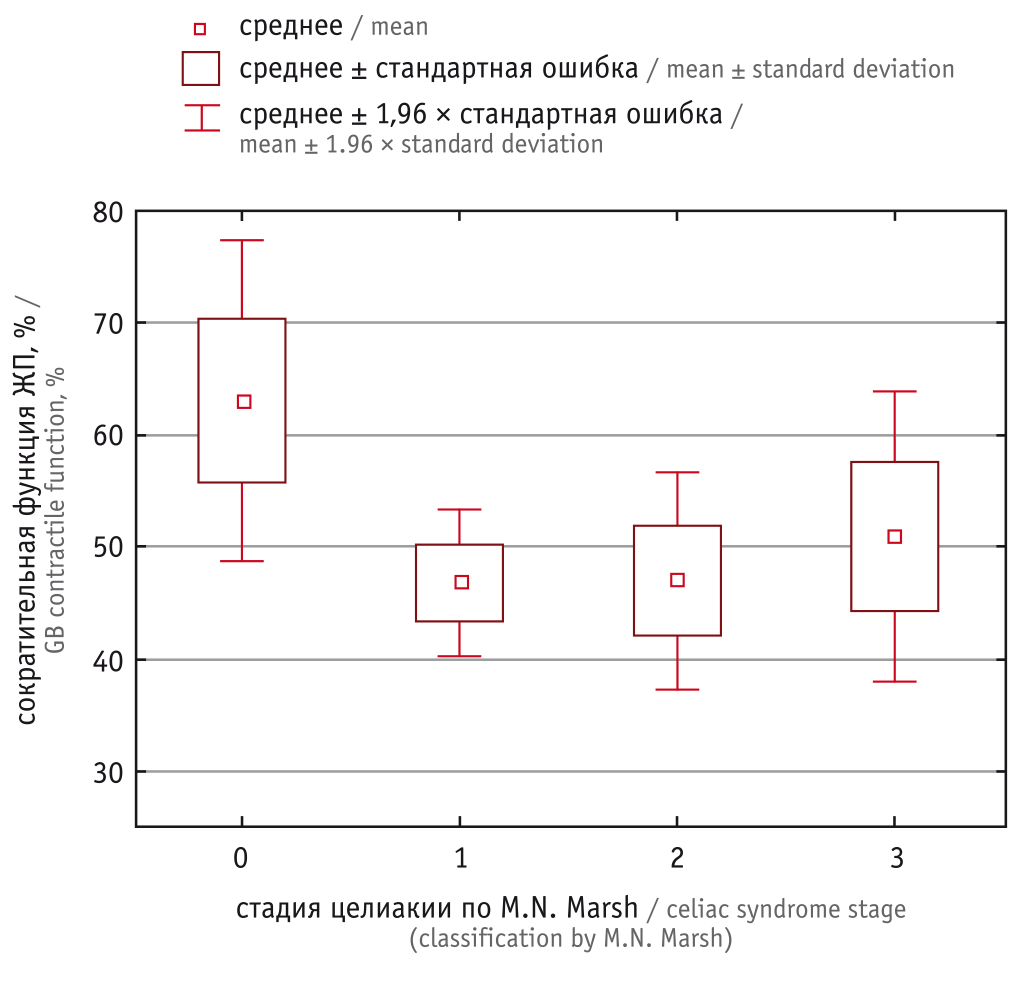
С целью уточнения влияния патоморфологической картины слизистой оболочки ДПК на функцию ЖП проводилась сравнительная оценка сократительной функции ЖП при различных стадиях по M.N. Marsh. Оказалось, что у больных целиакией по мере нарастания выраженности атрофических изменений слизистой оболочки ДПК снижается функция ЖП. Так, у пациентов со стадиями 1–3 по M.N. Marsh сократительная функция была ниже в 1,2–1,3 раза, чем у участников со стадией 0. Однако между пациентами со стадиями 1, 2 и 3 различий по сократительной функции ЖП не было (рис. 6).
Рис. 6. Показатели сократительной функции желчного пузыря (ЖП) при различных морфологических стадиях целиакии
ОБСУЖДЕНИЕ
В результате исследования установлено, что у больных целиакией наблюдается высокая частота сочетанной гастроэнтерологической патологии и заболеваний желчевыводящих путей, что определяет их общие патогенетические механизмы и, как следствие, формирование коморбидности. При целиакии как генетически детерминированном заболевании причина первичной билиарной дисфункции — врожденные аномалии ЖП, являющиеся висцеральным признаком дисплазии соединительной ткани, отражающим наследственные нарушения соединительной ткани с мультифакториальной природой, согласно Национальным российским рекомендациям по диагностике и лечению наследственных нарушений соединительной ткани (2012) [17].
Описанные анатомо-физиологические особенности пищеварительной системы, воспалительно-дистрофические изменения слизистой оболочки ДПК приводят к воспалению слизистой оболочки БДС и, как следствие, к нарушению функции СО, пассажа желчи и ее реологии. Кроме того, структурная перестройка слизистой оболочки ДПК в виде атрофических процессов оказывает негативное влияние на сократительную функцию ЖП, являясь фактором риска развития билиарной дисфункции.
Таким образом, связь синдрома билиарной дисфункции и целиакии — это установленный факт. В данной работе впервые уточнена значимость аномалий ЖП в развитии билиарной патологии. К факторам, влияющим на формирование синдрома билиарной диспепсии у больных целиакией, относятся выраженность хронического воспаления, стадия атрофических изменений слизистой оболочки ДПК и БДС.
ЗАКЛЮЧЕНИЕ
Проведенный анализ показал, что у пациентов с целиакией коморбидность сопряжена с синдромом билиарной дисфункции. Маркеры билиарной дисфункции — врожденные аномалии анатомического строения желчного пузыря, которые определяются его деформацией и дисхолией; выраженной степенью активности хронического воспаления слизистой оболочки двенадцатиперстной кишки (ДПК) и большого дуоденального сосочка; 3-й стадией, по M.N. Marsh, атрофических изменений слизистой оболочки ДПК.
Поступила: 26.03.2020
Принята к публикации: 20.04.2020








