ВВЕДЕНИЕ
Лучевые повреждения органов малого таза (постлучевой ректит, цистит, уретрит, грубые рубцовые деформации вульвы и промежности) — наиболее частые осложнения после лучевой терапии на органах малого таза у женщин. По данным различных авторов, частота поздних осложнений после лучевой терапии на органах малого таза составляет до 30%[1, 2]. Таким образом, треть пациенток, излеченных от злокачественного новообразования, приобретают новое заболевание, существенно снижающее качество жизни и требующее длительного лечения.
При лучевой терапии злокачественных новообразований органов малого таза у женщин в зону полей облучения могут попадать различные анатомические образования — мочевой пузырь, прямая кишка, внутритазовая клетчатка, кости таза и сосудисто-нервные пучки, вульва. Необходимо отметить, что изолированные поражения одного органа встречаются редко, в большинстве случаев они имеют сочетанный характер. Сложности дозиметрического планирования вызваны близким расположением органов в малом тазу, также существует индивидуальная чувствительность тканей к лучевой терапии[3, 4].
Осложнения после лучевой терапии на органах малого таза классифицируют на ранние и поздние. Острые токсические эффекты возникают в течение нескольких недель и продолжаются до 3 месяцев после лечения, они носят функциональный характер и часто бывают обратимыми. Поздние лучевые осложнения формируются не ранее чем через 3 месяца после окончания лечения и, как правило, бывают хроническими[1, 3, 4].
Хронические осложнения включают стенозы влагалища и уретры, стриктуры толстой кишки, образование свищей, постлучевые циститы, ректиты и недержание мочи. Распространенность нежелательных явлений в последние годы снизилась благодаря широкому использованию техник прицельного облучения[5, 6].
По данным ряда авторов, частота геморрагического цистита, индуцированного лучевой терапией, составляет от 5,7% до 11,5%, он может появляться в период от 2 месяцев до 10 лет после облучения[7, 8]. В основе радиационного повреждения тканей лежит цитотоксичность, вызывающая сублетальные клеточные повреждения, прогрессирующий облитерирующий эндартериит, ишемию тканей, потерю коллагена и фиброз. Гиповаскуляризация вызывает гипоксию тканей. В таких условиях поврежденные фибробласты не в состоянии вырабатывать коллаген.
При биопсии мочевого пузыря после облучения можно увидеть выраженный отек слизистой оболочки, сосудистые звездочки, петехиальные кровоизлияния в слизистой оболочке, облитерирующий эндартериит и фиброз гладкой мускулатуры[9–11].
К традиционным методам лечения относят внутрисосудистое введение нитратов и простагландина, местное применение формалина и растворов серебра, системное использование стероидов и аминокапроновой кислоты, антибиотиков, а также прижигание кровоточащих сосудов. В крайних случаях производят двустороннюю подчревную перевязку артерий[11].
Лучевая терапия может также изменять регенеративные способности тканей, так что повреждения, как правило, не заживают. Именно в таких случаях назначают иммунотерапию. Это относительно новое направление. Иммунотерапия при раке помогает организму справиться с заболеванием за счет активизации защитных ресурсов и не допустить развития повторных опухолей и метастазов. В онкологии используют интерфероны, вакцины от рака, интерлейкины, колониестимулирующие факторы и другие иммунные препараты[11].
Основные направления иммунотерапии:
- подавление роста опухолевых клеток и их последующее уничтожение;
- профилактика рецидива опухоли и образования метастазов;
- уменьшение побочного влияния противоопухолевых средств, лучевой терапии;
- профилактика инфекционных осложнений при лечении опухолей.
Цель данной статьи: оценить эффективность комплексного подхода к лечению постлучевых поражений органов малого таза у женщин.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
В статье описан клинический случай лечения пациентки с постлучевыми поражениями органов малого таза, проведенного на базе отделения эстетической гинекологии и реабилитации ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России в 2020 году.
В июне 2020 года пациентка Н., 65 лет, обратилась в отделение эстетической гинекологии и реабилитации с жалобами на постоянное недержание мочи, зуд, сухость и болезненность в области вульвы и влагалища, беспокоящие ее в течение 7 лет.
Из анамнеза. В январе 2012 года по месту жительства у больной проведена гистероскопия с раздельным диагностическим выскабливанием полости матки и цервикального канала по поводу аномальных маточных кровотечений. В ходе гистологического исследования обнаружена умеренно дифференцированная аденокарцинома эндометрия.
В феврале 2012 года выполнено оперативное лечение в онкологическом стационаре по месту жительства: лапаротомия, экстирпация матки с придатками. При гистологическом исследовании операционного материала диагноз был подтвержден: умеренно дифференцированная аденокарцинома эндометрия с инвазией в миометрий до 1,0 см и в слизистую внутреннего зева и цервикального канала Т1аN0M0.
В апреле 2012 года пациентка прошла курс дистанционной лучевой терапии (суммарная очаговая доза — 45 Гр на область таза). В январе 2014 года при ежегодном обследовании обнаружен метастаз дистального отдела уретры. Было проведено иссечение дистального отдела уретры по поводу новообразования. При гистологическом исследовании данное образование определено как метастаз основной опухоли в дистальный отдел уретры.
Далее пациентка получила 4 курса полихимиотерапии (доксорубицин 80 мг в/в, цисплатин 135 мг в/в). После иссечения дистального отдела уретры у пациентки появились жалобы на постоянную потерю мочи.
В конце 2018 года при плановом обследовании у больной найдено новообразование правой большой половой губы, проведена биопсия. По данным гистологического исследования биоптата, эпидермальный эпителий утолщен с акантозом без атипии, в подлежащей ткани умеренно выраженная, преимущественно лимфоидная инфильтрация.
Пациентка до настоящего времени находится на диспансерном наблюдении у онколога по месту жительства, отмечается ремиссия основного заболевания в течение 7 лет.
При гинекологическом осмотре обращает на себя внимание выраженный амонийный запах кожных покровов, вульварное кольцо зияет и рубцово деформировано, на больших половых губах имеются следы расчесов, кожа и слизистая с множественными изъязвлениями и трофическими язвами. При пальпации кожа половых губ плотная, умеренно болезненная. Вход во влагалище затруднен из-за выраженных рубцовых изменений после лучевой терапии, видимая слизистая влагалища покрыта плотным желтоватым налетом. Наружное отверстие уретры идентифицировано с трудом (рис. 1), стенозировано, с выраженным желтоватым налетом. Отмечается постоянное подтекание мочи небольшими порциями. Тело матки, шейка и придатки оперативно удалены (рис. 2).
Рис. 1. Наружное отверстие уретры пациентки Н. Здесь и далее в статье иллюстрации авторов
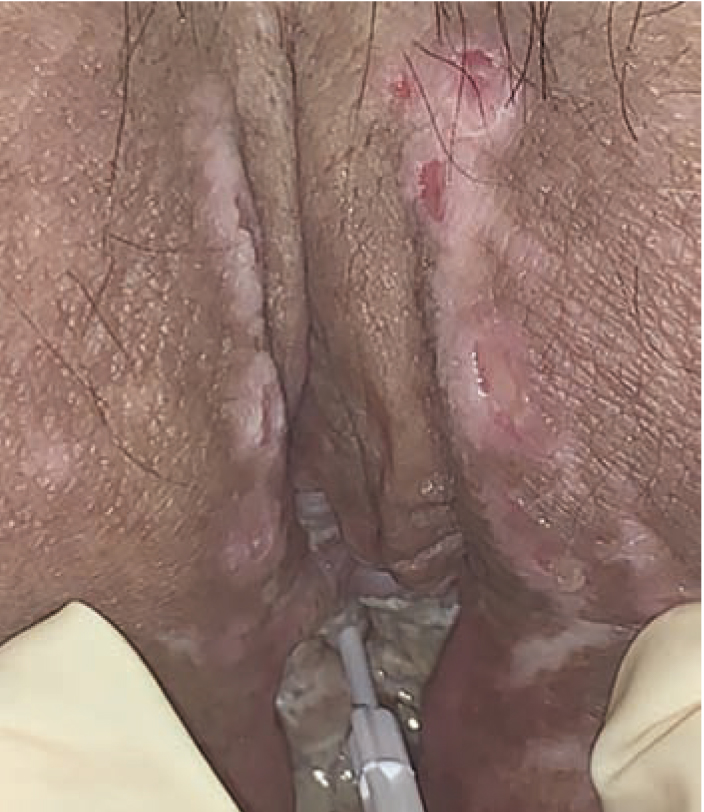
Рис. 2. Вид наружных половых органов и преддверия влагалища пациентки Н. после лучевой терапии
Проведено стандартное клинико-лабораторное обследование, отклонения не выявлены.
Установлен диагноз: Cr. сorp uteri Т1аN0M0 G 2. Состояние после хирургического лечения и курса дистанционной γ-терапии 2. Постлучевой стеноз влагалища. Стриктура уретры. Постлучевой цистит, ректит. Недержание мочи. Аммонийный дерматит.
Лечение пациентки осуществлялось поэтапно с учетом интегрального подхода и наличия мультиорганной патологии.
На первом этапе (июнь 2020 года) проводили терапию, направленную на устранение основных жалоб и улучшение состояния кожи вульвы, а также лечение цистита и нарушения мочеиспускания, включающее в себя:
- физиотерапию — низкочастотную ультразвуковую кавитацию на аппарате «Фотек» с чередованием растворов бензидамина и метронидазола по 100 мл № 7 с целью санации преддверия влагалища и вульвы; лазеротерапию на аппарате «Матрикс-Уролог» (внеполостная методика) № 7;
- внутрипузырные инстилляции гиалуроната натрия по 50 мл 2 раза в неделю № 4, затем 1 раз в неделю до № 15.
Данная терапия направлена на восстановление поврежденного гликозаминогликанового слоя уротелия и устранение симптомов ургентности, сопровождающих постлучевой цистит.
Из-за отсутствия дистального отдела уретры и нарушения функции внутреннего сфинктера мочевого пузыря, вследствие чего и происходит постоянное подтекание мочи, после выполнения инстилляции пациентка находилась в горизонтальном положении с катетером в уретре 30–40 мин для профилактики вытекания лечебного раствора из мочевого пузыря.
Проведен курс иммунотерапии с помощью рекомбинантного ИФН-γ Ингарона в виде подкожных инъекций по 100 000 МЕ в область вульвы через день № 5. Наблюдался выраженный положительный эффект. Уже после одной инъекции пациентка отметила почти полное заживление трофических язв, уменьшение зуда.
Ингарон — рекомбинантный ИФН-γ человека — состоит из 144 аминокислотных остатков, лишен первых трех из них (Cys-Tyr-Cys), замененных на Met. Молекулярная масса — 16,9 кДа. Получен микробиологическим синтезом в рекомбинантном штамме Escherichia coli и очищен колоночной хроматографией. Удельная противовирусная активность на клетках (фибробласты человека), инфицированных вирусом везикулярного стоматита, составляет 2 × 107 ЕД на 1 мг белка[9, 10].
ИФН-γ (иммунный ИФН) — важнейший провоспалительный цитокин, продуцентами которого в организме человека являются естественные киллерные клетки (NK-клетки), CD4 Th-клетки и CD8 цитотоксические супрессорные клетки. Противоопухолевое действие ИФН-γ связано также с его способностью активировать NK-клетки, цитотоксические Т-лимфоциты и макрофаги. По-видимому, противоопухолевое действие ИФН-γ обусловлено комбинацией его иммуномодулирующей активности, прямого антипролиферативного действия на опухолевые клетки и подавления ангиогенеза.
Интерфероны — это медиаторы иммунитета, специалисты выделяют их в особую систему нуклеинового гомеостаза, т. е. систему, защищающую генетическую информацию человека от неблагоприятных воздействий окружающей среды, таких как вирусные и микробные агенты, разнообразные мутагены и токсические вещества. Эта система глубоко интегрирована в основные системы организма, прежде всего иммунную, где все типы интерферонов играют важную роль. Интерфероны регулируют развитие адекватного иммунного ответа; в частности, ИФН-γ играет ключевую роль в формировании клеточной защиты. В некоторых работах продемонстрированы пилотные данные по повышению эффективности терапии постлучевых циститов с применением ИФН-γ (препарата Ингарон)[7, 11].
Больной Н. было назначено также применять аппликационные гидрогелевые салфетки с альгинатом натрия, диоксидином и лидокаином на область вульвы ежедневно 2 раза в день в течение 10 дней, затем в домашних условиях — материал гидрогелевый с Деринатом ежедневного локально на область вульвы до 1 месяца в качестве местного противовоспалительного и стимулирующего средства для лечения длительно не заживающих ран и трофических язв, в том числе лучевых реакций со стороны слизистых оболочек, и снятия болевых ощущений.
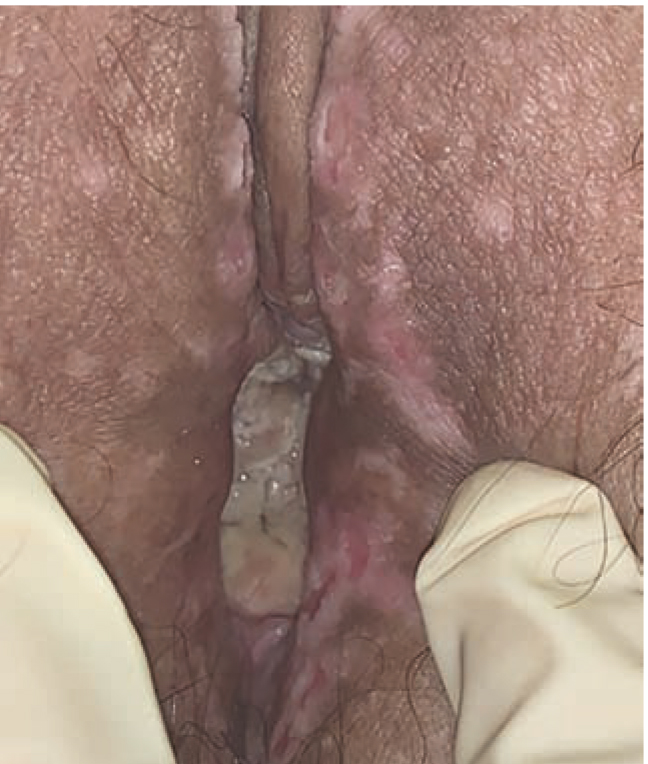
На втором этапе в июне–августе 2020 года произведено воздействие фракционным микроаблативным СО2 лазером (SMARTXIDE2 V2LR, MonaLisa Touch, DEKA, Florence, Italy) на область вульвы в режиме Power 30 W/ Dwell time 1000 μs/ Spasing 1000 μm/ 1 № 3 с интервалом 4 недели с целью негормональной коррекции симптомов генитоуринарного менопаузального синдрома (ГУМС). При осмотре в динамике отмечалось улучшение внешнего состояния кожи промежности, уменьшение зуда, мацерации (рис. 3).
Рис. 3. Динамика состояния пациентки Н. на фоне лечения (август и сентябрь 2020 г.)

В систематическом обзоре 2019 года 48 исследований по применению лазерного воздействия у женщин с ГУМС, перенесших рак молочной железы, продемонстрирована эффективность в 83,5% случаев при отсутствии каких-либо побочных эффектов. Тем не менее отдаленные результаты ни в одной работе не оценивались, требуется проведение хорошо спланированных рандомизированных контролируемых исследований[8].
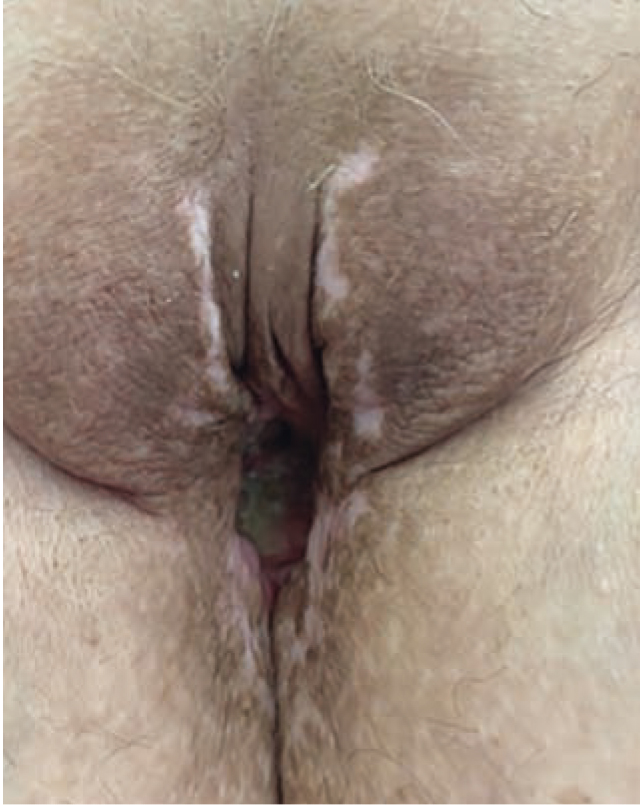
По результатам динамического наблюдения пациентки в декабре 2020 г. (рис. 4) жалобы на зуд и боли в области вульвы значительно уменьшились, носят эпизодический характер. Сохраняется постоянное недержание мочи. При осмотре вульварное кольцо зияет, кожа больших половых губ уплотнена, безболезненна, на месте язвенных поражений кожи депигментированные участки после заживления вторичным натяжением. Вход во влагалище затруднен из-за выраженных рубцовых изменений. Видимая слизистая влагалища без признаков воспаления.
Рис. 4. Состояние пациентки Н. в декабре 2020 г.
Проводится дальнейшее динамическое наблюдение пациентки с плановыми визитами для повторных физиотерапевтических и медикаментозных воздействий.
ЗАКЛЮЧЕНИЕ
Консервативная терапия постлучевых осложнений органов малого таза позволяет улучшить качество жизни пациенток, особенно если она начата в раннем послеоперационном периоде и сразу после лучевой терапии. Эффективность лечебных мероприятий при поздних лучевых повреждениях зависит от сроков поступления женщины в специализированное учреждение, степени тяжести патологического процесса, возраста и наличия сопутствующих хронических заболеваний. Наиболее эффективно комплексное лечение — местное и медикаментозное воздействие в сочетании с методами аппаратной физиотерапии.
Особое место занимает иммунотерапия с помощью подкожного введения ИФН-γ (Ингарона), так как в условиях сниженного иммунологического контроля затрудняется элиминация внутриклеточно расположенного возбудителя и создаются предпосылки для формирования хронической, рецидивирующей инфекции (цистит, дерматит у данной пациентки). Иммунотерапия эффективна не только для профилактики, но и для лечения постлучевых циститов и дерматитов, как показано в нашем клиническом наблюдении.
Оправдано также применение углекислотного фракционного микроаблативного лазерного воздействия на область вульвы и культи влагалища с целью стимуляции процессов неоколлагенеза и улучшения эластичности и трофики тканей в этой области[8].
Поступила: 06.04.2021
Принята к публикации: 17.06.2021








