Среди поражений половой системы женщины эндометриоидные кисты яичников (ЭКЯ) занимают второе место по частоте встречаемости[1, 9]. Эндометриоз яичников нередко приводит к нарушению репродуктивной функции[3, 10, 12]. Даже после адекватного двухэтапного хирургического и гормонального лечения часто наблюдаются рецидивы заболевания[1, 6, 13]. Таким образом, в настоящее время проблема ЭКЯ остается актуальной.
Несмотря на большое количество исследований, посвященных различным аспектам патогенеза и терапии эндометриоза, до сих пор до конца не выяснены многие механизмы, лежащие в основе его возникновения и прогрессирования[4, 13, 16].
В последние годы большое внимание уделяется проблеме недифференцированной дисплазии соединительной ткани (НДСТ), что связано с высокой распространенностью ее в популяции. По данным разных авторов, частота встречаемости НДСТ колеблется от 20% до 80%[7, 11].
НДСТ — генетически детерминированное нарушение развития соединительной ткани, приводящее к изменению ее структуры и функций и реализующееся в клиническом многообразии фенотипических признаков и органных проявлений. Она приводит к нарушению иммунитета, способствует прогрессированию патологических изменений внутренних органов. Результаты многочисленных исследований последних лет подтверждают значимость НДСТ и в развитии гинекологических заболеваний[2, 5, 7, 18].
В настоящее время имеются работы, свидетельствующие о важной роли факторов сосудистого роста, матриксных металлопротеиназ (ММР-2 и ММР-9), молекул адгезии в формировании генитального эндометриоза[4, 8, 14–17, 19]. Однако в доступной литературе нами не найдена информация о клинической значимости сопутствующей НДСТ и изменениях уровней факторов сосудистого роста, ММР, молекул адгезии у пациенток с ЭКЯ.
Цель исследования: определение роли НДСТ в прогрессировании ЭКЯ; расширение представлений о патогенезе ЭКЯ с определением уровней васкулоэндотелиального фактора роста А (VEGF-А), его растворимого рецептора 1 (sVEGF-R1), MMP-2 и MMP-9, тканевого ингибитора металлопротеиназы 2 (TIMP-2), растворимых межклеточных (sICAM-1) и внутрисосудистых (sVCAM-1) молекул адгезии.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включили 100 женщин, госпитализированных в гинекологическое отделение ГБУЗ «Ставропольский краевой клинический перинатальный центр» в 2008–2012 гг. Основную группу составили 35 пациенток с ЭКЯ, у которых было выявлено шесть и более фенотипических признаков НДСТ, группу сравнения — 35 женщин с ЭКЯ и с пятью и менее признаками НДСТ (согласно международной фенотипической шкале M. J. Glesby признаки в количестве менее шести не являются основой для диагноза НДСТ). В контрольную группу вошли 30 здоровых женщин репродуктивного возраста без ЭКЯ и НДСТ, поступивших для выполнения хирургической стерилизации.
В перитонеальной жидкости (ПЖ) всех участниц определяли уровни VEGF-A, sVEGF-R1, sICAM-1, sVCAM-1, MMP-2, MMP-9 и TIMP-2. Для исследования внешнего фенотипа применяли модифицированную фенотипическую карту с 63 показателями. Оценку степени тяжести НДСТ осуществляли по международной фенотипической шкале M. J. Glesby. Женщинам всех групп проведены клиниколабораторное и инструментальное обследования, лечебно-диагностическая лапароскопия. Диагноз ЭКЯ подтвержден гистологически.
Концентрацию VEGF-A в ПЖ измеряли методом твердофазного ИФА с использованием наборов Bioscience (США — Австрия), уровни sVEGF-R1, sICAM-1, sVCAM-1 и MMP-9 — с применением наборов Bender MedSystems (Австрия), содержание MMP-2 и TIMP-2 — с помощью наборов R&D Systems (США) согласно прилагаемым к ним методикам.
Статистическую обработку полученных данных проводили с использованием программы Statistica 10.0 (StatSoft, США), серийный номер — AXAR306F596204FA-J. В соответствии с целями и задачами исследования, а также с учетом специфики анализируемых переменных выполняли: расчет элементарных показателей — средних значений (M), ошибки средних (m), долей (%), стандартной ошибки долей (N); сравнение количественных данных с использованием непараметрического критерия Манна — Уитни. Различия считали статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При определении содержания фактора сосудистого роста и его рецептора в ПЖ установлено, что у пациенток группы сравнения уровень VEGF-A значимо не отличался от такового у здоровых женщин, а показатель sVEGF-R1 был выше, чем в контроле (р = 0,001) (табл. 1). У участниц основной группы наблюдали значимое увеличение концентрации sVEGF-R1 относительно ее значений у пациенток группы сравнения и здоровых женщин (см. табл. 1). Эти данные согласуются с результатами аналогичных исследований[15].
Таблица 1
Уровни васкулоэндотелиального фактора роста А и его растворимого рецептора 1 в перитонеальной жидкости обследованных женщин (M ± m), пкг/мл

Примечание. В таблицах 1–3: группа контроля — здоровые женщины репродуктивного возраста без эндометриоидных кист яичников (ЭКЯ) и недифференцированной дисплазии соединительной ткани (НДСТ); основная группа — пациентки с ЭКЯ и с шестью и более признаками НДСТ; группа сравнения — женщины с ЭКЯ и с пятью и менее признаками НДСТ.
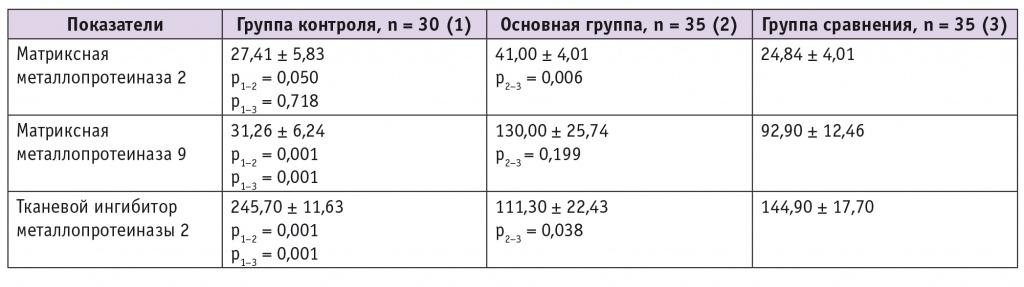
В ПЖ при ЭКЯ, независимо от наличия НДСТ, имели место значительное повышение содержания ММР-9 и снижение уровня TIMP-2 (р = 0,001). У пациенток группы сравнения содержание ММР-2 значимо не отличалось от такового у здоровых женщин. У женщин основной группы концентрация ММР-2 была существенно выше, а TIMP-2 — ниже, чем у участниц групп сравнения и контроля (р < 0,05) (табл. 2). Таким образом, результаты не противоречат данным аналогичных исследований[17].
Таблица 2
Уровни матриксных металлопротеиназ 2 и 9 и тканевого ингибитора металлопротеиназы 2 в перитонеальной жидкости обследованных женщин (M ± m), пкг/мл
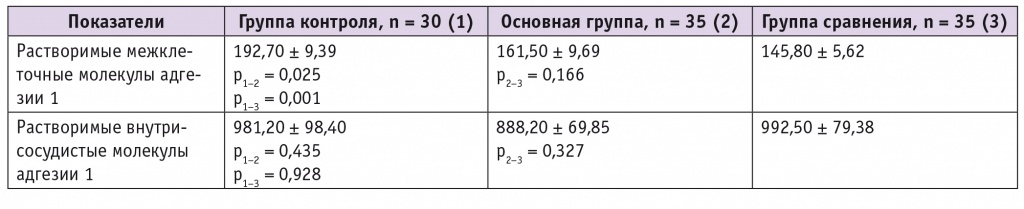
Согласно полученным данным, в ПЖ женщин с ЭКЯ, вне зависимости от наличия НДСТ, уровень sICAM-1 был достоверно ниже, чем у здоровых женщин, тогда как значимых различий между группами по содержанию sVCAM-1 не выявлено (табл. 3).
Таблица 3
Уровни растворимых молекул адгезии в перитонеальной жидкости обследованных женщин (M ± m), пкг/мл
Подтверждением повышенной проангиогенной активности ПЖ у женщин с ЭКЯ и НДСТ является выявленное увеличение по сравнению с показателями участниц групп сравнения и контроля уровней sVEGF-R1 (в 2,4 и в 5,1 раза соответственно, в обоих случаях р = 0,001) и VEGF-A (в 1,2 (p > 0,05) и 1,8 раза (p < 0,05) соответственно).
У пациенток с ЭКЯ наблюдается возрастание активности ММР-9 в ПЖ, особенно выраженное при НДСТ: ее концентрация в основной группе превышала показатели в группах сравнения и контроля в 1,4 и 4,2 раза соответственно. Содержание MMP-2 в ПЖ участниц основной группы было в 1,6 раза выше, чем у пациенток группы сравнения, и в 1,5 раза выше, чем у здоровых женщин. Обращает на себя внимание статистически значимое уменьшение содержания TIMP-2 в ПЖ при ЭКЯ, что следует рассматривать как одно из условий инвазии эндометриоидных гетеротопий. При этом при НДСТ уровень TIMP-2 в ПЖ был в 1,3 раза ниже, чем в группе сравнения (p < 0,05). В то же время концентрация sICAM-1, участвующих в реализации процессов апоптоза, в ПЖ пациенток с ЭКЯ была значимо снижена по сравнению с таковой у здоровых женщин. Таким образом, рост уровней ММР, принимающих участие в разрушении межклеточного матрикса, при одновременном снижении апоптоза в ПЖ и активации ангиогенеза может быть причиной большей инвазивности клеток эктопического эндометрия при НДСТ.
ЗАКЛЮЧЕНИЕ
Резюмируя представленные данные, можно утверждать, что у пациенток с эндометриоидными кистами яичников (ЭКЯ) сопутствующая недифференцированная дисплазия соединительной ткани (НДСТ) должна рассматриваться как фактор риска более агрессивного течения заболевания, что подтверждается значимым увеличением у таких пациенток уровней матриксных металлопротеиназ 9 и 2, разрушающих внеклеточный матрикс, при одновременном снижении содержания тканевого ингибитора металлопротеиназы 2, создающем условия для инвазии эндометриоидных гетеротопий. Вместе с тем повышение уровня усиливающего ангиогенез растворимого рецептора 1 васкулоэндотелиального фактора роста А свидетельствует о прогрессирующем течении заболевания.
Практические рекомендации:
- необходимо выявлять признаки НДСТ у всех пациенток с ЭКЯ как дополнительный критерий активности эндометриоидного процесса;
- при их наличии патогенетически обоснованным является назначение в качестве длительной противорецидивной терапии препаратов с антиангиогенными свойствами (диеногест).
Углубленное изучение особенностей патогенеза различных форм эндометриоза у пациенток с сопутствующей НДСТ, возможно, позволит разработать качественно новые, патогенетически обоснованные алгоритмы ведения этой когорты больных.








