В докладе ВОЗ 2014 г. о глобальном эпидемиологическом надзоре за устойчивостью к антибиотикам [30] говорится, что резистентность микроорганизмов к антибиотикам является не предсказанием будущего, она наблюдается уже сейчас во всем мире и ставит под угрозу возможность лечения распространенных инфекций. Без принятия срочных скоординированных мер в мире наступит «постантибиотиковая эра», когда общие инфекции и мелкие травмы, которые поддавались лечению в течение десятилетий, снова будут убивать [29].
В связи с публикацией этих материалов эксперты ВОЗ дают приведенные ниже пояснения.
Что такое устойчивость к противомикробным препаратам?Антимикробная резистентность — это устойчивость микроорганизма к препарату, который изначально был эффективен для лечения инфекций, вызванных им.
Устойчивые микроорганизмы (включая бактерии, грибки, вирусы или паразитов) способны противостоять действию препаратов таких групп, как антибактериальные (антибиотики), противогрибковые, противовирусные и противомалярийные. Стандартные виды лечения становятся неэффективными, а инфекции сохраняются, увеличивается риск их распространения.
Установленная резистентность микроорганизмов к антимикробным препаратам во всем мире:
-
инфекции, вызванные гонококком, — к цефалоспоринам третьего поколения; в результате увеличилась распространенность ассоциированных с ним заболеваний и осложнений (бесплодия, неблагоприятных исходов беременности и младенческой слепоты);
-
инфекции мочевыводящих путей, обусловленные Escherichia coli, — к фторхинолонам;
-
тяжелые госпитальные инфекции, вызванные стафилоккоками, — к препаратам первого ряда;
-
угрожающие жизни инфекционные заболевания, вызванные кишечными бактериями, — к карбапенемам (класс β-лактамных антибиотиков с широким спектром действия);
-
туберкулез — широкая лекарственная устойчивость и резистентность к любым фторхинолонам и инъекционным препаратам второй линии;
-
малярия, вызванная Plasmodium falciparum, угрожает глобальным усилиям по уменьшению бремени данного заболевания, так как указанный микроорганизм проявляет устойчивость ко многим противомалярийным препаратам (хлорохинину, артеметер-люмефантрину, дигидроартемизину и др.);
-
ВИЧ — к препаратам антиретровирусной терапии из схем первой и второй линии;
-
грипп — вирусы гриппа А проявляют устойчивость к препаратам, часто используемым для профилактики заболевания (амантадину и ремантадину).
Следующие микроорганизмы также проявили резистентность:
-
Klebsiella pneumoniae — к цефалоспоринам третьего поколения и карбапенемам;
-
Staphylococcus aureus — к метициллину;
-
Streptococcus pneumoniae — к пенициллину;
-
Nontyphoidal Salmonella — к фторхинолонам (ципрофлоксацину);
-
Shigella species — к фторхинолонам;
-
Candida species (и другие non-albicans) — к противогрибковым препаратам (флуконазолу).
Почему устойчивость к противомикробным препаратам является глобальной проблемой?
Новые механизмы устойчивости возникают и распространяются глобально и угрожают нашим возможностям лечения часто встречающихся инфекционных заболеваний, приводящих к смерти и инвалидности людей, которые до недавнего времени могли продолжать жить нормальной жизнью.
Без эффективной противоинфекционной терапии многие стандартные медицинские вмешательства могут оказаться неэффективными или превратиться в очень рискованные процедуры.
Инфекции, вызываемые устойчивыми микроорганизмами, часто не поддаются стандартному лечению, что приводит к затяжной болезни, более высоким расходам на здравоохранение и более высокому риску смерти.
Что ускоряет появление и распространение устойчивости к противомикробным препаратам?
Развитие антимикробной резистентности является естественным явлением. Однако определенные действия человека ускоряют ее возникновение и распространение. К ним относятся:
-
ненадлежащее использование противомикробных препаратов (бесконтрольный прием антибиотиков в популяции);
-
применение антимикробных средств в животноводстве, что способствует возникновению и селекции резистентных штаммов и передаче их человеку;
-
недостаточные меры по профилактике инфекций и инфекционному контролю в клинической практике.
Глобальный план действий по борьбе с антимикробной резистентностью
ВОЗ разработала проект глобального плана борьбы с антимикробной резистентностью [31], который был представлен и принят на 68-й сессии Всемирной ассамблеи здравоохранения, состоявшейся в мае 2015 г. По мнению экспертов ВОЗ, следует принять немедленные меры по борьбе с устойчивостью к противомикробным препаратам.
Для достижения этой цели глобальный план действий устанавливает пять стратегических задач:
-
повышение осведомленности об устойчивости к противомикробным препаратам и понимания этого явления;
-
укрепление знаний посредством наблюдений и клинических исследований;
-
принятие мер, направленных на уменьшение частоты инфицирования;
-
оптимизация использования противомикробных препаратов;
-
увеличение инвестиций в разработку новых лекарств, диагностических инструментов, вакцин и в другие мероприятия.
Разработка этого плана была основана на многочисленных консультациях экспертов во время проведения различных глобальных и региональных форумов.
Эксперты ВОЗ особо отмечают, что в борьбе с угрозой антибиотикорезистентности главным является снижение риска передачи резистентных организмов — дома, в населенных пунктах, медицинских учреждениях, пищевых учреждениях, в водоснабжении, сельском хозяйстве. Ключевой элемент — усиление мер по обеспечению гигиены.
За пациентов, обращающихся за медицинской помощью, медики несут особую ответственность во избежание заражения инфекциями в результате диагностических и лечебных мероприятий. Внутрибольничные инфекции являются одной из основных причин смерти и страдания госпитализированных больных по всему миру, поэтому их профилактика по праву считается краеугольным камнем безопасности пациентов.
Основные принципы:
-
стандартные меры предосторожности (гигиена рук, стерилизация и дезинфекция медицинских материалов, профилактика травм от острых инструментов);
-
раннее выявление инфекционного заболевания и меры по изоляции пациента, использование средств индивидуальной защиты;
-
осуществление инвазивных вмешательств с соблюдением асептики;
-
надлежащее обращение с отходами и их утилизация.
Роль антибиотиков в профилактике инфекционных осложнений в акушерстве и гинекологии
В материалах ВОЗ имеются рекомендации по необходимости профилактического применения антибиотиков в ситуациях, когда риск инфекционных осложнений высок.
На официальном сайте ВОЗ размещены материалы по использованию антибиотиков в профилактических целях, основанные на доказательствах, в разных областях медицины, в том числе в акушерстве и гинекологии, опубликованные Кокрановским сообществом в 2010–2015 гг. Так, рутинное профилактическое введение антибиотиков при кесаревом сечении уменьшает риск раневой инфекции, эндометрита и тяжелой инфекции на 60% и более [18, 26]. То же касается и применения антибиотиков при хирургическом аборте [14], хотя при других трансцервикальных манипуляциях доказательств оказалось не достаточно [22]. Высока эффективность антибиотикопрофилактики при тяжелых разрывах промежности [9].
Рекомендации, опубликованные ведущими мировыми профессиональными сообществами, с указанием силы доказательств и убедительности рекомендаций (табл. 1, 2) [4, 5, 7] приводятся ниже.
Таблица 1
Градация убедительности доказательств
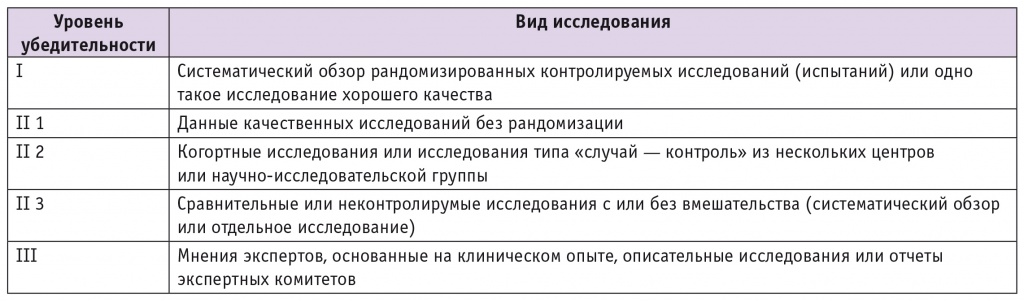
Таблица 2
Градация достоверности рекомендаций

Назначение антибиотиков с профилактической целью в гинекологии
Антибиотикопрофилактика рекомендуется:
-
всем пациенткам, подвергающимся чрезбрюшной или вагинальной гистерэктомии (I А); должен быть выбран антибиотик, применяемый в разовой дозе, из цефалоспоринов первого поколения; если у пациентки аллергия на них, то выбор должен быть сделан в пользу клиндамицина, эритромицина или метронидазола (I А); введение антибиотиков необходимо осуществлять в срок от 15 до 60 минут до разреза кожи; дополнительные дозы не рекомендуются (I А);
-
всем женщинам во время хирургического аборта (азитромицин или доксициклин в сочетании с метронидазолом) (I А);
-
женщинам с расширенными маточными трубами, обнаруженными во время гистеросальпингографии (доксициклин) (II 3B);
-
всем пациенткам при лапароскопической гистерэктомии или при лапароскопической поддержке вагинальной гистерэктомии (III B);
-
всем пациенткам, перенесшим операцию по поводу пролапса тазовых органов и/или стрессового недержания мочи (одну дозу цефалоспорина первого поколения) (III B);
-
женщинам с ожирением (ИМТ > 35 кг/м2) рекомендуется удвоить дозу вводимого антибиотика (III B);
-
если лапаротомическая операция продолжается более 3 часов или если кровопотеря составляет более 1500 мл, рекомендуется дополнительная доза антибиотика в интервале от 3 до 4 часов после введения первоначальной дозы (III С).
Антибиотикопрофилактика не рекомендуется при гистероскопических манипуляциях (II 2D).
Антибиотикопрофилактика не рекомендуется из-за отсутствия достаточных доказательных данных:
-
при введении внутриматочной спирали (ВМС) (I E), однако следует проводить скрининг на ИППП у женщин из групп населения высокого риска перед процедурой (III С);
-
после хирургического опорожнения матки при самопроизвольном аборте, в том числе при замершей беременности (I Е);
-
при проведении уродинамических исследований у женщин с низким инфекционным риском (I Е);
-
при лапароскопических операциях, которые предполагают отсутствие прямого доступа из брюшной полости в полость матки или влагалище (I Е);
-
при биопсии эндометрия (III L).
Назначение антибиотиков с профилактической целью в акушерстве
Антибитикопрофилактика рекомендуется:
-
всем женщинам, подвергающимся экстренному кесареву сечению (I А); выбор антибиотика — однократная доза цефалоспорина первого поколения; если у пациентки аллергия на пенициллин, могут быть использованы клиндамицин или эритромицин (I А); антибиотики следует ввести в срок от 15 до 60 минут до разреза кожи; дополнительные дозы не рекомендуются (I А);
-
пациенткам с травмами промежности 3-й и 4-й степени (I В);
-
женщинам с ожирением (ИМТ > 35 кг/м2) следует удвоить дозу антибиотика (III B).
-
Рекомендации, основанные на недостаточно доказательных данных:
-
если акушерская операция продолжается более 3 часов или если кровопотеря составляет более 1500 мл, рекомендуется дополнительная доза антибиотика в интервале от 3 до 4 часов после введения первоначальной дозы (III L);
-
антибиотики не следует применять исключительно для предотвращения эндокардита у пациенток при выполнении акушерских процедур любого рода (III L).
В сентябре 2015 г. экспертами ВОЗ были опубликованы рекомендации по профилактике и лечению послеродовых инфекций [28] — руководящий документ для разработки национальных клинических протоколов. Согласно данному документу, назначение антибиотиков рекомендуется:
при плановом или экстренном кесаревом сечении (за 30–60 минут до разреза кожи либо за 15–60 минут или после пережатия пуповины в условиях экстренной операции; цефалоспорины первого поколения и пенициллин являются препаратами выбора; также рекомендуется обработка влагалища повидон-йодом непосредственно перед кесаревым сечением);
-
при преждевременном разрыве плодных оболочек;
-
при ручном удалении плаценты;
-
при разрыве промежности 3–4-й степени;
-
при колонизации Streptococcus группы B для профилактики ранней неонатальнай инфекции.
Не рекомендуется рутинное профилактическое назначение антибиотиков при:
-
неосложненных вагинальных родах или оперативном влагалищном родоразрешении;
-
преждевременных родах с интактными плодными оболочками;
-
разрыве плодных оболочек, если роды происходят в срок или около срока (36 недель и более);
-
окрашенной меконием амниотической жидкости;
-
эпизиотомии;
-
во время второго или третьего триместра беременности с целью снижения инфекционной заболеваемости.
Согласно данному документу, следует постоянно обновлять национальные стандарты, учебные планы, клинические протоколы и программные материалы, которые будут содействовать поддержке и реализации новых руководящих принципов ВОЗ.
В клинических рекомендациях «Гнойно-воспалительные заболевания и сепсис в акушерстве», утвержденных Минздравом России 27 мая 2015 г. (№ 15.4/16/2-2469) [1], приведены следующие показания для антибактериальной профилактики.
-
Оперативные вмешательства:
-
кесарево сечение (всегда при экстренном, в группе высокого риска — при плановом);
-
ручное отделение плаценты и выделение последа;
-
ручное обследование полости матки;
-
поворот плода на ножку;
-
гистерэктомия;
-
использование акушерских щипцов.
-
-
Дородовое излитие околоплодных вод при недоношенной беременности (сразу после установления диагноза!) (1 А).
-
Дородовое излитие околоплодных вод при доношенной беременности при безводном промежутке более 18 часов (2 А).
-
Доказанное носительство β-гемолитического стрептококка (3 А).
-
Разрывы промежности 3-й и 4-й степени.
-
Выворот матки.
-
Разрыв матки.
-
Разрывы шейки матки II–III степени.
-
Глубокий разрыв влагалища.
Целесообразность профилактической антибиотикотерапии при аборте
Если при хирургическом прерывании беременности целесообразность профилактической антибиотикотерапии уже не обсуждается и поддерживается рекомендациями ВОЗ [17], то при медикаментозном аборте доказательств необходимости такой меры пока нет. Однако некоторые эксперты считают, что женщины из групп высокого риска ИППП, перенесшие прерывание беременности, должны получать антибиотики против хламидий, гонококков и анаэробов, чтобы уменьшить риск послеабортной инфекции [25], и это положение поддерживается экспертами Royal College of Obstetricians and Gynaecologists (уровень С) [16].
Хотя в отдельных исследованиях не было выявлено значительного сокращения инфекционной заболеваемости после операции по поводу неразвивающейся беременности или неполного аборта при профилактическом применении антибиотиков (из-за недостаточного количества исследований) [15, 24], эксперты American College of Obstetricians and Gynecologists считают достаточно значимыми рекомендации по антибиотикопрофилактике, она может уменьшить расходы на лечение послеабортных инфекционных осложнений после самопроизвольного прерывания беременности [3].
При использовании антибиотиков однократная доза является предпочтительной, учитывая недостаточную комплаентность при назначении многократного приема [15].
При консервативном (медикаментозном) завершении неполного выкидыша или неполного медицинского аборта рекомендуется, если имеются признаки инфекции, полный курс лечения антибиотиками [10].
Использование внутриматочных устройств пролонгированного обратимого действия на сегодняшний день рассматривается в качестве первой линии контрацепции для женщин, в том числе после родов и после аборта (уровень А) [13]. A. Templeton и D. A. Grimes [21] считают ВМС лучшим обратимым методом контрацепции для раннего предупреждения повторной нежелательной беременности после аборта. Исследования показывают небольшую частоту осложнений после немедленного введения ВМС после аборта, и нетто-коэффициент прекращения использования вследствие ВЗОМТ также был очень низким — в пределах от 0,0 до 0,8 на 100 женщин в год [12, 19]. На основании серии исследований, опубликованных в 2010–2012 гг., было принято решение в пользу раннего введения ВМС как при хирургическом аборте (сразу после завершения манипуляции), так и при медикаментозном (между 9-м и 14-м днем после приема мифепристона) (уровень В) [13].
Риск ВЗОМТ при введении ВМС составляет 0–2% в отсутствие цервикальной инфекции и 0–5%, если ВМС была введена на фоне недиагностированной инфекции [6]. Если женщина относится к группе риска по ИППП, то необходимо обследование с целью их раннего выявления. В случае, если такой необходимости не было и инфекцию выявили значительно позже и вне зависимости от введения ВМС, то вероятность развития ВЗОМТ низка даже без удаления ВМС, если незамедлительно будет проведено лечение [11, 32]. Рутинное профилактическое применение антибактериальных препаратов перед введением ВМС не рекомендуется [20, 23].
Рекомендации по лечению гонореи в условиях антибиотикорезистентности
Для гинекологов важно в условиях повышенной резистентности некоторых микроорганизмов к ранее эффективным препаратам внимательно следить за новыми рекомендациями по лечению заболеваний, ими вызванных.
Гонорея — одна из самых распространенных ИППП. В соответствии с пересмотренными руководящими принципами, опубликованными ВОЗ в августе 2014 г., наиболее эффективным методом лечения гонореи на сегодняшний день является комбинированная терапия: инъекционный антибиотик цефтриаксон вместе с одним из пероральных антибиотиков — либо азитромицином, либо доксициклином (в отличие от российских рекомендаций, где предлагается только один антибиотик — либо цефтриаксон, либо цефиксим или спектиномицин, причем последний — только для Уральского федерального округа) [2].
В прошлом гонококк развивал устойчивость к каждому антибиотику, который использовался для лечения гонореи, кроме цефалоспоринов, к которым относятся цефиксим и цефтриаксон. Последние лабораторные данные свидетельствуют, что цефиксим более не эффективен в лечении гонореи, и существуют опасения, что устойчивость может развиться ко всем цефалоспоринам. Ограничение использования цефиксима сейчас способно помочь сохранить цефтриаксон как средство лечения этой инфекции [8].
Меры по повышению осведомленности о проблеме устойчивости к антибиотикам
Осознание исключительной роли медицинских работников, а также руководителей здравоохранения и других лиц, принимающих решения, в сохранении здоровья общества оставляет надежду на преодоление этой глобальной современной проблемы.
Именно поэтому ВОЗ объявила о проведении Всемирной недели осведомленности и правильного использования антибиотиков 16–22 ноября 2015 г. [33]. Кампания была направлена на повышение осведомленности о глобальной устойчивости к антибиотикам и на поощрение лучших практик среди широкой общественности, представителей здравоохранения, политики и сельскохозяйственного сектора, чтобы избежать дальнейшего возникновения и распространения устойчивости к антибиотикам. Разработали специальные материалы для населения, медицинских работников, политиков и работников сельского хозяйства.
Решение о проведении столь масштабного мероприятия приняли на основании результатов опроса 9772 респондентов из 12 стран, которые ответили на 14 вопросов в режиме online или во время уличных интервью (1007 респондентов были из РФ) [27]. Более половины россиян (56%) сообщили, что принимали антибиотики в течение последних 6 месяцев (в других странах — 35–75%); столько же (56%) ответили, что курс антибиотиков был прописан им медицинским работником, что оказалось наименьшим показателем по сравнению с другими странами (72–92%). Примерно две трети (67%) респондентов неправильно думали, что простуду и грипп можно лечить с помощью антибиотиков (53–76% в других странах), и более четверти (26%) — что они должны прекратить прием антибиотиков, как только почувствуют себя лучше, вместо того чтобы пройти полный курс, как предписано (47–76% — показатель среди опрошенных из других государств). Осознание термина «устойчивость к антибиотикам» среди российских респондентов была высокой: 82% против 32–89% в других странах.
Кейджи Фукуда, специальный представитель Генерального директора по устойчивости к противомикробным препаратам, сообщил: «Эта кампания является лишь одним из способов нашей работы с правительствами, органами здравоохранения и другими партнерами для уменьшения устойчивости микроорганизмов к антибиотикам. Одна из самых больших проблем здравоохранения в XXI веке требует глобального изменения поведения отдельных лиц и общественности».
ЗАКЛЮЧЕНИЕ
Применение антибиотиков в эпоху все возрастающей резистентности микроорганизмов к ним как с лечебной, так и с профилактической целью, должно быть строго обосновано. Любые произвольные решения, не подкрепленные доказательными данными, как в отношении назначения, так и, наоборот, отказа от применения антибиотиков при наличии показаний, в том числе с профилактической целью, должны быть исключены.








