Эндометриоз является хроническим эстрогензависимым заболеванием, которое поражает около 10% женщин репродуктивного возраста, пик заболеваемости приходится на возраст 25–30 лет[13, 23, 32, 35, 38, 48].
Эндометриоидные очаги могут разрастаться вне матки, в том числе в яичниках и других органах малого таза. Эти повреждения вызывают хроническую воспалительную реакцию, которая может привести к образованию рубцовой ткани и спаек[19]. У каждой четвертой женщины с эндометриозом наблюдаются симптомы дисменореи, предменструальная боль, диспареуния и хроническая усталость[7, 42]. Эндометриоз может нарушать функцию кишечника или мочевого пузыря, до 50% женщин с данным заболеванием страдают бесплодием[17, 45].
Тем не менее клинические проявления эндометриоза могут варьировать в широких пределах, многие женщины с эндометриозом могут не иметь никаких симптомов болезни[14]. Не установлено четкой взаимосвязи между степенью эндометриоидных поражений и симптомами[18].
Исследования качества жизни у пациенток с эндометриозом показывают, что проявления заболевания влияют на многие аспекты жизни женщины, в том числе на работу, получение образования, социальные взаимоотношения[16]. При усугублении клиники эндометриоза отмечается снижение качества жизни. Установлено, что у женщин, страдающих эндометриозом, производительность труда снижена на 38%, что объясняется прежде всего уменьшением эффективности работы при наличии синдрома тазовой боли[33].
В исследовании R. P. Sepulcri и соавт. (2009) показано, что 87% женщин с эндометриозом страдают депрессивными симптомами, 88% из них — тревогой. Тяжесть симптомов тревожности коррелирует с интенсивностью боли[41].
Эндометриоз сегодня представляет собой значительное экономическое бремя для семьи и общества. Задержка в диагностике, высокая частота госпитализаций, необходимость хирургических процедур, случаи сопутствующих заболеваний делают эндометриоз более дорогостоящей проблемой общественного здоровья, чем другие хронические заболевания, такие как мигрень, болезнь Крона и т. д.[29].
В настоящее время однозначный подход к лечению эндометриоза отсутствует[39]. По мнению Американского общества репродуктивной медицины, эндометриоз должен рассматриваться как хроническая болезнь, требующая пожизненного плана лечения с целью максимально использовать медикаментозные методы и избежать повторных хирургических вмешательств[36]. Хирургическое вмешательство включает абляцию эндометриоидных поражений, удаление эндометриоидных кист, разделение спаек, что может уменьшить боль и восстановить фертильность. Однако даже хорошо выполненный оперативный этап не дает полного излечения: без медикаментозной терапии частота рецидивов достигает 40–50% в течение 5 лет. Применение лекарственных препаратов уменьшает риск рецидива[39]. Поэтому в настоящее время не вызывает сомнений необходимость комплексного подхода к лечению больных эндометриозом. Двухэтапная схема (деструкция очагов эндометриоза с последующей медикаментозной терапией) является патогенетически оправданной. Результаты исследования М. И. Ярмолинской (2009) показали, что после лапароскопической коагуляции очагов эндометриоза у 42,9% женщин с овариальной недостаточностью происходит восстановление овуляторного менструального цикла, однако без гормональной терапии через 1–1,5 года у 56,3% из них вновь отмечается овариальная недостаточность[3].
Анализ литературных данных о современных способах терапии эндометриоза свидетельствует о том, что существующие методы далеки от совершенства и не обеспечивают достижения стойких клинических эффектов и научно доказанных положительных результатов. Разработка новых методов лечения эндометриоза возможна только с учетом патогенетических вариантов течения заболевания[2]. При эндометриозе используется широкий спектр гормональных препаратов: гестагены, антигонадотропины, агонисты ГнРГ (аГнРГ). Однако эффективность его лечения не всегда предсказуема. Между тем хорошо известно, что своевременное назначение адекватной терапии позволяет значительно улучшить качество жизни и сохранить репродуктивную функцию пациенток. В последние годы установлено, что результативность лечения эндометриоза может определяться также генетическими факторами, в частности функциональным состоянием генов, контролирующих активность ферментов системы детоксикации ксенобиотиков и лекарственных препаратов[2].
В последнее время для лечения эндометриоидной болезни наиболее широко применяются аГнРГ[9]. По мнению некоторых авторов, сочетанное применение аГнРГ с противовоспалительным иммуномодулятором из группы гидрофталатов при наружном генитальном эндометриозе характеризуется бо’льшим снижением уровня провоспалительных цитокинов в периферической крови, чем монотерапия аГнРГ[2]. Однако из-за выраженных эстрогендефицитных побочных эффектов (приливы, сухость во влагалище, остеопороз и др.) применение аГнРГ ограниченно. Актуальным является поиск новых препаратов для лечения эндометриоза, которые не имели бы выраженных побочных эффектов[10].
В работе K. Chwalisz и соавт. (2005) показана эффективность применения селективных модуляторов прогестероновых рецепторов для лечения эндометриоза[10].
В настоящее время для лечения тазовой боли, обусловленной эндометриозом, широко применяются НПВП. Проведены исследования, показавшие их эффективность, однако многие авторы не считают эти исследования убедительными[5, 39], НПВП невозможно применять длительно. В единичных работах изучена эффективность электроакупунктуры для купирования болевого синдрома при эндометриозе[50].
Большие перспективы, по мнению некоторых авторов, связаны с применением ингибиторов ароматазы у пациенток с эндометриозом, не реагирующих на рутинное гормональное лечение[31], но и при использовании этих препаратов возможны неприятные для женщин побочные эффекты. Кроме того, в Российской Федерации ингибиторы ароматазы в настоящее время не имеют зарегистрированных показаний для лечения эндометриоза.
По данным Г. Д. Погосян (2009), применение антагонистов ГнРГ существенно уменьшает частоту дисменореи средней и тяжелой степени. С точки зрения автора, антагонист ГнРГ цетрореликс является препаратом выбора ввиду его наиболее высокой результативности при тазовых болях и диспареунии, в то время как аГнРГ (бусерелин) предпочтителен при лечении бесплодия у женщин с эндометриозом[1].
Существуют исследования, посвященные применению антигестагена мифепристона при эндометриозе. Показано, что мифепристон и аГнРГ гозерелин (Золадекс) сходны по клинической эффективности в составе комбинированной терапии наружного генитального эндометриоза. Однако частота и тяжесть побочных эффектов при лечении аГнРГ (50%) в 2 раза выше, чем при применении антигестагена (29%)[2].
В большом количестве исследований изучена эффективность применения КОК у пациенток с эндометриозом[12, 39, 40, 47, 49]. В последний систематический обзор L. Wu и соавт. (2013) включены 15 исследований с участием женщин после консервативного и хирургического лечения эндометриоза (1850 пациенток). У получавших после хирургического лечения терапию КОК частота ремиссии была значительно выше (OR = 2,55; 95%-й ДИ: 1,68 (3,86); р < 0,00001), а частота рецидивов — ниже (OR = 0,31; 95%-й ДИ: 0,22 (0,45); р < 0,00001). Не установлено статистически значимых различий в частоте наступления беременности у женщин с бесплодием между группой пациенток, применявших КОК, и группой женщин, получавших только хирургическое лечение или другие гормональные препараты. У женщин, которые применяли КОК, гестринон, мифепристон или аГнРГ, отсутствовали статистически значимые различия в частоте рецидивов эндометриоза. Пациентки, получавшие КОК, имели меньше побочных эффектов по сравнению с теми, кто использовал другие гормональные препараты[49].
Ранее другими авторами также указывалось, что медикаментозное лечение при эндометриозе не улучшает фертильность[26, 37]. Таким образом, результаты доступных на сегодняшний день контролируемых исследований показали, что препаратами первой линии у пациенток с болевым синдромом, обусловленным эндометриозом, по-прежнему являются КОК, используемые непрерывно. КОК широко применяются для лечения симптомов эндометриоза, хотя в большинстве стран это показание для них не одобрено из-за отсутствия качественных клинических испытаний. По той же причине практические руководства могут предложить ограниченное число схем применения КОК при эндометриозе. Клинический опыт показывает, что КОК могут быть использованы у многих женщин для долгосрочной терапии эндометриоза. Но общая проблема долгосрочных непрерывных схем применения КОК — прорывные маточные кровотечения. Решением этой проблемы, вероятно, является периодическая их отмена[39].
Прогестины с пероральным и парентеральным путями введения, а также имплантаты используются в лечении эндометриоза на протяжении десятилетий[39].
Большое количество качественных исследований посвящено изучению эффективности левоноргестрелвысвобождающей внутриматочной системы (ЛНГ-ВМС) при лечении эндометриоза[8, 15, 20, 24, 27]. В настоящее время доказано, что введение ЛНГ-ВМС уменьшает боль, обусловленную эндометриозом[8, 20, 24, 27]. Введение ЛНГ-ВМС при ректовагинальном эндометриозе уменьшает болевой синдром и размеры повреждений ректовагинальной перегородки[15]. ЛНГ-ВМС также не имеет зарегистрированного показания для лечения эндометриоза, хотя входит в первую линию терапии в большинстве международных клинических рекомендаций по ведению женщин с эндометриозом после оперативного лечения.
Однако для многих препаратов этой группы не доказана эффективность в контролируемых клинических испытаниях. Прогестины, одобренные для лечения эндометриоза в разных странах, различаются. Ярким примером является медроксипрогестерона ацетат (Депо-SubQ Провера 104™, компания Pfizer, Нью-Йорк), который утвержден в последнее время Управлением по контролю за пищевыми продуктами и лекарственными препаратами (Food and Drug Administration) США для лечения эндометриоза. В Европе этот препарат внесен в черный список в связи с возможностью потери костной ткани[39].
У многих женщин непрерывное применение прогестинов эффективно для лечения боли и других симптомов эндометриоза. Тем не менее некоторые прогестины приводят к положительному результату при эндометриозе только при высоких дозах, а это может увеличить вероятность побочных эффектов, таких как нарастание веса и андрогенные проявления, повышение риска сердечно-сосудистых заболеваний.
Диеногест (Визанна) представляет собой синтетический оральный прогестаген с уникальными фармакологическими свойствами для лечения эндометриоза. Структурная формула диеногеста в сравнении с прогестероном представлена на рисунке.
Рис. Структурная формула диеногеста в сравнении с прогестероном
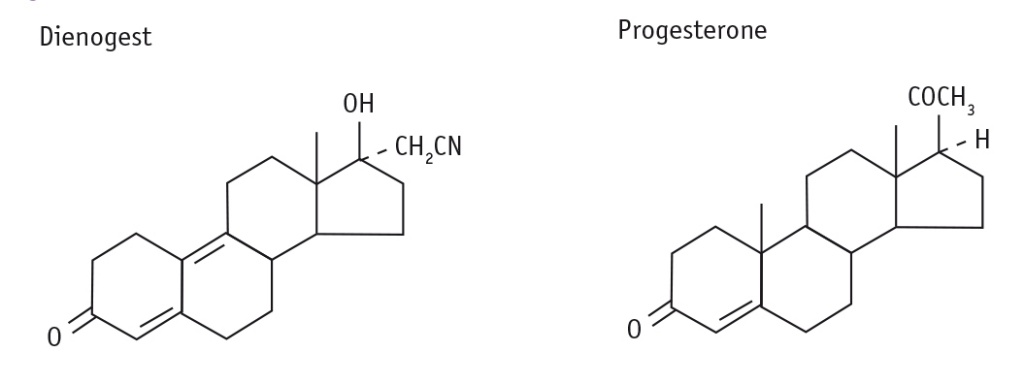
Фармакологически диеногест представляет собой комбинацию преимуществ 19-норпрогестинов и препаратов прогестерона. Связывание диеногеста с эстрогенными, глюкокортикоидными, минералокортикоидными рецепторами незначительно. В отличие от других 19-норпрогестинов, он не проявляет андрогенных эффектов и скорее обладает антиандрогенными свойствами, типичными для дериватов прогестерона, которые связаны с минимальными изменениями в липидном и углеводном обмене. Диеногест почти полностью абсорбируется и обладает высокой биодоступностью при пероральном применении, сходной с таковой у других 19-норпрогестинов. Относительно короткий период полураспада (10 часов) означает отсутствие риска аккумуляции при введении повторных доз. Более 85% дозы диеногеста, полученного перорально, выводится с мочой в течение 24 часов[39].
Диеногест подавляет эндометриоидные очаги путем влияния на различные биологические механизмы. Он умеренно подавляет секрецию гонадотропинов, что приводит к незначительному снижению продукции эстрадиола. При постоянном применении диеногест оказывает гипоэстрогенное и гиперпрогестагенное локальное эндокринное воздействие, приводящее к децидуализации эндометриальной ткани с последующей атрофией эндометрия. В экспериментальной модели эндометриоза диеногест демонстрирует антипролиферативный, противовоспалительный и антиангиогенный эффекты[39]. В настоящее время доказано, что он снижает пролиферацию, экспрессию ароматазы и ангиогенез и повышает апоптоз при эндометриозе[30].
Экспериментальное исследование, проведенное в Японии, показало, что индукция декорина диеногестом, вероятно, играет ключевую роль в подавлении эндометриоза благодаря антипролиферативному эффекту и остановке клеточного цикла продукцией р21 человеческих эктопических и эутопических эндометриальных клеток[34].
Диеногест хорошо изучен в рандомизированных плацебо-контролируемых исследованиях и одобрен для монотерапии эндометриоза в Европе, Японии, Австралии и Сингапуре. Он имеет умеренное сродство к рецепторам прогестерона и в дозе 2 мг/сут только незначительно подавляет уровень эстрадиола[39]. Лечение диеногестом хорошо переносится: в 80% случаев против 58% при использовании норэтиндрона ацетата[46].
В рандомизированных плацебо-контролируемых клинических испытаниях доказана эффективность диеногеста в купировании тазовых болей у женщин с подтвержденным эндометриозом[28].
В 24-недельном рандомизированном исследовании T. Strowitzki и соавт. (2010, 2012) показано, что диеногест так же эффективен в отношении облегчения болей, обусловленных эндометриозом, как аГнРГ лейпролида ацетат[43, 44]. В проспективном многоцентровом исследовании M. Cosson и соавт. (2002), где проводилось сравнение с трипторелином, доказана сходная эффективность диеногеста в лечении эндометриоза после лапароскопической хирургии при значительно меньших побочных эффектах[11].
Эффективность и безопасность диеногеста подтверждены во время длительного лечения (в течение 52 месяцев). Диеногест, как правило, хорошо переносился и не считался связанным с клинически значимыми андрогенными эффектами. При его использовании отмечалось значительно меньше гипоэстрогенных эффектов, чем при применении аГнРГ[39].
Диеногест в дозе 20 мг/сут не оказывает клинически значимого действия на функции надпочечников и щитовидной железы, электролитный баланс, гемопоэз, липидный обмен, ферменты печени, уровни глюкозы и инсулина. Ни в одном случае не зарегистрированы менопаузальные или нежелательные андрогензависимые эффекты. Показано, что применение диеногеста связано с увеличением количества аномальных маточных кровотечений, но это в целом хорошо переносится пациентками, частота и интенсивность кровотечений со временем снижаются. После прекращения лечения диеногестом менструальный цикл, как правило, восстанавливается. Таким образом, пероральное применение диеногеста является эффективным, хорошо переносимым вариантом долгосрочной терапии эндометриоза[39]. Определенные ограничения при этом могут быть обусловлены его контрацептивными свойствами и стоимостью[6].
В исследовании J. Kitawaki и соавт. (2011) 38 женщин с эндометриозом получали лечение аГнРГ в течение 4–6 месяцев с последующим назначением диеногеста в дозе 1 мг/сут на протяжении 12 месяцев. При этом доза диеногеста повышалась до 1,5 или 2 мг/сут, когда возникало неконтролируемое маточное кровотечение (у 33 женщин). Еще 33 женщины получали лечение только диеногестом в дозе 2 мг/сут в течение 12 месяцев. Уменьшение болевого синдрома было значительным в обеих группах и не имело значимых различий. Показано, что при приеме 1 мг диеногеста в сутки сохраняется как минимум в течение 12 месяцев эффект агонистов в отношении облегчения тазовой боли, обусловленной эндометриозом, и уменьшается количество нерегулярных маточных кровотечений, которые случаются в начале приема диеногеста[22]. Ранее J. Kitawaki и соавт. (2008) показали эффективность низких доз даназола и оральных контрацептивов в сохранении эффекта агонистов в отношении ассоциированных с эндометриозом тазовых болей[21].
В литературе представлено описание эффективного лечения глубокого инфильтративного эндометриоза у 38-летней женщины путем назначения диеногеста в дозе 2 мг/сут в течение 16 месяцев. Исходно у пациентки был эндометриодный узел мочевого пузыря размером 3,3 см, подтвержденный при цистоскопии, и имелось образование в заднем своде влагалища размером 2,6 см. Женщина страдала гематурией, дизурией, дисменореей. После проведенного лечения образования значительно (более чем на 50%) уменьшились, а симптомы были купированы. Таким образом, диеногест может быть вариантом медикаментозного лечения молодых женщин с глубоким инфильтративным эндометриозом, особенно в случае отказа от хирургического лечения[4].
U. Leone Roberti Maggiore и соавт. (2014) описан случай успешного лечения диеногестом 32-летней пациентки с эндометриозом мочевого пузыря и недержанием мочи[25].
ЗАКЛЮЧЕНИЕ
С учетом того, что каждой пациентке с эндометриозом требуется выработка индивидуального плана ведения с планированием хирургического вмешательства (при необходимости) и медикаментозного лечения, обладающего максимальной эффективностью, незначительными побочными эффектами и сохраняющего возможность реализовать репродуктивную функцию, необходимо очень тщательно выбирать препараты для терапии эндометриоза. Современные препараты обладают разной степенью эффективности и безопасности, но большинство из них невозможно применять длительно, поэтому следует оценивать соотношение рисков и пользы выбранного класса лекарственных средств.
Результаты доступных на сегодняшний день контролируемых исследований показывают, что препаратами первой линии у пациенток с болевым синдромом, обусловленным эндометриозом, по-прежнему являются комбинированные оральные контрацептивы, используемые непрерывно. Прогестины представляют разумную, приемлемую альтернативу и также относятся к терапии первой линии. У женщин с ректовагинальным и колоректальным эндометриозом следует отдавать предпочтение норэтистерона ацетату в низкой дозе. Агонисты гонадотропин-рилизинг-гормона (ГнРГ) обладают высокой эффективностью, но лекарственные средства этой группы целесообразно рассматривать в качестве терапии второй линии по причине их значительных побочных эффектов. Нестероидные противовоспалительные препараты широко используются, однако доказательства их эффективности в облегчении тазовой боли, связанной с эндометриозом, неубедительны. Такие средства, как антагонисты ГнРГ, ингибиторы ароматазы, иммуномодуляторы, селективные модуляторы рецепторов прогестерона, видимо, очень перспективны, но на данном этапе нет достаточных доказательств, чтобы поддержать их внедрение в повседневную клиническую практику[51].
Таким образом, в настоящее время безопасным и эффективным методом первой линии у пациенток с эндометриозом с зарегистрированными в Российской Федерации показаниями является пероральное назначение диеногеста в дозе 2 мг/сут как при консервативной терапии, так и после проведенного хирургического лечения.








