Многие пациенты с хроническими заболеваниями вне обострения могут достаточно успешно лечиться в домашних условиях [2]. При этом особенно результативным видится проведение длительных программ реабилитации и вторичной профилактики у больных ИБС, традиционно имеющих высокий риск госпитализации [3]. Однако развитие таких организационных форм требует значительной информационной поддержки принятия рациональных решений, обеспечивающих качественное врачебное наблюдение.
С этой точки зрения несомненный интерес представляют компьютеризированные системы поддержки принятия решений (СППР), воспроизводящие путем алгоритмизации традиционный врачебный процесс принятия решений. Внедрение документов доказательной медицины (протоколов ведения больных, клинических рекомендаций и стандартов) позитивно повлияло на разработку таких систем. Заложенная в них информация, интегрирующая результаты масштабных клинических исследований с ожиданиями пациентов, сделала возможным создание интеллектуальных СППР, предоставляющих инструменты для генерации научно обоснованных решений при использовании пациенториентированных технологий (ПОТ) [4].
Отечественная практика применения интеллектуальных СППР в организации первичной помощи пациентам с кардиоваскулярными заболеваниями (КВЗ) пока невелика; при этом отсутствуют рабочие критерии эффективности этих инструментов «электронного» здравоохранения для анализа практического применения ПОТ [5]. Очевидно, что оценки непосредственных пользователей — врачей и пациентов — будут наиболее ценными: они дополнят перечень общепринятых показателей клинической эффективности и безопасности, результаты клинического и инструментального анализа [6].
Касаясь общих вопросов применения СППР как технологического компонента ПОТ, нетрудно предположить, что в числе сфер активного потребления таких систем будут кардиоваскулярная профилактика и реабилитация как наиболее социально значимые, но наименее технически оснащенные области российского здравоохранения.
Целью исследования стала пользовательская оценка эффективности СППР как организационнофункционального компонента пациенториентированной модели реабилитационной помощи больным с острым инфарктом миокарда с подъемом сегмента ST (ИМсST).
Материалы и методы
Проспективное исследование выполнялось в течение 6 месяцев в рамках государственного задания «Создание дистанционной системы оказания реабилитационной помощи пациентам с острыми и хроническими формами ИБС после эндоваскулярных вмешательств на базе информационных технологий» на базе НИИ кардиологии ФГБОУ ВО «CГМУ им. В. И. Разумовского» Минздрава России (директор — П. Я. Довгалевский, д. м. н., профессор).
Дизайн исследования одобрен локальным этическим комитетом CГМУ им. В. И. Разумовского. В исследование включали пациентов с ИМсST, прошедших II этап кардиологической реабилитации (КР) и подписавших информированное согласие на участие. Имелись дополнительные критерии включения: наличие у больного или у членов его семьи мобильного компьютерного устройства с операционной системой Android не ниже 4.2.
Означенным критериям соответствовали 28 пациентов, составившие группу дистанционного амбулаторного наблюдения на III (амбулаторном) этапе реабилитации. Их средний возраст — 55,3 ± 5,3 года. Большинству больных (18; 64,3%) выполнили первичное чрескожное коронарное вмешательство (ЧКВ), они имели низкий/промежуточный 6месячный риск фатальных осложнений (средний балл по шкале Global Registry of Acute Coronary Events — 92 ± 12) и относились к легкой (6; 21,4%) и среднетяжелой (22; 78,6%) реабилитационным группам ИМсST. Дистанция 6минутной ходьбы у больных в среднем составляла 365 ± 17 м. Другие клинические характеристики участников представлены в таблице 1.
Таблица 1
Клиническая характеристика пациентов, включенных в исследование, n (%)
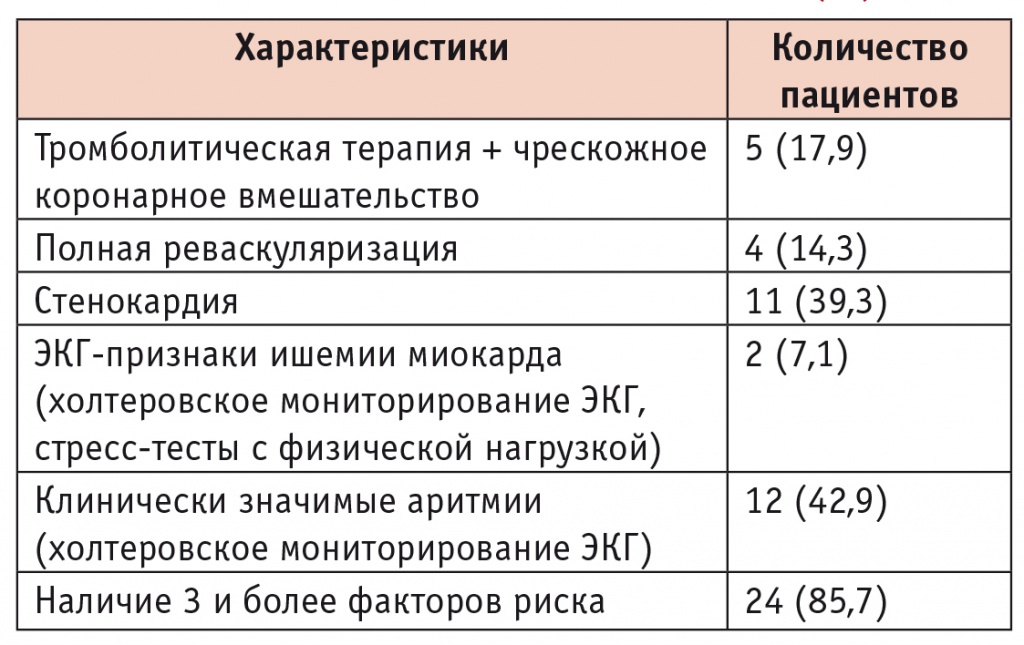
В соответствии с дизайном «точкой ввода» в исследование являлась офисная консультация врача, имеющего навыки реабилитационного консультирования. Компьютеризированный алгоритм консультирования предоставлялся СППР «Выбор программы физической реабилитации для пациентов с инфарктом миокарда с подъемом сегмента ST» (Свидетельство о государственной регистрации программы для ЭВМ № 2016618410 от 28.07.2016 г.) и был разработан на основе российских клинических рекомендаций [7]. Заключительным документом консультации была электронная «Реабилитационная карта пациента», содержащая структурированные медицинские данные и автоматически сформированную индивидуальную программу КР, хранящаяся в личном профиле пациента в виде «Истории реабилитации».
В процессе обсуждения отдельных мероприятий программы КР оценивали способность врача и пациента к выработке совместных лечебнореабилитационных решений. Анализировали пять коммуникативных поведенческих категорий: I — демонстрация уверения и убеждения пациента в необходимости применения той или иной врачебной рекомендации; II — формирование у него уверенности и убежденности в необходимости выполнения рекомендации; III — врачебное информирование больного о наличии особенностей выполнения рекомендации; IV — получение от пациента информации об изменении отношения и индивидуальных эффектах в процессе применения или выполнения рекомендации; V — достижение взаимного согласия на выполнение той или иной рекомендации с градацией по разрядам: 0 — не выражено, 1 — слабо выражено, 2 — сильно выражено. При сумме баллов, равной 10, делалось заключение о наличии полного совместного решения; за отсутствие решения принимался 0 баллов. Промежуточные значения оценивались как «близкие к совместному решению» (6–9 баллов) или «далекие от совместного решения» (1–5 баллов) [8].
Оценка пригодности СППР для принятия врачебных решений проводилась по результатам пользовательского тестирования. Группу респондентов составили 15 врачейспециалистов (врачи кардиологического диспансера, кардиологического отделения санатория, городских поликлиник). Использовались специально подготовленные задания (45 вариантов), соответствующие интерфейсу программы и содержащие описания реальных клинических ситуаций в контексте сценария «Формирование программы III этапа физической реабилитации для пациента с инфарктом миокарда». В программу тестирования входило заполнение опросника, включающего вопросы, связанные с обнаруженными недостатками СППР, трудностями использования и удовлетворенностью работой. Анализировались по 10 балльной шкале следующие ключевые метрики: характеристика респондентов, оценка интерфейса, оценка работы пользователя с системой. Число допущенных ошибок рассчитывалось как соотношение отвергнутых врачом ответов из общего числа вариантов, предложенных СППР.
Оценка пациентами качества реабилитационных программ, сформированных СППР, производилась по данным их электронных отчетов (electronic PatientReported Outcomes, еPRO) в процессе интернетмониторинга мероприятий физической реабилитации (ФР) [9]. Дистанционный мониторинг (ИАС «РеаПроф», «Волготех», Россия) включал контроль клиникофункциональных параметров, необходимых для коррекции лекарственной терапии и реабилитационных программ. Мониторировались данные самостоятельных измерений: уровня АД, ЧСС, количества шагов по данным шагомера, субъективные показатели переносимости физических нагрузок, ЭКГ. Телеметрия ЭКГ выполнялась как аутотрансляция с использованием мобильных устройств и «облачного» сервиса ECG Dongle («НордавиндДубна», Россия). Данные саморегистрации анализировались сотрудником кабинета телеметрии НИИ кардиологии и использовались для принятия решений в формате отсроченного телемедицинского консультирования.
Конфиденциальность данных пациента достигалась особенностями процедуры регистрации в интернетсервисе с использованием кодирования и индивидуальной идентификации для персонального доступа. Идентификационные данные врача и пациента (включая логин и пароль) не сохранялись в системе, а имелись только у врача (для доступа к данным больного) и у пациента (для входа в личный кабинет); при этом врач имел доступ к электронным картам пациента, содержащимся только в его профиле.
Статистический анализ выполнен с помощью пакета прикладных программ Excel. Для количественных показателей определялись средние значения (М), среднее квадратичное отклонение (σ) и стандартная ошибка среднего (SD). Различия считали статистически значимыми при р < 0,05.
Результаты
Оценка степени вовлеченности пациентов в процесс принятия решений о дальнейших терапевтических планах показала, что уже в ходе первичного (офисного) консультирования 10 (35,7%) больных выразили полное согласие выполнять лечебнореабилитационные рекомендации; еще 12 (42,9) были близки к этому. У 6 (21,4%) человек ситуация была оценена как «далекая от совместного решения» и «отсутствие совместного решения».
Группа тестирования врачей была представлена в основном специалистами амбулаторного звена различной квалификации — потенциальными пользователями реабилитационной СППР, 6 (40%) из которых имели опыт работы с программными продуктами подобного назначения. При общем позитивном настрое (80%) перед тестированием СППР успешное выполнение задания продемонстрировало подавляющее большинство участников — 12 (80%) (табл. 2).
Таблица 2
Ключевые метрики оценки системы поддержки принятия решений (ССПР) по результатам пользовательского тестирования
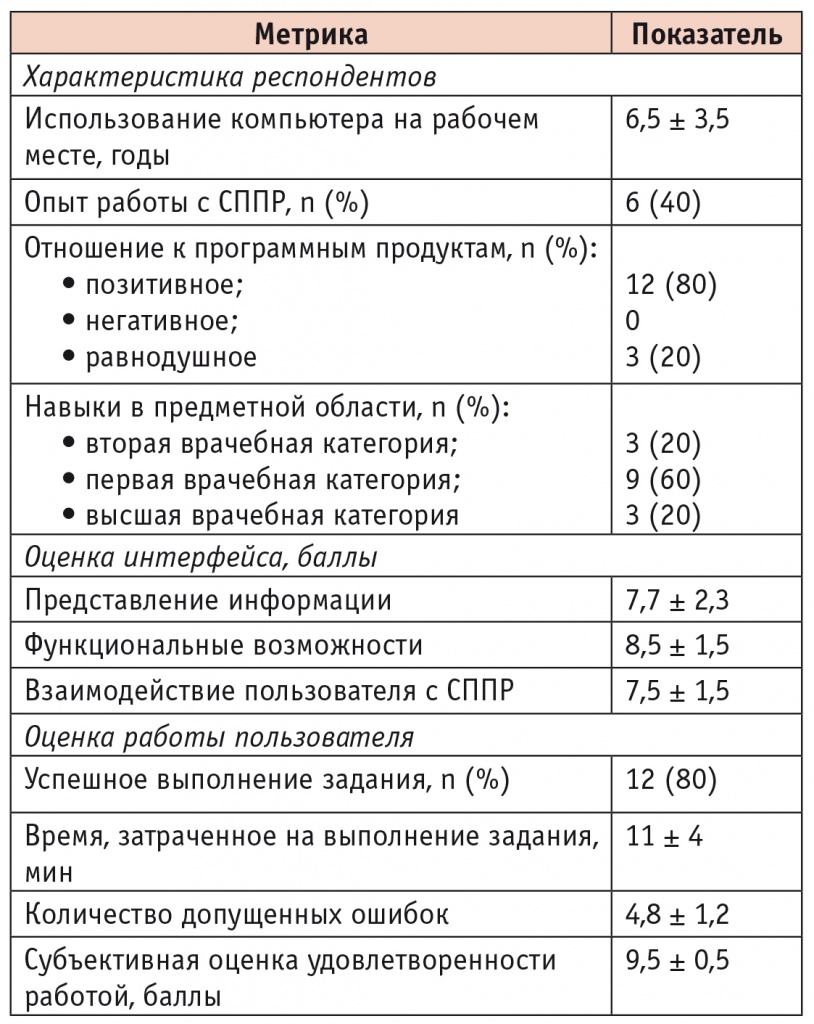
Средняя продолжительность формирования электронного документа «Реабилитационная карта пациента» составила 11 ± 4 мин (при условии автоматической обработки опросника «Мотивационная готовность пациента к реабилитации»). При этом число врачебных ошибок, связанных с назначением мероприятий реабилитации, — 4,8 ± 1,2. Наиболее типичные ошибки касались: 1) интерпретации автоматических оценок уровня и типа мотивации пациента к реабилитации; 2) учета противопоказаний к мероприятиям КР; 3) учета риска осложнений на этапах ФР; 4) выбора основных позиций реабилитационных программ, связанных с риском осложнений у пациента с ИМсST. Участники не назвали ни одной функции/термина СППР, незнакомых врачу. В числе рекомендации по оптимизации были повышение доступности СППР и возможность ее представления в формате webприложения (портала).
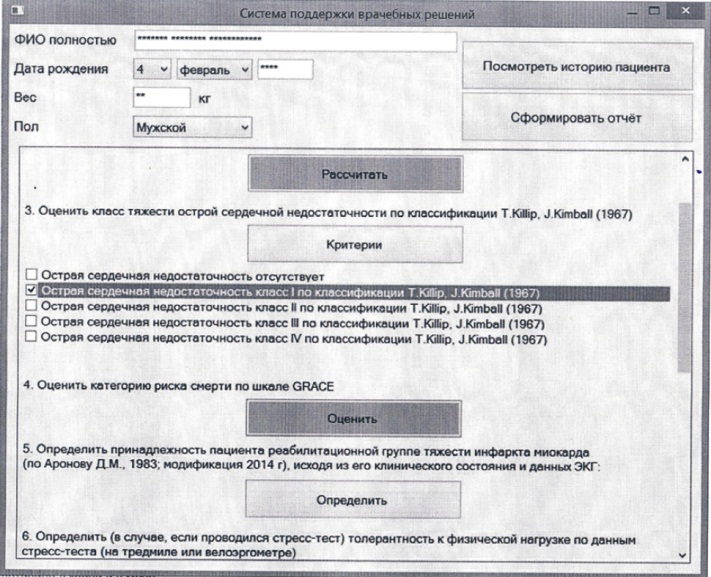
Следующий этап исследования пользовательской эффективности — выход за пределы проверочных сценариев и оценка полученных решений другим реальным пользователем продукта СППР — пациентом. Анализ информации, извлеченной в течение 6 месяцев наблюдения из ePRO, показал, что у 15 (53,6%) больных имел место преимущественно физиологический тип реакции на тренировочные нагрузки в рамках сформированной СППР программы ФР (рис.); 6 (21,4%) пациентам с промежуточным типом реакции проводилась коррекция физических нагрузок в рамках дистанционной консультации. Исключение составили 7 (25,0%) человек с выявленными критериями патологической реакции, потребовавшими не только коррекции домашних программ ФР, но и изменения тактики ведения. Стоит заметить, что в основном это были ЭКГкритерии: депрессия сегмента ST, нарушения ритма и проводимости. Тактические решения касались дополнительного планового обследования, в т. ч. проведения суточного мониторирования ЭКГ у 3 и коронароангиографии у 2 пациентов с неполной первичной реваскуляризацией и у 2 человек без реваскуляризации в анамнезе.
Рис. Этап автоматического формирования программы физической реабилитации
Обсуждение
Реальные условия принятия решений в области КР выдвигают на первое место вопросы информационной поддержки, соответствующей сегодняшнему уровню знаний в этой области. Конкретная задача заключается в повышении оперативности, достоверности и обоснованности реабилитационных рекомендаций и программ в целом.
Анализ эффективности оказания реабилитационной помощи в 13 субъектах РФ (17 лечебных учреждениях) выявил наличие значительных трудностей с организацией III этапа КР у всех участников исследования. В рейтинге факторов, сдерживающих оказание реабилитационной помощи пациентам с КВЗ в амбулаторных условиях, лидировали «отсутствие подготовленных специалистов» (77%) и «отсутствие или недостаточное освещение вопросов реабилитации в повседневной практике» (67%). При этом готовность больных к продолжению реабилитации после выписки из стационара была достаточно высокой (62%) при наличии реальных условий для ее оказания (87% по данным опроса врачей) [10]. Эти и другие выводы «Пилотного проекта» подтверждают высокую потребность амбулаторной практики в инструментах функциональной поддержки и организации КР, что обусловило цель и задачи нашего исследования.
В международных требованиях к технологиям, ориентированным на человека, в перечне ключевых условий указывается активное вовлечение всех участников процесса при наличии необходимого уровня понимания ими технологических задач и оптимальном распределении функций между техническим средством и пользователями [11]. Высокая степень вовлеченности пациентов в процесс совместного принятия решений показана в нашем исследовании уже в ходе первичного реабилитационного консультирования в виде «полного совместного решения» у 10 (35,7%) и «близости к полному совместному решению» у 12 (42,9%) больных.
При этом совместное решение о дальнейшем наблюдении вырабатывалось в ходе общения пациента с врачом при убежденности больного в необходимости, безопасности и эффективности врачебных рекомендаций, достижения согласия и перспективы постоянных контактов и обмена информацией. Полученные результаты, на наш взгляд, были обусловлены высоким методическим уровнем врачебного реабилитационного консультирования и его информационнотехнического оснащением (использованием СППР).
Целью пользовательского тестирования СППР в исследовании являлось выяснение уровня понимания врачами технологических задач, решаемых с ее помощью, и обоснованности заложенного распределения функций. В медицинских системах две эти характеристики приобретают особый смысл, поскольку традиционно имеет место недоверие со стороны врачейпользователей к результатам, автоматически генерируемым программными средствами. Кроме этого, на респондентов в этом исследовании было возложено определение «слабых мест» СППР в алгоритме принятия персонализированных реабилитационных решений.
С учетом того факта, что разработанная СППР — программный продукт, целиком построенный на современных знаниях и использующий для генерации программ реабилитации научно обоснованный алгоритм выбора отдельных мероприятий КР, мы рассматривали работу врача с системой как дополнительный функционал в виде повышения уровня практического внедрения клинических рекомендаций. Так, при анализе пользовательского интерфейса метрики «представление информации» и «функциональные возможности» получили довольно высокие оценки (7,7 ± 2,3 и 8,5 ± 1,5 балла соответственно). Итоговая субъективная оценка удовлетворенности врачей работой с СППР также оказалась довольно высокой (9,5 ± 0,5 балла). Такой результат мы объясняем еще и тем, что в группе разработчиков (экспертов) СППР были врачиисследователи — потенциальные пользователи инструмента в рамках выполнения прикладного научного исследования.
В основе ПОТ ведения пациентов с КВЗ лежит постулат «чем эффективнее лечение в амбулаторных условиях, тем меньше вероятность госпитализации». Доказано, что залогом успешного применения этого правила являются 1) проведение программ профилактики; 2) осуществление программ ведения хронических больных; 3) активное вовлечение пациентов в процесс лечения [12]. Помощь пациенту в принятии решений может предоставляться в виде подробной информации о недостатках/преимуществах метода не только в рамках офисных консультаций, но и дистанционно через Интернет [13]. В проведенном исследовании данные ePRO, собранные дистанционно в соответствии с доказательными критериями переносимости физических нагрузок, были положены в основу оценки безопасности и эффективности программ ФР, полученных с помощью СППР. Так, по данным 6месячного мониторинга, большинство пациентов (53,6%) адекватно реагировали на рекомендованные нагрузки, демонстрируя физиологический ответ на программы ФР. Больным с промежуточным типом ответа потребовалась дистанционная коррекция параметров программы; появление критериев патологической реакции служило поводом для офисных консультаций и принятия серьезных тактических решений.
В современной практике, ориентированной на пациента, данным их отчетов придается большое клиническое и аналитическое значение. Так, в определении действенности реабилитации эти документы могут выступать в роли первичной или вторичной конечной точки; например, утомляемость или боль в субъективной оценке реакции могут оказаться единственной реальной конечной точкой при отсутствии других маркеров, подлежащих инструментальному или лабораторному измерению [14]. Регистрация конкретных субъективных ощущений у пациентов с недавно перенесенным ИМсST, совмещенная с необходимыми самостоятельными измерениями, дает наиболее надежную информацию и позволяет представить реальную динамику заболевания под влиянием реабилитационных вмешательств.
Выводы
1. Место СППР в организации пациенториентированной модели реабилитационной помощи на амбулаторном этапе наблюдения определяется высоким уровнем потребности врачей в информационнокоммуникационной поддержке принятия эффективных решений, отвечающих доказательным критериям безопасности и переносимости домашних программ ФР.
2. Использование интеллектуальной СППР, разработанной на базе клинических рекомендаций, расширяет возможности реабилитационного офисного консультирования пациентов с КВЗ. Ее применение не только обеспечивает врача доказательно обоснованной информацией, но и сокращает время, затраченное на формирование программ ФР.
3. СППР, предназначенная для решения конкретных задач реабилитации и разработанная при участии экспертов в области КР, напрямую заинтересованных в конечном программном продукте, продемонстрировала высокую пользовательскую эффективность по результатам тестирования врачейкардиологов.
4. Пригодность для пациентов программ ФР, генерируемых СППР, может и должна быть оценена ими в отношении подтверждения безопасности, переносимости и эффективности. Использование ePRO с этой целью позволяет получить информацию для формирования выводов о характере индивидуальной реакции при выполнении домашних программ ФР.
Заключение
Проведение данного исследования было инициировано существующими потребностями в обновлении модели организации амбулаторной кардиологической реабилитации (КР) пациентов, перенесших инфаркт миокарда с подъемом сегмента ST. Оценка компьютеризированной информационнокоммуникационной системы поддержки принятия решений, разработанной на базе доказательной медицины, непосредственными участниками реабилитационного процесса показала ее высокую практическую значимость и достаточную эффективность в организации домашних программ КР. Применение информационнокоммуникационных технологий для вовлечения пациентов в лечебнореабилитационный процесс позволило не только получить информацию о безопасности автоматически сформированных программ КР, но и оценить ее значимость для принятия пациенториентированных тактических решений в процессе амбулаторного реабилитационного наблюдения.








