ВВЕДЕНИЕ
Основными этиологическими факторами развития пороков сердца у населения развитых стран являются дегенеративное поражение и кальцификация клапана аорты. В структуре патологии клапанного аппарата сердца удельный вес тяжелого аортального стеноза достигает 41,2% [1]. Пятилетняя смертность у пациентов со средним и тяжелым аортальным стенозом без хирургического лечения составляет 56% и 67% соответственно [2], что определяет исключительную важность своевременного хирургического вмешательства.
С целью коррекции пороков аортального клапана выполняют два типа реконструктивных операций: открытые (в условиях искусственного кровообращения) и рентген-хирургические (транскатетерная имплантация аортального клапана). По данным регистра, включавшего 867 658 случаев протезирования аортального клапана в Соединенных Штатах Америки в 2003–2016 гг., произошло линейное увеличение количества открытых и рентген-хирургических операций с 96 до 137 на 100 000 человек, при этом доля рентген-хирургических операций достигла 40% [3].
Концепция послеоперационной мозговой дисфункции успешно применяется в хирургической и клинической практике с 2014 г. для профилактики, своевременной диагностики и лечения основных нозологических форм церебральных последствий хирургических операций (рис.) [4, 5].
Рис. Патогенез и клинические типы послеоперационной мозговой дисфункции при хирургических операциях
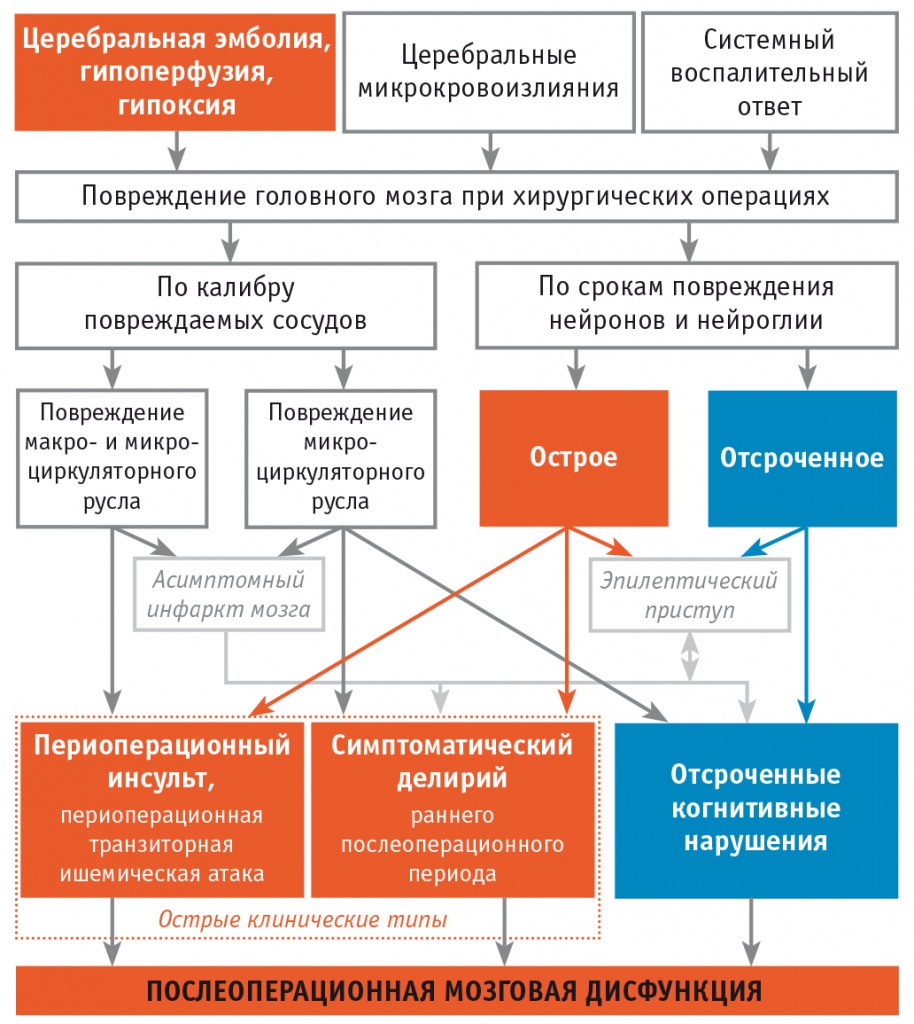
С учетом преимущественно сосудистого генеза послеоперационной мозговой дисфункции клинический опыт ведения пациентов с цереброваскулярной болезнью используется для решения задач по защите головного мозга у больных хирургического профиля. При операциях коронарного шунтирования доказана эффективность предоперационной церебропротекции с применением таблетированной формы антигипоксантного цитопротективного комбинированного лекарственного препарата на основе янтарной кислоты [4], который с 2021 г. имеет новое показание к применению — профилактика когнитивных расстройств после обширных хирургических вмешательств у пациентов пожилого возраста.
Нейромедиаторную основу послеоперационной мозговой дисфункции составляет холинергический дефицит, который в ангионеврологической практике в течение более чем 20 лет безопасно и эффективно корректируется применением холина альфосцерата [6]. Компенсация церебральной холинергической нейромедиаторной недостаточности ускоряет восстановление при синдроме спутанности в остром периоде ишемического инсульта [7].
Перспективным направлением защиты головного мозга в хирургической практике является раннее послеоперационное применение антигипоксантных и нейромедиаторных препаратов.
Цель исследования: определить структуру послеоперационной мозговой дисфункции при открытом и рентген-хирургическом протезировании аортального клапана, а также установить факторы риска и способы профилактики послеоперационной мозговой дисфункции при открытых операциях.
МАТЕРИАЛЫ И МЕТОДЫ
Нами обследованы 114 пациентов (92 мужчины и 22 женщины) в возрасте 67 [58; 76] лет, которым были выполнены плановые хирургические операции протезирования аортального клапана сердца. Все пациенты проходили стационарное обследование и лечение на Первой кафедре и клинике хирургии (усовершенствования врачей) имени П.А. Куприянова Военно-медицинской академии имени С.М. Кирова (г. Санкт-Петербург).
Критерии включения в исследование:
-
планируемая открытая или рентген-хирургическая операция протезирования аортального клапана;
-
возраст старше 18 лет.
Критерии невключения:
-
наличие ранее установленного диагноза новообразования головного мозга, демиелинизирующего заболевания ЦНС, эпилепсии, деменции;
-
ЧМТ или нейрохирургическое вмешательство в течение предшествующих 3 лет;
-
мозговой инсульт в течение предшествующих 3 месяцев;
-
беременность;
-
неспособность пациента к нейропсихологическому и психометрическому обследованию на момент включения в исследование.
Все больные были распределены на три группы: «открытая операция» (n = 82), «церебропротекция» (n = 16) и «рентген-хирургия» (n = 16). В группах «открытая операция» и «церебропротекция» пациентам выполняли открытые хирургические операции протезирования аортального клапана в условиях искусственного кровообращения, в группе «рентген-хирургия» — транскатетерную имплантацию аортального клапана (transcatheter aortic valve implantation). Характеристика исследуемых групп представлена в таблице 1.
Таблица 1
Характеристика исследуемых групп
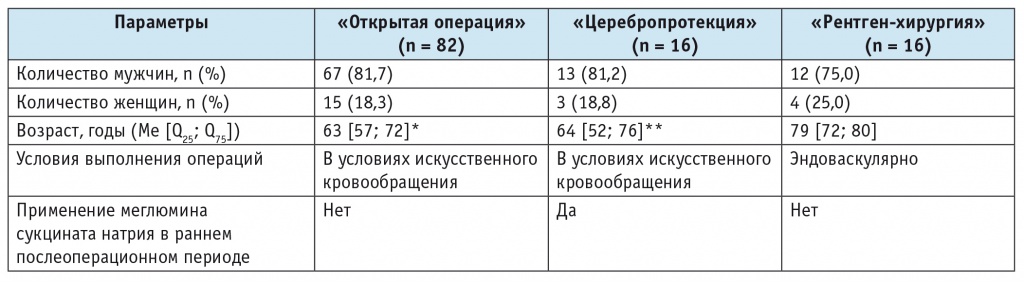
Примечание. Отличия от группы «рентген-хирургия» статистически значимы: (*) — р = 0,0233; (**) — р = 0,0215.
Все пациенты в периоперационном периоде получали стандартное медикаментозное лечение с учетом основного и сопутствующих заболеваний (в т. ч. антиагрегантные или антикоагулянтные, антигипертензивные, антиаритмические лекарственные препараты), симптоматическую терапию. Пациенты в группе «церебропротекция» дополнительно получали 1,5% раствор меглюмина натрия сукцината с 1-го по 5-й день после хирургической операции по схеме: 250 мл один раз в день утром (после еды) в/в капельно со скоростью 20–40 капель/мин. В группах «открытая операция» и «рентген-хирургия» пациенты не получали меглюмина натрия сукцинат.
Для диагностики послеоперационной мозговой дисфункции и ее клинических типов проведено комплексное периоперационное обследование всех больных:
-
неврологический осмотр и оценка неврологического статуса с использованием шкалы National Institutes of Health Stroke Scale за 2–3 сут до операции и через 3 сут после операции (при выявлении клинических признаков периоперационного инсульта выполняли КТ головного мозга);
-
оценка спутанности сознания методом CAM (Confusion Assessment Method) в раннем послеоперационном периоде, при подозрении на делирий — с последующей консультацией психиатра для подтверждения диагноза;
-
нейропсихологическое тестирование по шкале Montreal Cognitive Assessment (MoCA) и батарее Frontal Assessment Battery (FAB) за 2–3 сут до операции и через 7–10 сут после операции (у пациентов с периоперационным инсультом послеоперационное нейропсихологическое тестирование не выполняли);
-
психометрическая оценка по шкале Hospital Anxiety and Depression Scale за 2–3 сут до операции и через 7–10 сут после операции.
Отсроченные когнитивные нарушения (послеоперационную когнитивную дисфункцию) диагностировали при послеоперационном уменьшении числа баллов по шкале MoCA и/или батарее FAB на 2 и более по сравнению с предоперационными значениями [8].
Все пациенты подписали добровольное информированное согласие на участие в исследовании. Проведение исследования одобрено локальным этическим комитетом ФГБВОУ ВО «Военно-медицинская академия имени С.М. Кирова» Министерства обороны Российской Федерации.
Статистическая обработка данных произведена в среде IBM SPSS v23, Statistica for Windows v12, на табличном процессоре MS Excel 2013. На первом этапе отобранные независимые переменные (n = 75) были разделены по шкалам изменения на дихотомические, порядковые (до 5 рангов) и количественные. На втором этапе для дихотомических факторов рассчитаны коэффициенты корреляции с исходами (послеоперационная мозговая дисфункция в целом и ее клинические формы) в режиме четырехпольных таблиц сопряженности.
Для порядковых факторов использованы многопольные таблицы сопряженности (2 × n, где n — число рангов) с выделением ранга, по достижении которого растет частота исходов. Данный ранг обозначался уровнем отсечения (cut-off), переменная из ранговой превращалась в дихотомическую со значением 0, если ранг не был достигнут, и со значением 1, если ранг был достигнут.
Для количественных факторов рассчитаны cut-off уровни при помощи ROC-анализа с исходом в качестве прогнозируемой переменной. Значение уровня отсечения получено по максимальной сумме чувствительности и специфичности (метод Юдена).
Различия считали статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ
По результатам обследования в предоперационном периоде рассеянная неврологическая симптоматика или неврологический синдром были выявлены у 72 (63,2%) пациентов, из них у 14 (19,4%) в анамнезе был диагностирован мозговой инсульт (табл. 2).
Таблица 2
Результаты предоперационного обследования пациентов
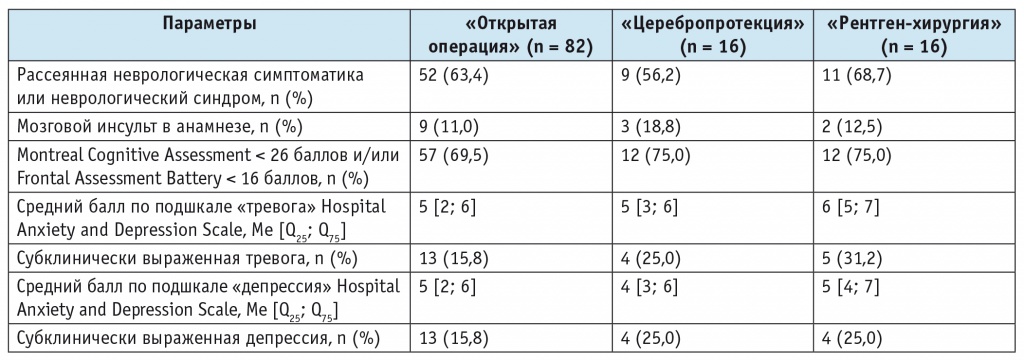
По данным предоперационной психометрической оценки, клинически выраженная тревога и/или депрессия отсутствовали у пациентов исследуемых групп.
По результатам комплексного периоперационного обследования частота послеоперационной мозговой дисфункции и ее клинических типов при протезировании аортального клапана сердца была следующей:
-
послеоперационная мозговая дисфункция — 47 (41,2%);
-
острые клинические типы послеоперационной мозговой дисфункции — 21 (18,4%);
-
периоперационный инсульт — 2 (1,7%);
-
симптоматический делирий раннего послеоперационного периода — 19 (16,7%);
-
отсроченные когнитивные нарушения — 32 (28,6%) из 112 пациентов (исключены 2 человека с инсультом) (табл. 3).
Таблица 3
Структура послеоперационной мозговой дисфункции при хирургических операциях протезирования аортального клапана, n (%)
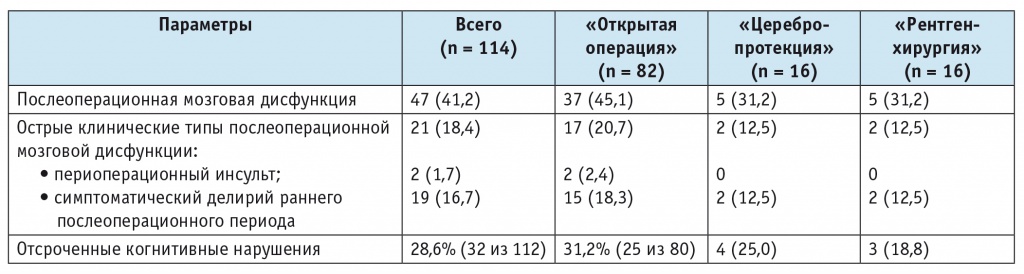
Периоперационный инсульт выявлен только в группе «открытая операция» у двух пациентов, в дальнейшем один из них умер. Наиболее частым клиническим типом послеоперационной мозговой дисфункции явились отсроченные когнитивные нарушения, у шести пациентов диагностированы два клинических типа — симптоматический делирий раннего послеоперационного периода и отсроченные когнитивные нарушения. Различий по частоте и структуре послеоперационной мозговой дисфункции между исследуемыми группами не было.
По результатам анализа полученных данных установлены 18 факторов риска послеоперационной мозговой дисфункции и ее клинических типов при открытых хирургических операциях протезирования аортального клапана. Большинство (15 из 18) факторов риска являются предоперационными, ниже все установленные факторы риска перечислены по мере уменьшения ОШ.
Из 75 оценивавшихся параметров значимую связь с развитием послеоперационной мозговой дисфункции показали следующие:
-
уровень липопротеинов очень низкой плотности в плазме крови более 1,0 ммоль/л (ОШ = 6,83; 95% ДИ: 2,80–16,69; p < 0,0001);
-
уровень общего холестерина в плазме крови более 5,0 ммоль/л (ОШ = 6,64; 95% ДИ: 2,68–16,46; р < 0,0001);
-
уровень ЛПНП в плазме крови более 3,2 ммоль/л (ОШ = 4,41; 95% ДИ: 1,86–10,46; p = 0,0008);
-
АГ, требующая приема антигипертензивных лекарственных препаратов (ОШ = 4,03; 95% ДИ: 1,53–10,61; p = 0,0047);
-
продолжительность ИВЛ более 14,5 ч (ОШ = 3,51; 95% ДИ: 1,51–8,11; p = 0,0034);
-
возраст старше 73 лет (ОШ = 3,33; 95% ДИ: 1,25–8,87; p = 0,0159).
Для периоперационного инсульта не определены факторы риска, что может быть связано с малым количеством случаев периоперационного инсульта в исследуемых группах.
Для симптоматического делирия раннего послеоперационного периода найдено наибольшее количество факторов риска:
-
предоперационный балл по шкале MoCA менее 20 (ОШ = 17,11; 95% ДИ: 4,29–68,33; p = 0,0001);
-
уровень липопротеинов очень низкой плотности в плазме крови более 1,3 ммоль/л (ОШ = 8,77; 95% ДИ: 2,78–27,70; p = 0,0002);
-
ударный объем ЛЖ менее 63 мл (ОШ = 5,80; 95% ДИ: 1,91–17,61; p = 0,0019);
-
минимальный интраоперационный гематокрит менее 26% (ОШ = 4,35; 95% ДИ: 1,44–13,12; p = 0,009);
-
давность выявления порока аортального клапана менее 2,5 года (ОШ = 4,33; 95% ДИ: 1,16–16,24; p = 0,0296);
-
атеросклеротический стеноз брахиоцефальных артерий (ОШ = 3,47; 95% ДИ: 1,07–11,30; p = 0,0388);
-
отсутствие высшего или среднего специального образования (ОШ = 3,08; 95% ДИ: 1,01–9,41; p = 0,0484).
Для отсроченных когнитивных нарушений определены следующие факторы риска:
-
уровень общего холестерина в плазме крови более 5,1 ммоль/л (ОШ = 4,64; 95% ДИ: 1,84–11,67; p = 0,0011);
-
АГ, требующая приема антигипертензивных лекарственных препаратов (ОШ = 4,27; 95% ДИ: 1,34–13,61; p = 0,0142);
-
предоперационный уровень тромбоцитов менее 220 × 109/л (ОШ = 4,15; 95% ДИ: 1,42–12,14; p = 0,0093);
-
средний интраоперационный гематокрит менее 28% (ОШ = 4,01; 95% ДИ: 1,61–10,01; p = 0,0029);
-
уровень липопротеинов очень низкой плотности в плазме крови более 1,2 ммоль/л (ОШ = 4,01; 95% ДИ: 1,61–9,99; p = 0,0029);
-
уровень ЛПНП более 3,2 ммоль/л (ОШ = 3,74; 95% ДИ: 1,51–9,28; p = 0,0044).
При изучении особенностей послеоперационной мозговой дисфункции при протезировании аортального клапана сердца также установлены два церебропротективных фактора — предоперационный ИМТ более 25 кг/м2 и применение меглюмина натрия сукцината в раннем послеоперационном периоде. При предоперационном ИМТ более 25 кг/м2 уменьшалась вероятность развития симптоматического делирия раннего послеоперационного периода (ОШ = 0,32; 95% ДИ: 0,11–0,95; p = 0,0407). Продолжительность симптоматического делирия в группе «церебропротекция» была меньше, чем в группе «открытая операция»: 1,5 [1,25; 1,75] дня против 4,0 [3,0; 5,0] дней (p = 0,0441).
ОБСУЖДЕНИЕ
Отсутствие различий по частоте и структуре послеоперационной мозговой дисфункции при открытых и рентген-хирургических операциях протезирования аортального клапана сердца демонстрирует однородность влияния этих видов хирургических операций на функциональное состояние головного мозга. Более старший возраст пациентов в группе «рентген-хирургия» является наиболее вероятной причиной отсутствия значимого церебропротективного эффекта транскатетерной имплантации аортального клапана.
Преобладание предоперационных факторов риска послеоперационной мозговой дисфункции указывает на важность их своевременной диагностики и коррекции в течение всего предоперационного периода, начиная с момента выявления показаний к хирургическому вмешательству.
По данным литературы, ведущими причинами повреждения головного мозга при операциях на сердце считаются церебральная эмболия и церебральная гипоперфузия [4, 9–11], при этом в кардиохирургии две трети периоперационных ишемических инсультов происходят на границе водоразделов бассейнов кровоснабжения головного мозга, что характерно для ишемического инсульта вследствие гипоперфузии [12, 13]. Установленные в ходе нашего исследования сосудистые факторы риска послеоперационной мозговой дисфункции и ее клинических типов (дислипидемия, ударный объем ЛЖ менее 63 мл, атеросклеротический кардиосклероз брахиоцефальных артерий, минимальный интраоперационный гематокрит менее 26%, средний интраоперационный гематокрит менее 28%) подтверждают роль церебральной гипоперфузии в патогенезе послеоперационной мозговой дисфункции.
Необходимость применения антигипертензивных лекарственных препаратов характеризует более позднюю стадию гипертонической болезни и более высокую степень АГ. Длительно существующая АГ повышает риск церебральных микрокровоизлияний, в том числе периоперационных церебральных микрокровоизлияний. Это может объяснять роль АГ, требующей приема антигипертензивных лекарственных препаратов, как фактора риска послеоперационной мозговой дисфункции. Низкий уровень интраоперационного гематокрита является фактором риска периоперационных церебральных микрокровоизлияний в кардиохирургии [14], что также может объяснять механизм влияния низкого интраоперационного гематокрита на вероятность симптоматического делирия раннего послеоперационного периода и отсроченных когнитивных нарушений.
По данным предоперационного обследования, большинство пациентов имели клинические признаки цереброваскулярной болезни. Кроме того, большинство установленных факторов риска являются общими для послеоперационной мозговой дисфункции и церебральной микроангиопатии (в том числе болезни малых сосудов) — пожилой и старческий возраст, гипертоническая болезнь и необходимость приема антигипертензивных препаратов, дислипидемия, атеросклеротический стеноз брахиоцефальных артерий.
Распространенность церебральной микроангиопатии в популяции у лиц в возрасте до 50 лет составляет 5%, она выявляется почти у всех больных старше 90 лет [15]. Микроангиопатия — ведущий патогенетический фактор в 25% случаев церебральных ишемических инсультов [16] и в 45% случаев деменции [17].
Протезирование аортального клапана выполняют преимущественно пациентам пожилого и старческого возраста, часто имеющим клинические признаки поражения головного мозга, в том числе когнитивные нарушения. Вышеизложенное позволяет предположить высокую распространенность церебральной микроангиопатии и ее значительную роль в патогенезе послеоперационной мозговой дисфункции при протезировании аортального клапана.
Первым из двух установленных церебропротективных факторов явился предоперационный ИМТ более 25 кг/м2. Средний ИМТ у пациентов с симптоматическим делирием раннего послеоперационного периода составил 26,4 ± 3,9 кг/м2, без него — 28,3 ± 4,4 кг/м2. Пациенты с выраженным дефицитом массы тела (ИМТ менее 15,9 кг/м2) и ожирением III степени (ИМТ более 40 кг/м2) отсутствовали в нашем исследовании.
Послеоперационный период характеризуется повышением активности катаболических процессов [18, 19]. Вероятно, меньшая значимость катаболических процессов у пациентов с умеренно повышенным предоперационным ИМТ может объяснять его церебропротективные свойства в послеоперационном периоде.
Системный воспалительный ответ также оказывает существенное влияние на функциональное состояние головного мозга после кардиохирургических операций [4, 9, 20], поэтому церебропротективные свойства раннего послеоперационного применения меглюмина натрия сукцината могут быть результатом сочетания антигипоксантного и дезинтоксикационного действия.
ЗАКЛЮЧЕНИЕ
Различные виды протезирования аортального клапана характеризуются высокой частотой послеоперационной мозговой дисфункции, развивающейся более чем у 40% пациентов. С учетом продолжающегося увеличения количества операций протезирования аортального клапана необходимо дальнейшее совершенствование методов периоперационной церебропротекции, основными направлениями которой являются своевременная диагностика и коррекция факторов риска, дифференцированная тактика ведения пациентов в зависимости от вероятности развития послеоперационной мозговой дисфункции, а также применение нефармакологических и фармакологических методов защиты головного мозга.
Поступила: 11.01.2022
Принята к публикации: 02.02.2022








