ВВЕДЕНИЕ
Согласно третьей редакции Международной классификации головной боли (МКГБ-3) (2018)1, лекарственно-индуцированная (ЛИГБ), или абузусная, головная боль является хронической цефалгией, возникающей чаще 15 дней в месяц у пациентов, страдающих одной из первичных форм головной боли, в результате регулярного и избыточного использования средств для купирования приступов цефалгии на протяжении более 3 месяцев. Абузусная головная боль формируется при приеме 15 и более доз в месяц простых анальгетиков на протяжении 3 месяцев, а для триптанов, эрготамина, комбинированных и опиоидных анальгетиков пороговое значение — 10 доз в месяц2. Таким образом, согласно МКГБ-3, достоверный диагноз ЛИГБ может быть установлен уже во время первичного осмотра[1]. Важно, что у пациентов, чрезмерно много принимающих обезболивающие средства при других болевых синдромах (суставной боли, боли в пояснице, тазовой боли), лекарственно-индуцированная цефалгия не развивается[2].
Анализ эпидемиологических исследований большой популяции больных с хронической головной болью показал, что в 66% случаев пациенты исходно страдали мигренью, в 27% — головной болью напряжения и в 7% — смешанными и другими формами первичных головных болей, в том числе новой ежедневно персистирующей головной болью[3]. Отличие ЛИГБ от лекарственной зависимости состоит в существовании одной из первичных форм цефалгий, ставшей причиной регулярного бесконтрольного применения обезболивающих средств и развития лекарственного абузуса[4].
Распространенность ЛИГБ составляет 1–1,8% в общей популяции, чаще встречается у женщин 40–50 лет (до 5%); среди всех пациентов с ЛИГБ доля женщин составляет от 62 до 92%[1].
ЛИГБ — одна из самых частых форм головной боли у пациентов, обращающихся в специализированные клиники головной боли. Так, в европейских клиниках головной боли количество больных с ЛИГБ — 30% от всех обратившихся за помощью, а в клиниках головной боли США — более 50%. В соответствии с данными эпидемиологических исследований, ЛИГБ занимает третье место среди заболеваний, сопровождающихся головной болью, уступая только головной боли напряжения и мигрени[5]. Следует отметить, что это тяжелый, дезадаптирующий вид головной боли, качество жизни пациентов с данным диагнозом значительно хуже, чем у лиц с эпизодическими головными болями[6].
К факторам, предрасполагающим к хроническому течению цефалгии и, как следствие, к увеличению дозы и кратности приема обезболивающих, относят женский пол, низкий социально-экономический статус, ожирение (ИМТ > 30 кг/м2), тревожно-депрессивные расстройства, апноэ во сне и другие нарушения сна, неправильный прием препаратов для купирования головной боли в момент приступа и др. Склонность к злоупотреблению также часто развивается у пациентов с семейным анамнезом головной боли, когда с детского возраста они наблюдали чрезмерное употребление анальгетиков старшими членами семьи и используют этот опыт поведения[7, 8].
Злоупотребление психоактивными лекарственными средствами и зависимость — хорошо известные проблемы, которые имеют физические, психологические и социальные последствия. Злоупотребление лекарствами подразумевает их преднамеренно неправильное использование или чрезмерное употребление, несмотря на вред[2]. По определению МКБ-10, синдром зависимости — это «сочетание физиологических, поведенческих и когнитивных явлений, при которых употребление вещества или класса веществ начинает занимать первое место в системе ценностей индивида. Основной характеристикой синдрома зависимости является потребность (часто сильная, иногда непреодолимая) принять психоактивное вещество, алкоголь или табак». В Diagnostic and Statistical Manual of Mental Disorders V предложено объединить злоупотребление психоактивными веществами и синдром зависимости в одно расстройство с выделением степени его тяжести[9].
Стоит отметить, что в диагностических критериях ЛИГБ не имеют значения характеристики головной боли, ее интенсивность, вид лекарственного препарата или его дозировка. Учитывается только количество дней использования симптоматического средства для облегчения цефалгии и наличие исходно головной боли у пациента (до избыточного применения лекарственных средств). Между тем фенотипы ЛИГБ различны и, по-видимому, зависят от типа исходной первичной головной боли.
Лечение ЛИГБ включает в себя отмену «виновного» препарата. Согласно клиническим рекомендациям РФ от 2021 года[5], есть два метода отмены: полная и частичная, когда пациенту разрешается принять до 2 доз анальгетика в неделю. M. Nielsen и соавт. исследовали 72 пациентов с ЛИГБ на протяжении 12 месяцев, наиболее быстрое улучшение, по шкалам оценки головной боли (Headache Under-Response to Treatment, HURT) и качества жизни (World Health Organization Quality of Life Instruments-BREF — краткий опросник ВОЗ для оценки качества жизни), отмечено в группе полной отмены анальгетика[10].
Следующими, но не менее важными аспектами являются подбор препарата для профилактической терапии исходного типа цефалгии, поведенческая, психотерапия. Необходимость проведения детоксикации, применения глюкокортикостероидов в комбинации с сульфатом магния до сих пор остается дискуссионной, не относится к рекомендациям с уровнем убедительности А.
В момент резкой отмены анальгетика, вызвавшего ЛИГБ, возможен «рикошетный» синдром отмены, проявляющийся тяжелой фоновой головной болью, тошнотой, рвотой. В данном случае допускается использование анальгетического препарата другой группы для купирования головной боли периода отмены (не более 2 доз в неделю), противорвотных средств, анксиолитиков. Эффективность терапии оценивается спустя 3 месяца от начала лечения.
«Золотым стандартом» оценки эффективности лечения является уменьшение частоты и/или интенсивности головной боли на 50% от исходных характеристик. Однако лечение ЛИГБ — клинически трудная задача, так как обычно подобные пациенты имеют множественные психические коморбидные нарушения, зависимость от лекарственных препаратов, у них отсутствует самоконтроль[11, 12]3.
Цель исследования: оценить закономерности формирования ЛИГБ, эффективность терапии, а также сравнить две группы пациентов с хронической мигренью и злоупотреблением симптоматическими средствами: с ЛИГБ и без нее.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включены 20 пациентов от 18 до 75 лет с установленным диагнозом хронической мигрени и чертами злоупотребления симптоматическими средствами, поступивших в Клинику нервных болезней им. А.Я. Кожевникова в период с ноября 2021 по март 2022 года. Дополнительными критериями включения были возраст от 18 до 75 лет и наличие письменного информированного согласия пациента на участие в исследовании. Критерии исключения — возраст менее 18 лет и более 75 лет, а также наличие сопутствующей тяжелой соматической или психиатрической патологии в стадии декомпенсации, выраженные когнитивные нарушения, препятствующие полноценному клиническому исследованию. Период наблюдения составил 3 месяца.
Всем пациентам диагноз установлен в соответствии с МКГБ-3, подробно проанализированы жалобы, анамнез заболевания, социо-демографический статус. У больных проводилась оценка влияния головной боли на повседневную активность (Headache Impact Test 6), влияния мигрени на повседневную активность (Migraine Disability Assessment), времени, потерянного из-за головной боли (Headache-Attributed Lost Time), качества жизни при мигрени (Qualité de Vie et Migraine), уровня катастрофизации боли (шкала Pain Catastrophizing Scale). Кроме того, определяли эффективность предшествующего лечения головной боли (HURT), приверженность к лечению (Morisky Medication Adherence Scale 8), общую эффективность терапии мигрени (Migraine Treatment Optimization Questionnaire 5).
С целью выявления особенностей формирования ЛИГБ проанализированы клинико-психологический статус пациентов и склонность к зависимости (Лидский опросник зависимости, шкала импульсивности Барратта 11, шкала обсессивно-компульсивных расстройств Йеля — Брауна, Торонтская алекситимическая шкала 26, шкала ситуативной и личностной тревожности Спилбергера — Ханина, Госпитальная шкала тревоги и депрессии, Patient Health Questionnaire 15 — оценка сопутствующих физических симптомов), а также качество жизни и работоспособность (Migraine Work and Productivity Loss Questionnaire — анкета по эффективности работы с мигренью и потере производительности труда, World Health Organization Quality of Life Instruments-BREF — краткий опросник ВОЗ для оценки качества жизни) и возможные когнитивные нарушения (Краткая шкала оценки психического статуса, Батарея лобной дисфункции).
Пациенты были осмотрены на 1–3-й, 6-й и 10-й дни наблюдения. Проведены также телефонные интервью с ними через 3 месяца после завершения стационарного лечения.
Анализировался паттерн головной боли в момент поступления, в момент проведения детоксикационной терапии и начала профилактического лечения, а также спустя 3 месяца после начала терапии, оценивались возможные причины отказа от препарата и возможная приверженность к лечению.
РЕЗУЛЬТАТЫ
Проведен клинический анализ пациентов на момент первичного осмотра в стационаре и через 3 месяца наблюдения. Их средний возраст составил 36,75 года. Динамика характеристик цефалгического синдрома представлена в таблице 1.
Таблица 1
Анализ динамики характеристик головной боли пациентов с лекарственно-индуцированной головной болью
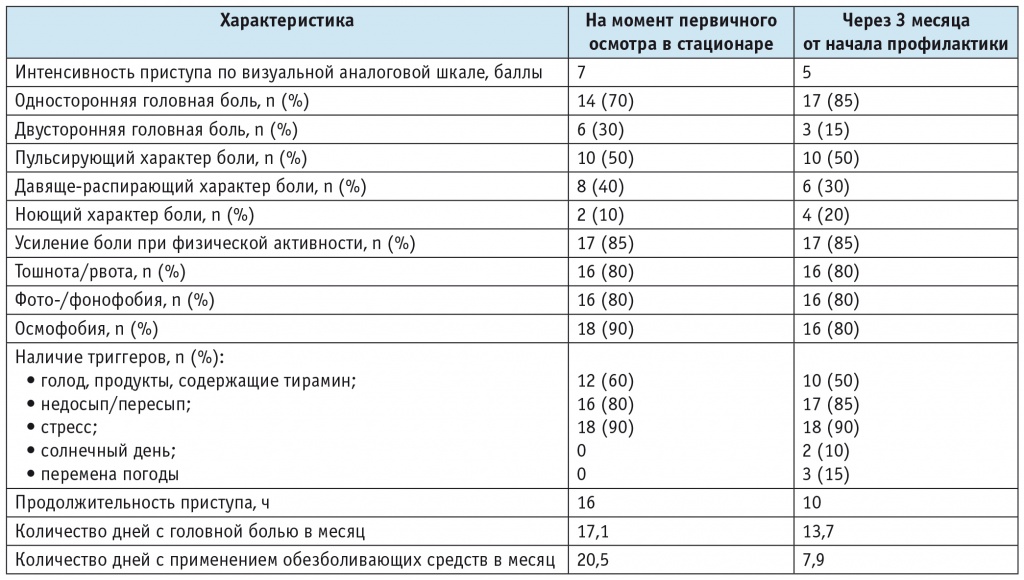
Как видно из таблицы, за 3 месяца наблюдения интенсивность приступа головной боли снизилась на 2 балла по ВАШ, а продолжительность — в среднем на 6 часов, количество дней с головной болью уменьшилось в среднем на 3,4 дня, количество дней с применением обезболивающих средств в месяц — на 12,6 дня, пациенты стали лучше отслеживать свои триггеры цефалгии путем ведения дневника головной боли.
Можно судить о том, что у пациентов начала уменьшаться фоновая головная боль, а приступ цефалгии стал принимать исходные мигренозные черты: через 3 месяца в 85% случаев преобладала односторонняя головная боль по сравнению с 70% при первичном осмотре.
Длительность злоупотребления анальгетиками варьировала от 1 года до 13 лет и составила в среднем 3,55 года.
У 5 (25%) участников исследования в возрасте от 19 до 25 лет не было фоновой головной боли. Как правило, фоновая головная боль преобладала у больных более старшего возраста, при более длительном стаже злоупотребления симптоматическими средствами, в частности комбинированными анальгетиками.
Период от дебюта мигрени (по ретроспективному анализу жалоб) до начала злоупотребления и хронизации цефалгии — в среднем 6,6 года, до постановки диагноза ЛИГБ — 13,2 года.
Из 20 пациентов ранее обращались к неврологу по месту жительства более 3 раз 9 человек, 5 ранее получали профилактическую терапию хронической мигрени препаратами с доказанной эффективностью при хронической головной боли, а 10 (50%) — без доказанной эффективности.
Сопутствующий хронический болевой синдром наблюдался у 14 (70%) человек, катастрофизация боли, когнифобия и цефалгофобия — у 16 (80%), тревожно-депрессивные расстройства — у 17 (85%), алекситимия — у 17 (85%), склонность к импульсивному поведению — у 6 (30%). Данные о влиянии головной боли на функционирование, качество жизни, эффективности и приверженности к терапии мигрени, а также характеристики ЛИГБ представлены в таблице 2.
Таблица 2
Данные анкетирования пациентов на момент осмотра в условиях стационара
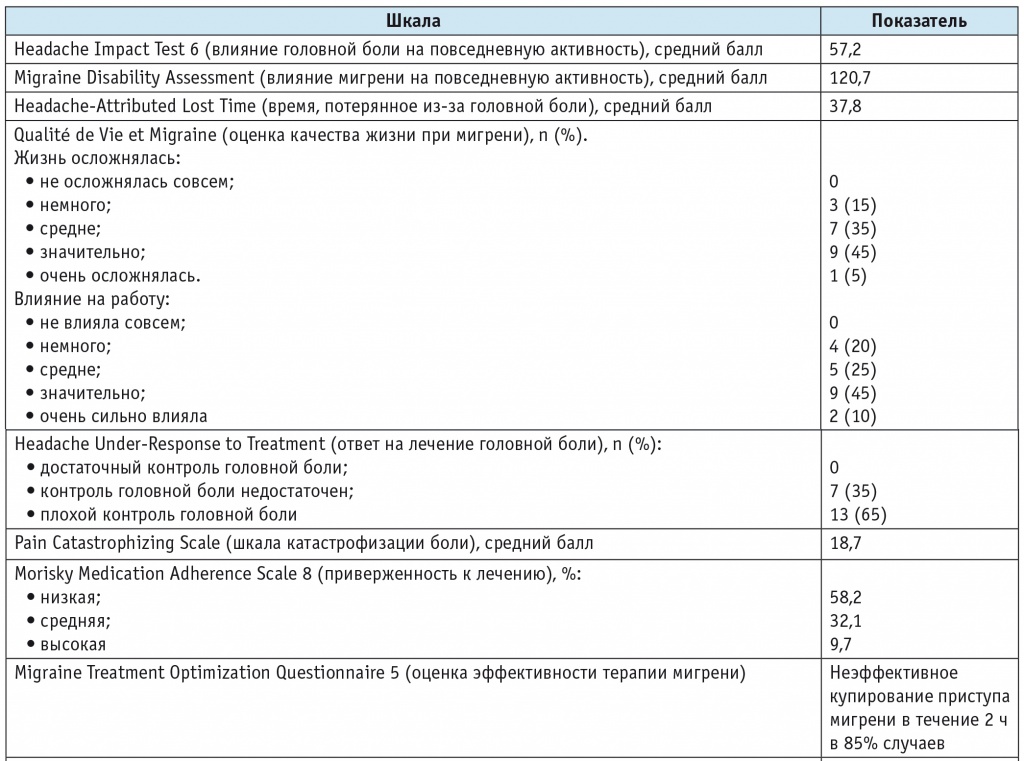
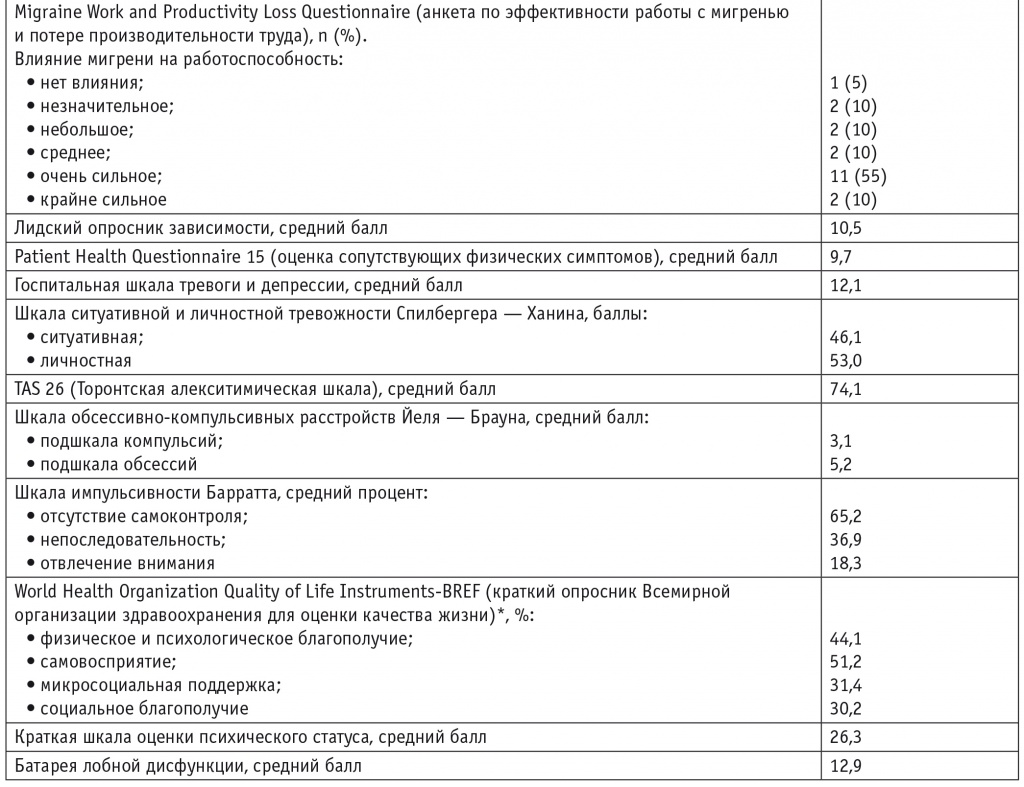
* Визуальная оценка качества жизни, максимум — 100%.
Как видно из таблицы, включенные в исследование пациенты исходно испытывали выраженное ограничение повседневной активности из-за головной боли и ее существенное влияние на жизнь, у них были плохой контроль и низкая эффективность купирования приступов цефалгии, низкая приверженность к лечению и катастрофизация боли. Больные также имели тревожные расстройства, алекситимию, склонность к импульсивному поведению, черты умеренной степени зависимости от симптоматических препаратов для купирования головной боли. При оценке когнитивного статуса выявлены умеренные когнитивные нарушения и умеренная лобная дисфункция.
Наличие сопутствующих зависимостей: курение — у 9 (45%) (индекс курильщика — 9), употребление алкоголя — у 2 (10%), применение ранее наркотиков — у 7 (35%), игромания — у 4 (20%) человек. Анальгетик принимали «впрок» для предотвращения головной боли из-за страха/тревоги перед возможной болью 13 (65%) участников.
Среднее количество дней нетрудоспособности в год у 15 работающих пациентов составило 21,3. Однако у тех больных, которые не обращались в медицинские организации для получения листка нетрудоспособности, развивались элементы презентеизма (дни присутствия на рабочем месте со снижением функционирования) и абсентеизма (дни отсутствия на работе) в 100% случаев.
Всем пациентам проводилась терапия в соответствии с рекомендациями Российского общества по изучению головной боли от 2022 года[7], в которых указано, что необходимы отмена «виновного» анальгетика и ограничение приема препарата с обезболивающим действием из другой группы (не более 2 дней в неделю) (в обоих случаях уровень убедительности рекомендаций А); рекомендованы и проведение детоксикации с использованием глюкокортикостероидов и прием противорвотных средств по потребности (уровень убедительности рекомендаций С). Согласно клиническим рекомендациям с уровнем убедительности В, требуется назначение профилактической терапии мигрени, причем при сочетании хронической мигрени и ЛИГБ предпочтение следует отдавать топирамату в дозе 100 мг в сутки, ботулиническому токсину типа А по протоколу PREEMT, введению моноклональных антител (фреманезумаба, эренумаба) подкожно.
В момент отмены «рикошетные» симптомы и синдром отмены развились у 14 (70%) человек. Детоксикационная терапия (дексаметазон 4–8 мг на 200 мл физраствора и магнезия 10% 25 мл № 10) проводилась у 12 (60%) больных.
Продолжали вести дневник головной боли и отслеживать динамику сопутствующих симптомов 16 человек. Во-первых, это влияло на оценку эффективности профилактики, а во-вторых, косвенно свидетельствовало о приверженности больных к лечению и отслеживанию своих симптомов.
Для профилактики у данных пациентов использовались метопролол в 6 (30%) случаях, топирамат — в 2 (10%), амитриптилин — в 30%, венлафаксин — в 30%. Спустя 3 месяца от начала терапии наибольшее снижение частоты и интенсивности головной боли отметили пациенты при приеме амитриптилина в дозе до 50 мг, венлафаксина в дозе до 150 мг.
Ограничения назначения и приема топирамата, несмотря на то что он имеет уровень доказательств А в качестве профилактического средства от мигрени, связаны с побочным действием в виде общей заторможенности. Четверо (20%) работоспособных пациентов вынуждены были отменить препарат и начать прием другого средства для профилактического лечения.
Ограничение приема антидепрессантов вызвано в первую очередь стигматизацией и убеждением, что эти препараты должны принимать только пациенты с грубой психиатрической патологией. Несмотря на положительный эффект от приема амитриптилина/венлафаксина в течение 3 месяцев, 3 (15%) человека не преодолели психоэмоциональный барьер и отменили препарат. Среди них только 1 больной был согласен начать профилактическую терапию препаратом из другой группы. Два (10%) пациента не согласились на прием превентивной терапии, по данным дневников головной боли, они отметили учащение приступов головной боли, которые хорошо купировались приемом напроксена в дозе 500 мг в сутки.
Ограничение назначения моноклональных антител (фреманезумаба, эренумаба), а также ботулинического токсина типа А обусловлено ценой препаратов.
Следует отметить, что среди 11 пациентов молодого возраста (от 20 до 39 лет) у 9 человек отсутствовала ЛИГБ, несмотря на значимое злоупотребление анальгетиками.
ОБСУЖДЕНИЕ
Обращает на себя внимание факт, что 11 (55%) больных не знали о исходном диагнозе мигрени, 16 (80%) пациентов, злоупотреблявших анальгетиками, несмотря на их неэффективность, не знали о наличии имеющихся специальных средств для купирования приступа головной боли — триптанов, а 90% не были информированы об ограничении приема простых анальгетиков до 15 доз в месяц, а комбинированных анальгетиков/триптанов — до 10 доз в месяц.
У 9 (45%) пациентов из Москвы, Московской области и близлежащих областей на руках имелись не менее трех результатов МРТ головного мозга, в том числе в режиме магнитно-резонансной ангиографии и контрастного усиления, ЭЭГ, ультразвуковой доплерографии брахиоцефальных артерий, они регулярно пользовались услугами мануального терапевта и остеопата, не менее 2 раз в год получали курс сосудистых и ноотропных препаратов. У них наиболее часто встречались следующие диагнозы: вегето-сосудистая дистония, цервикокраниалгия, сосудистая головная боль, дисциркуляторная энцефалопатия, цереброваскулярная болезнь, хроническая ишемия головного мозга с цефалгическим синдромом. В данной группе пациентов обращали на себя внимание выраженное болевое поведение и катастрофизация боли, цефалгофобия, когнифобия.
Тревожность и убежденность пациентов, что имеющаяся головная боль связана с сосудистой патологией (например, с непрямолинейностью хода позвоночных артерий, по результатам ультразвуковой доплерографии брахиоцефальных артерий), по всей видимости, смещали фокус внимания на внутримышечное или внутривенное введение ноотропа. Наибольшие трудности возникли в группе больных с длительным анамнезом злоупотребления (в среднем 7,3 года), сопутствующими зависимостями — курением более пачки сигарет в день. Как правило, такие пациенты, зачастую неосознанно, принимали анальгетики «впрок», т. е. для профилактики возникновения боли.
Отсутствие ЛИГБ при наличии абузуса чаще наблюдалось в группе пациентов более молодого возраста (от 20 до 39 лет), которые чаще злоупотребляли простыми анальгетиками, имели относительно небольшой стаж мигрени.
ЗАКЛЮЧЕНИЕ
Результаты проведенного исследования позволили сделать несколько выводов.
Необходимо повышение осведомленности терапевтов, неврологов о причинах, закономерностях, методах лечения лекарственно-индуцированной головной боли, а также о факторах риска ее рецидивирования.
Комплаенс пациентов можно повысить путем телефонных интервью, очных консультаций через 1–3 месяца от начала профилактической терапии, подробной беседы о природе заболевания, его доброкачественности, методах профилактической терапии и возможных побочных эффектах препаратов.
При правильном приеме профилактического препарата и соблюдении рекомендаций по ограничению злоупотребления симптоматическими средствами уже через 3 месяца повышается качество жизни больных, головная боль по частоте и интенсивности уменьшается, в среднем на 40–50% улучшаются когнитивные функции
При наличии выраженной психиатрической коморбидности и других зависимостей у пациента нужна работа в группе с психиатром. Немаловажными также являются немедикаментозные методы лечения и самообразование пациента, знания о методах психотерапевтической поддержки (майндфулнессе, таблице автоматических мыслей, когнитивно-поведенческой терапии и др.).
Поступила: 04.04.2022
Принята к публикации: 06.07.2022
________
1 Evers S., Jensen R. Treatment of medication overuse headache — guideline of the EFNS headache panel. Eur. J. Neurol. 2011; 18(9): 1115–21. DOI: 10.1111/j.1468-1331.2011.03497.x; Headache Classification Committee of the International Headache Society (IHS). The international classification of headache disorders, 3rd edition. Cephalalgia. 2018; 38(1): 1–211. DOI: 10.1177/0333102417738202
2 Там же.
3 Всероссийское общество неврологов, Российское общество по изучению головной боли. Мигрень. Клинические рекомендации 2020, 2021 гг.








