ВВЕДЕНИЕ
Зрительной агнозией (ЗА), т.е. нарушением зрительного гнозиса, называют неспособность узнать зрительно представленный объект, несмотря на сохранность элементарных зрительных функций, таких как острота и поля зрения[1–3]. Отечественные авторы выделяют такие виды ЗА, как объектная (или предметная) (ОЗА), пространственная зрительная агнозия (ПрЗА), цветовая, лицевая агнозия (ЛА), или прозопагнозия, симультанная, буквенная агнозия[3].
Объектная ЗА (ОЗА) — отсутствие узнавания объектов окружающей среды[1, 3–5]. Нарушение узнавания может быть вызвано тем, что пациент либо не способен распознать форму объекта по его одномерному контуру[6], либо интегрировать воспринятые детали в целостное изображение[1, 3], либо он не может совершать «ментальный поворот» объекта и воспринимать его с необычной точки зрения[7]. Наиболее грубые случаи ОЗА связаны с неспособностью выделять фигуру из фона, что рассматривается как процесс на самых ранних этапах анализа зрительной информации[8].
ПрЗА называется нарушение распознавания пространственных взаимоотношений между объектами и пространственных признаков отдельных изображений, при сохранности узнавания самих объектов[3]. Разновидностями ПрЗА считаются односторонний зрительный неглект (ОЗН) и «апрактоагнозия»[3].
ОЗН, обозначаемый также как «зрительное игнорирование половины пространства», представляет собой неспособность пациента замечать (при отсутствии специального привлечения внимания) объекты на контралатеральной очагу поражения стороне[3, 9].
«Апрактоагнозия» предполагает сочетание нарушения пространственного восприятия с пространственной апраксией как расстройством пространственно-организованной деятельности, выявляемым, в частности, в тесте на копирование фигур[3].
ЛА — это неспособность узнать ранее знакомые лица или запоминать новые[1, 3–5].
Частота различных видов ЗА при ишемическом инсульте (ИИ) изучена мало, а приводимые сведения противоречивы[10]. Так, F. Rowe и соавт. обнаружили ЗА менее чем у 20% больных в восстановительном периоде ИИ, при этом у подавляющего числа этих больных имелся ОЗН (у 15% всех обследованных ими больных с ИИ)[11]. Однако О. Martinaud и соавт. (2012) выявили ЗА почти у половины больных с инсультами, но при этом следует учитывать, что эти авторы обследовали лишь пациентов с инсультами, развившимися в зонах кровоснабжения задних мозговых артерий, и применяли специальные высокочувствительные к агнозии тесты[10].
В то же время частота встречаемости ЗА и ее связь с другими нейропсихологическими нарушениями в остром периоде ИИ требуют уточнения, поскольку такие сведения позволили бы расширить представления о причинах ограничений жизнедеятельности пациентов с инсультом и способствовать разработке персонифицированного подхода к их нейрореабилитации.
Цель работы — установить частоту встречаемости разных видов ЗА, их сопряженность друг c другом и другими нейропсихологическими нарушениями, у пациентов в остром периоде полушарного нелакунарного ИИ.
Дизайн исследования: исследование являлось ретроспективным.
МАТЕРИАЛЫ И МЕТОДЫ
Обследовано 104 пациента в остром периоде полушарного нелакунарного ИИ, подтвержденного по данным нейровизуализации, всего 38 женщин и 66 мужчин в возрасте 46–86 лет (средний возраст 66,7 [9,4] года). Всем пациентам проведено клинико-неврологическое, лабораторное и инструментальное исследование в соответствии с отечественными клиническими рекомендациями, а также нейропсихологическое исследование по А.Р. Лурия[12]. Дополнительно проводилось углубленное исследование зрительного гнозиса, праксиса и кратковременной зрительной памяти с применением специальных чувствительных стандартизированных тестов.
Для диагностики нарушений памяти использовался «Тест с кубиками Корси» (англ. Corsi Block Tapping Test), в котором врач в определенной последовательности прикасался к размещенным на доске кубикам, после чего пациента просили повторить это действие. В норме человек способен воспроизвести последовательность прикосновений к 4 кубикам и более[13].
Диагностика апраксии рук (всех ее вариантов в целом) осуществлялась с помощью теста «Скрининг на апраксию по методу TULIA» (англ. — The Apraxia Screen of TULIA — AST)[14]. В данном тесте пациенту начислялись баллы за верное копирование жестов или выполнение действий с воображаемыми предметами. Апраксия верхних конечностей устанавливалась, если балл, набранный пациентом при выполнении заданий, составлял менее 9.
Для диагностики лобной дисфункции применялась «Батарея лобной дисфункции» (англ. — Frontal Assessment Battery — FAB)[15].
С целью оценки ранних этапов обработки зрительной информации использован тест «Выделение фигуры из фона» (англ. — Visual Figure-Ground) из «Сборника тестов на зрительно-перцептивные навыки, версия 4» (англ. — TVPS-4)[16]. Пациенту предлагались 18 последовательных заданий, в ходе которых ему необходимо было отыскать заданную форму на одном из нескольких изображений.
Что касается собственно нарушений зрительного гнозиса, то для выявления ОЗА проводился тест «Называние рисунков» (англ. — Picture Naming) из сборника «Бирмингемская батарея распознавания объектов»[17], в котором пациенту предлагалось дать название 18 черно-белым контурным изображениям животных или растений; за каждый верно названный объект начислялся 1 балл. ОЗА диагностировалось, если пациент набирал менее 13 баллов, и при этом клинически у него отсутствовали признаки аномии как нарушения способности именовать узнанные предметы.
Оценка ПрЗА включала тесты на ОЗН и апрактоагнозию. ОЗН диагностировался при помощи теста «Бисекция отрезков» по Шенкенбергу[18], в котором пациенту предлагалось разделить на две равные половины 18 горизонтальных отрезков прямых линий, расположенных на листе бумаги один под другим. Центр 6 отрезков расположен по средней линии листа бумаги, у 6 отрезков центр смещен вправо от средней линии, и у 6 — влево от средней линии. В каждой из этих трех подгрупп имеются отрезки длиной 100, 120, 140, 160, 180 и 200 мм. Оценка теста проводилась с установлением отклонений точки деления отрезка пациентом от истинного центра отрезка для каждого из 18 отрезков. Отклонение считалось положительным, если пациент делил отрезок справа от его настоящего центра и отрицательным, если пациент делил отрезок слева от его центра. Далее вычислялось среднее арифметическое этих отклонений. Зрительный неглект устанавливался, если модуль указанного среднего арифметического отклонений превышал 7 мм[19].
Апрактоагнозию диагностировали с применением теста «Копирование сложной фигуры» (англ. — Complex Figure Copy Task) из сборника «Бирмингемский когнитивный скрининг», в котором пациенту предлагалось скопировать черно-белую фигуру, состоявшую из множества элементов. Результаты выполнения задания количественно оценивали по методу J.M. Humphreys и соавт.[20], при этом учитывали правильность копирования как формы, так и расположения каждого элемента фигуры. Максимальная оценка за тест составляла 47 баллов. Точки отсечения результатов применения теста копирования сложной фигуры для диагностики апрактоагнозии составляли 44 балла для пациентов моложе 64 лет, 43 балла для пациентов 65–74 лет и 37 баллов для пациентов старше 75 лет (более низкие значения считались признаком апрактоагнозии)[21]. Важно отметить, что результаты выполнения теста «Копирование сложной фигуры» могли определяться наличием не только апрактоагнозии, но и ОЗН. Для того, чтобы выяснить, являлась ли причиной нарушения копирования сложной фигуры апрактоагнозия либо ОЗН, оценивали симметричность копирования 7 элементов с каждой стороны фигуры по методу M. Chechlacz и соавт.[21]. Апрактоагнозия диагностировалась лишь в случае, когда нарушения копирования были симметричны, а данные теста на бисекцию отрезка исключали ОЗН[21].
ЛА диагностировалась путем применения тестов на лицевой гнозис (узнавание портретов известных личностей) в соответствии с принятыми в отечественной нейропсихологии подходами[22].
ЗА, выявленную по результатам тестирования, мы считали клинически выраженной, если она и вызываемые ей нарушения жизнедеятельности осознавались больным и были заметны окружающим (что выяснялось путем опроса). При отсутствии такого осознания ЗА считалась субклинической.
Клинико-анатомических сопоставлений нарушений зрительного гнозиса в рамках настоящего исследования не проводилось, поскольку данный вопрос весьма сложен и заслуживает отдельного рассмотрения.
Статистический анализ полученных данных проводили с использованием компьютерной программы Statistica 12.0. Нормальные распределения количественных признаков описывались средними значениями и стандартными отклонениями. Определялась абсолютная и относительная (в процентах) частота встречаемости различных неврологических и нейропсихологических симптомов. Различия частот признаков в независимых группах анализировали с вычислением точного критерия Фишера. Корреляцию данных устанавливали по методу Спирмена. Независимые выборки при анализе порядковых данных изучали при помощи непараметрического метода Манна–Уитни. Для установления закономерностей объединения в отдельные группы больных с разными видами ЗА применяли метод кластерного анализа с использованием агломеративного способа k-средних. Для кластеризации использовали количественные показатели выполнения тестов «Называние рисунков», тест узнавания портретов известных личностей, «Бисекция отрезков» по Шенкенбергу, «Копирование сложной фигуры», «Тест с кубиками Корси», тест «Выделение фигуры из фона». Число кластеров пациентов было равно 3.
РЕЗУЛЬТАТЫ
В исследование были включены 104 пациента с очагами острого ИИ, подтвержденными по КТ или МРТ головного мозга. Очаги ишемии в правом полушарии головного мозга имели 40 (38%) пациентов, очаги ишемии левосторонней латерализации — 62 (60%), билатеральное поражение очагов головного мозга — 2 (2%).
Наиболее частыми неврологическими и нейропсихологическими нарушениями у пациентов являлись контралатеральный очагу ишемии гемипарез — у 49 (47%) пациентов, нарушения чувствительности — у 43 (41%), апраксия верхних конечностей — у 9 (9%).
ЗА в целом (клинически выраженная либо субклиническая) диагностирована у 54 (52%) пациентов с острым ИИ. ПрЗА выявлена у 43 (41%) больных (апрактоагнозия — у 21 человек, ОЗН — у 22). ОЗА имелась у 19 (18%) пациентов, а ЛА — у 8 (8%) (рис. 1).
Рис. 1. Частота встречаемости различных видов ЗА пациентов с острым полушарным нелакунарным ИИ
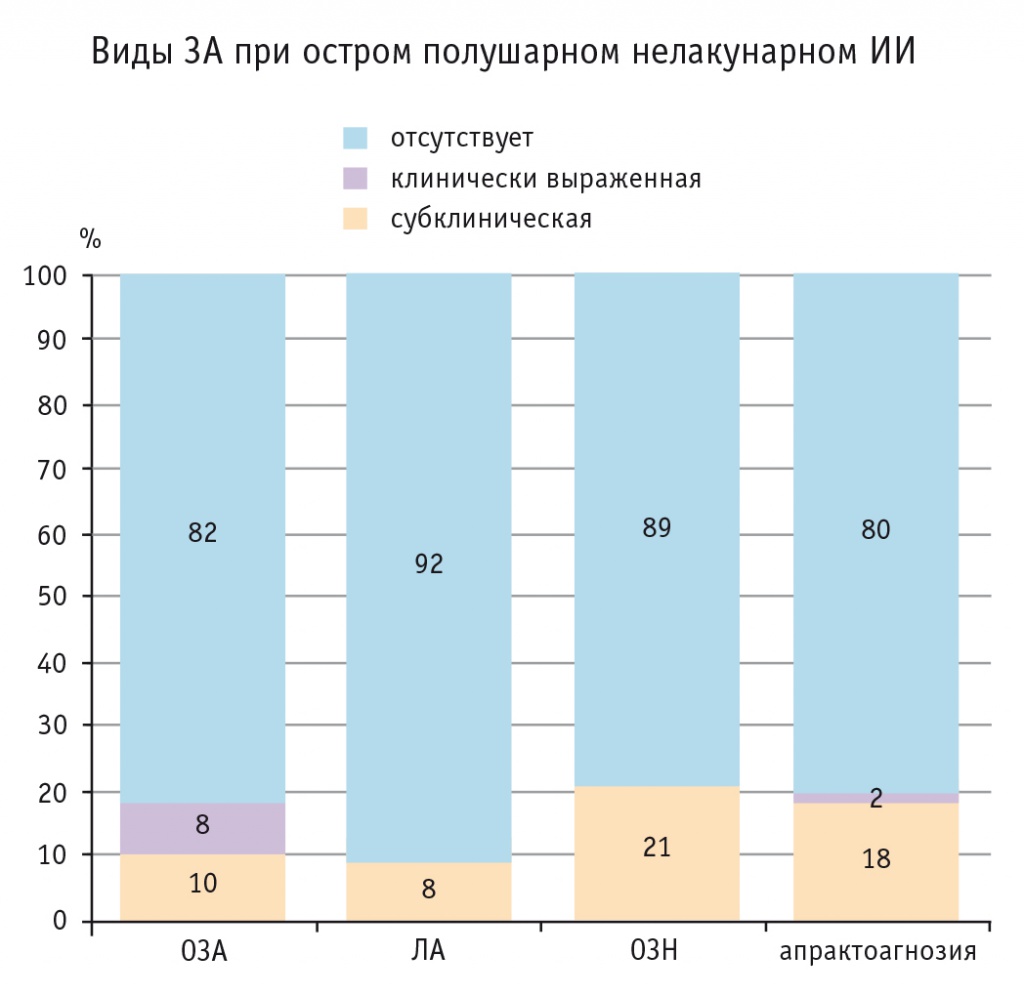
Клинически выраженные нарушения при объектной ЗА (8 из 19, или 42% пациентов) встречалась статистически значимо чаще, чем при ОЗН (0%; p = 0,0011) и чем при апрактоагнозии (2 из 21 или 10% пациентов; p = 0,0065).
Между тем даже те больные, которые осознавали наличие у себя нарушений гнозиса, с трудом вербализовали жалобы, указывая, например, на «перекос в глазах» или «неясность видения». Некоторые больные описывали возникшие у них расстройства таким образом: «Пятерка кажется восьмеркой», «С трудом могу разглядеть экран телефона».
Корреляционный анализ указал на существование статистически значимых (p < 0,05) связей между выраженностью регуляторной (лобной) дисфункции и снижением объектного и пространственного гнозиса, снижением объема кратковременной зрительной памяти и ухудшением выполнения тестов на объектный, лицевой и пространственный гнозис (таблица).
Таблица
Коэффициенты корреляции результатов выполнения тестов на зрительный гнозиc, регуляторную (лобную) дисфункцию и кратковременную зрительную память

* Статистически значимые корреляции (p = 0,05).
Результаты кластерного анализа, проведенного для выделения характерных сочетаний нарушений высших зрительных функций, приведены на рис. 2.
Рис. 2. Кластерный анализ тестов на нарушения высших зрительных функций. Кластер 1 соответствует профилю пациентов без нарушений зрительного гнозиса; кластер 2 — профилю пространственных зрительных нарушений; кластер 3 — профилю нарушений узнавания лиц и объектов. По оси ординат — стандартизированные оценки выполнения тестов пациентами
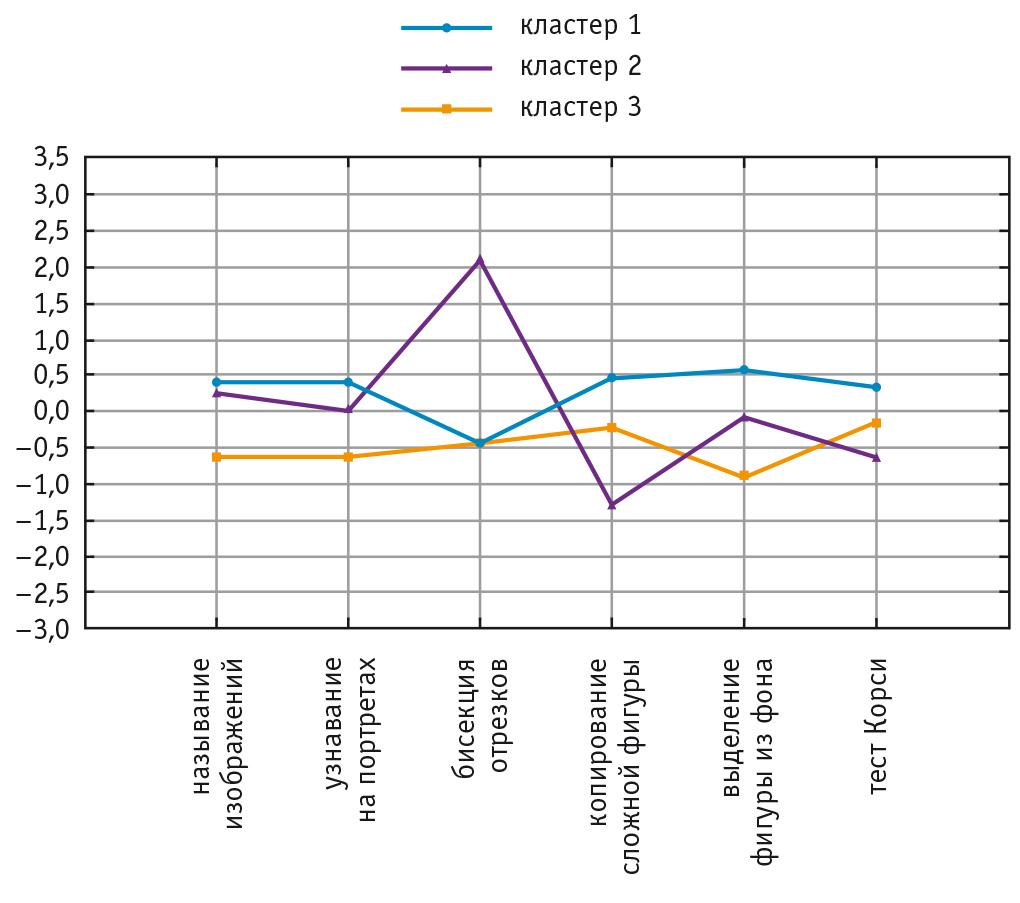
Из заданных трех кластеров, объединенных по сходству результатов выполнения тестов, пациенты первого кластера (n = 60) отличались сохранностью зрительного гнозиса.
Пациенты второго кластера (n = 18) демонстрировали нарушения выполнения заданий на ПрЗА. В частности, результаты «Теста бисекции отрезков» и теста «Копирование сложной фигуры» у них были статистически значимо ниже, чем у больных из первого кластера (p = 0,000077 и p = 0,00000 соответственно), и статистически значимо ниже, чем у больных третьего кластера (p = 0,045141 и p = 0,00000 соответственно). Нарушения кратковременной зрительной памяти у пациентов второго кластера были статистически значимо более выражены, чем у пациентов без зрительной агнозии (p = 0,012280). Пациенты третьего кластера (n = 26) отличались более низкими результатами выполнения тестов на ОЗА и ЛА. Так, показатели теста «Называние рисунков» и теста на узнавание портретов известных личностей у них были статистически значимо ниже, чем у больных первого кластера (р = 0,000477 и р = 0,001674 соответственно). Результаты узнавания портретов известных личностей у больных третьего кластера также были статистически значимо ниже, чем у больных второго кластера (р = 0,029986). Имелась также тенденция к более низким баллам в тестах «Выделение фигуры из фона» у пациентов третьего кластера по сравнению с пациентами второго кластера, но она не достигала статистической значимости.
Статистически значимых различий по выполнению тестов на зрительный праксис между вторым и третьим кластерами не было.
ОБСУЖДЕНИЕ
ЗА диагностирована у 54 (52%) пациентов в остром периоде крупноочагового ИИ супратенториальной локализации. Такая частота хорошо согласуется с данными A.J. Beaudoin с соавт. (2013), установившими, что нарушения зрительного восприятия отмечаются у 49,2% пациентов в первый месяц после инсульта[23], а также результатами O. Martinaud с соавт. (2012)[10], диагностировавшими ЗА у 49% пациентов с ИИ в бассейне задней мозговой артерии. В то же время полученная нами частота значительно выше той, на которую указывают F. Rowe c соавт. (2017), обнаружившие зрительный неглект в 15% случаев ИИ, а нарушения зрительного гнозиса — в 4,6% случаев[11]. Это можно объяснить тем, что F. Rowe и соавт. диагностировали нарушения зрительного восприятия лишь по результатам опроса пациентов и наблюдавших за ними лиц, но не использовали объективных стандартизированных тестов для оценки зрительного гнозиса.
В нашей работе обращала внимание высокая частота встречаемости субклинических форм ЗА. В частности, субклиническая ЗА отмечалась у 58% пациентов с ОЗА, у 90% пациентов с апрактоагнозией и во всех случаях ОЗН. Тот факт, что больные с поражением головного мозга плохо осознают имеющиеся у них нарушения зрительного гнозиса, отмечался и другими авторами[3, 5]. В этой связи мы полагаем, что термин «анозогнозия», использовавшийся ранее лишь в контексте обсуждения дефицита осведомленности пациентов о наличии у них ОЗН, можно экстраполировать на весь спектр ЗА[24]. Причины такой разновидности анозогнозии на сегодняшний день изучены недостаточно[24], но установлено, что отсутствие осознания больными нарушений высших зрительных функций значительно затрудняет своевременное распознавание этих расстройств в клинической практике и снижает эффективность реабилитации пациентов[11].
В структуре ЗА в нашем исследовании преобладала ПрЗА, выявленная у 41% обследованных больных с ИИ. Обращало внимание, что почти половину всех случаев ПрЗА составил ОЗН. Частота встречаемости ОЗН при ИИ в целом составила 21,2%. Эти данные согласуются с данными J. Rengachary с соавт. (2011), согласно которым зрительный неглект в конце острого периода ИИ наблюдается у 25–30% больных[25]. Близкая к этому частота встречаемости ОЗН (29%) отмечена и в исследовании E. Esposito с соавт. (2021), не учитывавшем, однако, давности ИИ[26].
Апрактоагнозия и ОЗА были диагностированы нами у 20 и 18% больных с полушарным ИИ соответственно. Ранее было показано, что эти виды агнозии могут возникать на фоне так называемых «зрительных нарушений низкого уровня», проявляющихся, в частности, в виде затруднения выделения объекта из окружающего его фона[2, 27].
Проведенное исследование указало на то, что результаты выполнения тестов на разные виды ЗА зависят от выраженности регуляторной (лобной) дисфункции. Этот факт представляется вполне закономерным, поскольку хорошо известно влияние функции лобных долей на показатели выполнения нейропсихологических тестов[3]. В то же время нами обнаружено, что ухудшение результатов тестов на ПрЗА, ОЗА и ЛА статистически значимо связано со снижением кратковременной зрительной памяти. Это согласуется с мнением исследователей о важности зрительной кратковременной памяти как для распознавании объектов[28], так и для определения их пространственных взаимоотношений[29].
Кластерный анализ позволил выявить два основных профиля нарушений высших зрительных функций у обследованных нами пациентов. Первый клинический профиль характеризовался нарушением выполнения тестов на ОЗН и копирование сложных фигур, тенденцией к выраженным нарушениям кратковременной зрительной памяти (по результатам «теста с кубиками Корси»). Второй профиль отличался ухудшением выполнения заданий на узнавание объектов среды и человеческих лиц, что сопровождалось затруднениями в таком тесте на относительно простые виды зрительного анализа, как «Выделение фигуры из фона».
Полученные нами характерные для острого ИИ сочетания разных видов ЗА хорошо объясняются с позиции предложенной M.A. Goodale и соавт. теории «двух потоков» распространения зрительной информации[30]. В соответствии с этой теорией зрительные области коры головного мозга, активность которых связана с процессами узнавания пространственных взаимоотношений (путь «Где?»), в анатомическом и функциональном планах частично обособлены от областей, вовлеченных в активность, связанную с распознаванием окружающих объектов и лиц (путь «Что?»). Поражение структур пути «Где?» приводит к возникновению первого профиля нарушений, пути «Что?» — к появлению второго профиля нарушений.
ЗАКЛЮЧЕНИЕ
ЗА встречается у половины пациентов с острым полушарным нелакунарным ИИ, но в подавляющем большинстве своих случаев является субклинической. В ее структуре доминирует односторонний зрительный неглект (21%), «апрактоагнозия» (20%) и ОЗА (18%).
ОЗА, ЛА и ПрЗА статистически значимо связаны с выраженностью дисфункции лобных долей. Все виды ЗА сопряжены также и с нарушениями кратковременной зрительной памяти.
Сочетания разных видов ЗА можно разделить на два варианта («профиля»), первый из которых отличается наличием пространственных зрительных нарушений, а второй — нарушением узнавания объектов и лиц людей.
Клиническая диагностика ЗА требует применения специальных чувствительных тестов и имеет важное практическое значение, поскольку расстройства зрительного гнозиса снижают качество жизни больных с ИИ.
Поступила: 11.07.2022
Принята к публикации: 26.09.2022







