ВВЕДЕНИЕ
Рост числа деструктивных пневмоний (ДП) в последнее время очевиден. Так, в 2021–2022 гг. в категории «общепедиатрические», т. е. не относящиеся к компетенции «узких специалистов»[6], было всего 8 (5%) таких обращений из 167 больных, в 2023 г. — 36 (18%) из 198, за 2 мес 2024 г. — 8 (19%) из 42. Изучение этиологии и патогенеза ДП показало преобладание пневмококков, клиническую рефрактерность к лечению антибиотиками, иммунопатологическую природу метапневмонического плеврита и сопровождающей его «безмикробной» лихорадки. Было обосновано лечение ДП стероидами и показана его эффективность. Эти положения нашли отражение в Клинических рекомендациях, в том числе одобренных Минздравом РФ[1–3] (они доступны в Интернете в руководстве, с наглядными иллюстрациями)[4]. Рекомендуемые щадящие методы лечения значительно сокращают инвазивные вмешательства, рекомендуемые детскими хирургами[5].
Цель исследования: изучить проблемы, с которыми сталкиваются педиатры в процессе ведения пациентов с ДП, и показать возможные пути совершенствования подходов к их лечению.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование основано на анализе всех обращений в НМИЦ здоровья детей по поводу ДП. Нами проводился детальный анализ выписок из историй болезни и амбулаторных карт, рентгено- и томограмм, такой подход позволил оценить, как клинические особенности пневмоний, так и преобладающую тактику педиатров в ведении больных.
В анализ были включены 52 пациента с тяжелой пневмонией по определению Всемирной организации здравоохранения[7], характеризовавшейся фебрильной температурой, кашлем, признаками дыхательной недостаточности (тахипноэ, затрудненным и/или «кряхтящим» дыханием, втяжением уступчивых мест грудной клетки на вдохе) и рентгеновской картиной альвеолярного инфильтрата — консолидации с наличием полостей деструкции. Клинические, рентгенологические и лабораторные данные оценивали в динамике, что позволило проследить течение процесса. Фиксировали стартовые назначения антибиотиков, их замены, а также прием других средств. По каждому больному по месту его лечения отсылали запросы недостающих документов (обычно снимков) и рекомендации.
Исключались больные пневмонией без деструкции либо развившейся на фоне иной патологии (чаще как следствие синдрома аспирации пищи, обычно у детей с неврологическим дефицитом).
РЕЗУЛЬТАТЫ
Возраст больных ДП мало отличался от описанного в литературе: преобладали дети в возрасте до 5 лет (до 1 года — 9 детей, 1–3 года — 18, 4–5 лет — 9, 6–11 лет — 12, 12–17 лет — 4). Значимого преобладания полов в группе не было.
Дебют. Заболевание часто начиналось с 1–3-дневного недомогания с невысокой температурой, кашлем, обычно с диагнозом «острая респираторная вирусная инфекция», что уменьшало настороженность родителей и педиатров, особенно когда температура снижалась за счет приема жаропонижающих средств. Характерные для тяжелой бактериальной инфекции признаки (адинамия, рвота, отсутствие аппетита, отказ от еды и питья) были указаны у 16 больных, но, как правило, не нацеливали на диагноз. Об этом говорят поздние сроки госпитализации: в первые 2–3 дня — всего у 5 детей из 38, на 4–5-й — у 14, на 6–8-й — у 16, после 10-го — у 5. Эти сроки установить было сложно у 6 детей с пневмонией после кори, у 3 — на фоне коклюша, у 1 — скарлатины, у 2 — отита, у 2 — тонзиллита. Трое детей с болями в животе сперва были помещены в хирургическое отделение.
Хотя процесс деструкции развивается в первые дни болезни и определяется во многом вирулентностью возбудителя, позднее начало лечения, если и не является причиной деструкции, несомненно, утяжеляет токсемию и другие проявления воспалительного процесса.
Лечение на амбулаторном этапе. Помимо жаропонижающих и других симптоматических средств, часто использовались ингаляции с беродуалом и будесонидом, не рекомендованные при пневмонии. Видимо, у отдельных больных за обструкцию принимали затрудненное, кряхтящее дыхание, но скорее это связано с распространенным среди педиатров назначением этих ингаляций при любом кашле. Большинство детей получали виферон или гриппферон, отдельным детям назначались арбидол, Анаферон, изопринозин, витамин D3, бронхомунал; ожидание эффекта от этих средств также могло затягивать диагностику.
Антибиотики до госпитализации были назначены 20 больным, у 10 детей это был рекомендованный амоксициллин/клавуланат, но дозы его были либо низкими (ниже 30 мг/кг/сут), либо не указывались в выписках. Не рекомендованный при типичной пневмонии цефиксим получали 7 детей, макролиды — 3; оценить эффект этих препаратов было невозможно.
Госпитализация многих детей осуществлялась в районные или инфекционные больницы, откуда они обычно переводились в учреждения более высокого уровня. Часть детей уже при поступлении помещались в отделения реанимации и интенсивной терапии (ОРИТ) или в хирургическое отделение, многие переводились туда из пульмонологических или педиатрических отделений по показаниям или для проведения плевральной пункции.
Диагноз у большинства больных был поставлен после рентгенографии и звучал как «полисегментарная двусторонняя пневмония», иногда поражение другого легкого выявлялось при компьютерной томографии (КТ) либо при повторных исследованиях, односторонние поражения были единичными (у некоторых больных с уверенностью говорить было сложно). При поступлении после 6–7-го дня болезни многие больные уже имели воздушные полости — буллы, у остальных они появлялись на 2–3-й неделе; обращало внимание то, что некоторые педиатры и рентгенологи считали появление булл не завершением гнойного процесса, а осложнением.
Всем больным наряду с рентгенографией проводилась КТ. Сравнение этих методов показало, что КТ при пневмонии, в том числе ДП, редко дает дополнительную информацию и не влияет на выбор терапии; лишь в отдельных случаях она выявляет интерстициальные изменения, объясняя сохранение одышки. Многим больным за время болезни проводили КТ 2–4 раза, не получая, как правило, дополнительной информации по сравнению с серийными рентгенограммами.
Температуру как индикатор течения болезни и эффекта лечения в выписках отмечали редко, отсутствовали не только температурные кривые, но подчас и упоминания о температуре на протяжении всей болезни. Лишь температура в конце процесса часто являлось причиной обращения за консультацией.
Плевральный выпот при поступлении был зафиксирован у 43 детей. В 30 случаях плеврит имел признаки синпневмонического. Пневмоторакс при поступлении (прорыв гнойного легочного очага в полость плевры) имелся у 5 больных: 4 поступили на 5–8-й день болезни и 1 — на 2-й (?). У 6 детей он развился на фоне лечения. Метапневмонический плеврит при поступлении был у 9 детей, в дальнейшем его развитие было отчетливым еще у 11, у многих его можно было предполагать по увеличению скорости оседания эритроцитов (СОЭ). Однако различие между этими типами плевритов мы нашли лишь в 5 выписках.
Этиологическая диагностика у большинства больных проводилась по посевам из верхних дыхательных путей и мокроты (в 7 случаях с определением резистентности выделенной флоры), что малопродуктивно: лишь у 3 детей был выделен возбудитель (1 пневмококк и у 2 больных с тонзиллитом — гемолитический стрептококк). Остальные анализы выявляли обычную флору (в том числе стафилококк) и лишь путали врача в выборе антибиотика.
Посевы плеврального экссудата и в отдельных случаях крови проводились обычно на фоне антибиотиков, лишь в 1 случае был высеян пневмококк, а из гнойного экссудата (в поздние сроки из дренируемых полостей) по 1 разу — клебсиелла и стафилококк. Стафилококк был высеян из полости перикарда у больного с септической пневмонией. Очевидно, что следует внедрять практику взятия посевов крови до антибактериального лечения, а также осваивать индикацию антигенов в крови и плевральном экссудате (полимеразная цепная реакция, латекс-агглютинация и другие методы).
Лабораторная и инструментальная диагностика у всех больных была достаточной, часто избыточной, что объяснимо тяжестью и торпидностью процесса. Клинические анализы крови (обычно с анализатора с массой незначимых для больного показателей) у большинства больных проводились каждые 2–4 дня, у всех в динамике исследовался уровень С-реактивного белка (СРБ), проводились биохимические анализы, у большинства также определяли содержание прокальцитонина. По показаниями определяли кислотно-щелочное состояние, уровни электролитов, показатели свертываемости.
Выполнялись не только необходимые анализы, но часто также масса других исследований. Рутинная индикация респираторных вирусов, антител к герпетическим и атипичным возбудителям, иногда к широкому кругу инфекций, определение иммунного статуса, «ревматоидные» анализы, как правило, не выявляли значимых для ДП отклонений; создавалось впечатление о стремлении врачей найти с их помощью что-то, объясняющее тяжесть пневмонии.
Существенным дефектом ведения больных являлось некачественное исследование плеврального экссудата (тем более, проводимого далеко не во всех случаях) — без количественного подсчета цитоза, уровня кислотности и глюкозы, что не позволяло определить тип плеврита.
Инструментальные исследования (ультразвуковое исследование, электрокардиографию, эхокардиографию, по показаниям магнитно-резонансную томографию) проводили в полном объеме. Ультразвуковое исследование нередко применяли для наблюдения за динамикой плеврита.
Особенности пневмонии после перенесенной кори. Из 6 детей с ДП на фоне кори 5 были в возрасте 0,5–1,5 года, 1 — в возрасте 4 лет, ни один из них не был привит от кори. Заболевание началось непосредственно после угасания сыпи у 5 детей, через 10 дней — у 1. У 2 детей корь развилась после выписки из больницы, где они лечились от пневмонии (у 1 ребенка — ДП), новая пневмония развилась в ранее непораженных отделах легких. Во всех случаях имела место выраженная дыхательная недостаточность (тахипноэ, сатурация кислорода 88–90%), плеврит, у 3 развился пневмоторакс. Характерным в дебюте была лейкопения ниже 4 × 109/л, сменявшаяся лейкоцитозом. Течение пневмонии было длительным — у 3 детей, возможно, в связи с осложнениями при дренировании, у 2 детей сохранение одышки и температуры было связано с формированием так называемой организующейся пневмонии (по клиническим данным и результатам КТ), потребовавшей длительного курса стероидов; такой исход описан ранее[8].
Лечение. Интенсивная терапия проводилась по показаниям, в том числе в ОРИТ в полном объеме. Практически все больные получали дыхательную поддержку — кислород, в том числе высокодозовый, методом создания постоянного положительного давления в дыхательных путях (Continuous Positive Airway Pressure, СРАР), ряд больных — искусственную вентиляцию легких. У некоторых детей в остром периоде в ОРИТ назначались стероиды в течение 1–3 дней.
Пункции и дренирование плевральной полости проводились по рекомендуемым показаниям у 5 детей с пневмотораксом и у 4 детей с объемным выпотом. Без этих показаний были дренированы 24 ребенка, у 6 из них возник пневмоторакс, возможно, связанный с манипуляцией; у 3 из этих детей развился пиоторакс, по поводу которого проводилось торакоскопическое вмешательство.
Бронхоскопия, вопреки рекомендациям детских хирургов[5], была проведена по особым показаниям 2 больным (подозрение на инородное тело и длительная трахеостома).
Инфузионная терапия проводилась всем больным, по показаниям — коррекция гемостаза. Использовались в основном избыточные объемы инфузий, судя по указанным цифрам (50, 80 и 100 мл/кг в сутки), наличию отеков или необходимости введения фуросемида. Не во всех выписках указывался путь введения, но, судя по данным в тексте и КТ, катетеризация крупных вен не являются редкостью (в 1 случае — с развитием медиастинита). Рекомендуемые объемы в пределах 25–30 мл/кг в сутки упомянуты лишь в 3 выписках.
Симптоматическая и патогенетическая терапия. Характерная для педиатрических стационаров полипрагмазия[9] имела место у большинства больных. И если это может быть необходимым в ОРИТ, то применение нескольких не рекомендованных, не имеющих доказательств эффективности при пневмониях средств вне ОРИТ не может быть оправдано.
Как правило, больные получали флуконазол и пробиотики (бифидумбактерин и др.), хотя 10–20-дневный курс антибиотиков, как правило, не вызывает клинически значимого дисбиоза. Большинство больных получали ингаляции β-миметиков и будесонида, реже эуфиллина, не показанные при характерных для пневмонии рестриктивных изменениях в легких и практически всегда отсутствующей обструкции. Большинство детей получали амброксол в ингаляциях или внутрь, хотя обилие мокроты, тем более затруднения с ее удалением, если и фиксировалось у отдельных больных, то было в виде кратковременного эпизода при опорожнении полостей деструкции. Совершенно не оправдана «гастропротекция» (омепразолом или фамотидином).
Представление о связи тяжелой пневмонии со «слабостью иммунитета» служило причиной частого назначения внутривенного иммуноглобулина (ВВИГ). Эффективный при врожденных иммунодефицитах и ряде аутоиммунных болезней ВВИГ не содержит специфических антител в достаточном количестве, чтобы оказать иммунотерапевтический эффект при сепсисе и других тяжелых бактериальных инфекциях, в том числе пневмонии.
Антибиотики. Основные проблемы при ведении больных, побуждающие врачей обращаться за телеконсультацией, были связаны с антибиотиками; они могли быть сформулированы следующим образом:
– лихорадка и маркеры не снижаются, несмотря на адекватную терапию антибиотиками;
– лихорадка сохраняется и нарастает плеврит, несмотря на снижение уровня маркеров;
– как долго следует лечить остаточные изменения после нормализации состояния больного.
Ответы на эти вопросы требуют учета последовательности процессов при деструкции, в свете которых и производилась оценка терапии антибиотиками.
1. Рекомендованная стартовая монотерапия была начата всего 15 детям (амоксициллином/клавуланатом — у 6, цефтриаксоном — у 9) из 52. Остальным назначали комбинации цефалоспоринов 3–4-го поколения с аминогликозидом (9 детей), ванкомицином (10 детей), макролидом (3 детей), или меропенема с ванкомицином (9 детей), или линезолидом (6 детей). Эффект в виде снижения температуры, уровня маркеров и значительного улучшения общего состояния отсутствовал у всех больных, хотя иногда можно было видеть сокращение периферической зоны инфильтрации в легких. Отсутствие эффекта связано не с резистентностью возбудителя (не «сработал» ни один препарат), а с клинической резистентностью гнойного воспаления: до опорожнения полостей деструкции (как и любого гнойника) температура, уровни маркеров не падают или даже нарастают, что не является показанием для смены стартового препарата.
2. Второй курс антибиотиков был назначен всем 52 больным, у 32 на его фоне состояние улучшилось, у 20 он не улучшил состояние, несмотря на очищение полостей деструкции (появление булл) и снижение маркеров (обычно на 2–3-й неделе болезни). У этих больных обычно появляется серофибринозный — метапневмонический плеврит (хирурги называют его экссудативной фазой плеврита [5]). Его важный признак — нарастание СОЭ, на лихорадку и обилие выпота не действуют ни антибиотики, ни удаление экссудата. Рекомендуется назначать преднизолон (1 мг/кг в сутки) на 4–6 дней, что быстро снижает температуру и СОЭ, позволяя сократить длительность дренирования. Такой курс стероидов получили всего 3 больных, остальным был назначен 3-й курс антибиотиков (фактически новые комбинации тех же препаратов).
3. Отсутствие видимой обратной динамики плевральных и/или деструктивных изменений в легких на 3–4-й неделе лечения (после или на фоне 2-го или 3-го курса антибиотиков) при нормальном состоянии больного, температуре и маркерах было частой причиной обращений за консультацией. Деструктивный процесс завершается (на 2–4-й неделе болезни) формированием множественных воздушных полостей, их обратное развитие с восстановлением архитектуры паренхимы занимает 2–6 мес (рассасывание фибрин на плевре — меньше) и не требует антибиотиков или других средств ускорения, кроме общеукрепляющего режима и лечебной физкультуры при асимметрии грудной клетки. Попытки ускорить обратное развитие плеврита (торакоскопия, дренаж, фибринолиз) лишь усложняют лечение[10], они показаны только при гнойных процессах в плевре со стойким пневмотораксом и осложнениями дренирования.
Для наблюдения за разрешением процесса достаточно 1–3 рентгенографий, тем не менее практически у всех детей проводилась КТ, изменения на которых и были чаще всего поводом для обращения за консультацией.
ОБСУЖДЕНИЕ
Периодическое повышение заболеваемости детей ДП отражает чаще всего появление новых серотипов пневмококков после повышения иммунитета к ранее циркулировавшим. По нашим данным, в 1980–1983 гг. деструкция наблюдалась у 7,4% госпитализированных больных пневмонией детей, а в 2008–2015 гг. — у 16%. Подобное отмечалось многократно в разных странах на протяжении последних 50 лет. И после внедрения пневмококковой вакцинации через несколько лет после резкого сокращения заболеваемости произошел рост деструктивных форм, вызванный невакцинными штаммами пневмококков[11]. В США массовая вакцинация 7-валентной вакциной снизила заболеваемость ДП на 60–70%, но через 3–5 лет их частота выросла. То же повторилось и после перехода на вакцину Превенар 13[12], которая с 2014 г. используется и в России. Рост заболеваемости ДП связывают с серотипами 10А, 11А, 18C 19F, 22F, 23B, 33F, 35B и серогруппой 15, отсутствующими в этой вакцине. Сейчас в разных фазах разработки находятся 15-, 20- и 23-валентные конъюгированные пневмококковые вакцины[13]. Наблюдаемый с 2023 г. рост частоты ДП, вероятно, связан и с ростом заболеваемости корью и коклюшем.
Анализ телеобращений позволяет считать условия для лечения таких тяжелых больных вполне адекватными, в больницах 2–3-го уровня нет недостатка в лабораторном обслуживании, выполняются все необходимые инструментальные исследования, интенсивная терапия и хирургическая помощь представляются без задержек и ограничений. Тем не менее лечение может быть оптимизировано за счет более прицельного ведения больных с сокращением нагрузки антибиотиками и инвазивными вмешательствами, а также с использованием стероидов.
Своевременно назначенные антибиотики снижают выраженность инфекционного токсикоза на фоне формирования очагов деструкции, который может привести к неблагоприятному исходу. В дебюте под их влиянием уменьшается дыхательная недостаточность, но не объемы консолидации. Возможно, развитие пневмоторакса также связано с поздним назначением антибиотиков. То же можно сказать и о синпневмоническом плеврите — ни у одного больного не было прогрессирования изначально гнойного процесса в плевре (т. е. формирования эмпиемы); гнойный процесс имел место лишь у детей с пневмотораксом, они получили необходимые хирургические пособия.
Наш анализ показал неуверенность врачей в преобладании пневмококка при ДП. Ошибочно связывая неэффективность антибиотиков с микробиологической (а не клинической) резистентностью в фазе формирования очагов деструкции (1–2-я неделя болезни), врачи переходили на препараты резерва и их комбинации, которые также не снижали температуру и активность маркеров. И далее на 2–4-й неделе болезни рефрактерность температуры и фибринозного плеврита (имеющих иммунопатологический генез) побуждала врачей к смене антибиотиков и дренированию, а не стероидной терапии, доказавшей свою эффективность[1–4, 14].
Врачи редко связывают клиническую оценку динамики процесса с днем болезни, его фазой, что не восполняется числом и кратностью лабораторных и инструментальных исследований. При этом можно лишь редко встретить оценку эффективности лекарственного или инвазивного воздействия,
Преодоление указанных недочетов требует от врача вдумчивого анализа клинических и лабораторных данных каждого больного ДП, соотнося с ним свои действия. Примером такого подхода может быть следующее наблюдение.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
Ребенок В., 6 лет. Болен 5 дней, температура ≥ 39°С, кашель, рвота, отказ от еды, пьет плохо. Назначенный педиатром амоксициллин за 2 дня эффекта не дал.
День 5-й: при приеме в стационар токсичен, частота дыхания — 32 в минуту, SpO2 — 93%. В легких — укорочение при перкуссии и ослабленное дыхание с 2 сторон, больше справа. На рентгенограмме двусторонняя внебольничная пневмония (рис. 1, а). Диурез снижен, признаков обезвоживания нет (гематокрит 28).
Рис. 1. Рентгенограммы легких больного В., 6 лет, с двусторонней деструктивной пневмонией. Иллюстрации авторов
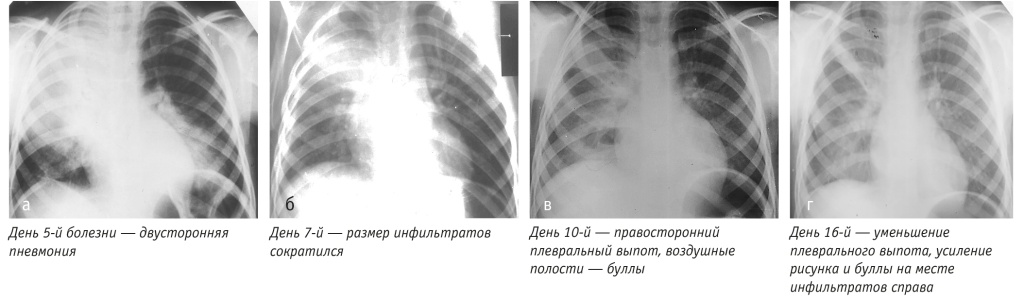
Вероятный возбудитель — пневмококк, что требовало объяснить отсутствие ответа на амоксициллин (гемофильную инфекцию исключали высокие уровни маркеров, вероятность стафилококка при внебольничной пневмонии крайне низкая). Выясняем у матери: ребенку была назначена низкая доза амоксициллина — 28 мг/кг в сутки, недостаточная при пневмококках со сниженной чувствительностью (что вероятно у ребенка, посещающего детское дошкольное учреждение).
Замена амоксициллина на амоксициллин/клавуланат 90 мг/кг в сутки внутривенно, показаний для инфузионной терапии нет. Оральная гидратация, при отказе от питья — через назогастральный зонд.
Дни 6–8-й: состояние больного стабильно тяжелое, сохраняются высокие уровни температуры, лейкоцитоза и СРБ. На рентгеновском снимке — сокращение размеров инфильтратов в обоих легких (рис. 1, б). Пьет достаточно.
Эффект антибиотика частичный, сохранение высоких температуры и уровней маркеров связано, вероятно, с деструктивным процессом. Смена антибиотика не показана.
Дни 8–11-й: состояние больного стабильно тяжелое. На рентгеновском снимке — появление воздушных полостей и плеврального выпота в правом легком (рис. 1, в). Продолжает лихорадить, несмотря на снижение уровней лейкоцитоза и СРБ.
Появление булл и снижение уровней маркеров — признак стихания воспалительного процесса в паренхиме легких, причина сохранения лихорадки — метапневмонический плеврит; о чем говорит и повышение СОЭ. Показания к стероидной терапии.
Дни 13–17-й: на фоне преднизолона быстро нормализовались состояние и аппетит, снизились температура (рис. 2) и СОЭ. Антибиотик прекращен на 13-й день болезни (получал 8 дней). На рентгеновском снимке видно уменьшение плеврального выпота, буллы на фоне усиления легочного рисунка (рис. 1, г). Ребенок выписан на 17-й день болезни, провел 12 койко-дней.
Рис. 2. Температурная кривая больного В., 6 лет, с двусторонней деструктивной пневмонией
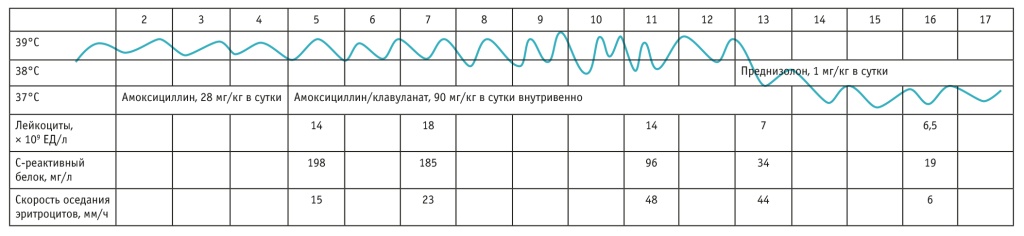
Выводы
1. Анализ телеобращений по поводу ДП показал наличие всех необходимых условий для современной диагностики и лечения этой категории больных. В то же время выявилось слабое знакомство врачей с существующими клиническими рекомендациями,
2. Наиболее значимыми недочетами являются длительное неоправданное применение нескольких курсов терапии резервными антибиотиками, избыточное использование плевральных пункций и дренирования.
3. Слабое знакомство врачей с динамикой деструктивного процесса, в том числе с иммунопатологической его фазой, является причиной недоиспользования стероидов, существенно укорачивающих длительность госпитализации.
ЗАКЛЮЧЕНИЕ
Врачи мало знакомы с клиническими рекомендациями, на это указывает нерациональное применение 2–3 курсов резервных антибиотиков, избыточное использование плевральных вмешательств, недоиспользование терапии стероидами, существенно укорачивающих длительность госпитализации.
Поступила: 07.03.2024
Принята к публикации: 20.03.2024








