Внутрибольничные инфекции (ВБИ), или, в соответствии c современной терминологией, инфекции, связанные с оказанием медицинской помощи (ИСМП), остаются основной причиной смерти и страданий госпитализированных пациентов во всем мире[2]. Частота развития ИСМП в отделениях высокого риска, таких как реанимация, может достигать 40%[20]. Известно, что в экономически развитых странах ВБИ развиваются у 5–12% пациентов, в то время как в развивающихся странах, в том числе в России, этот показатель как минимум в 2 раза выше[4, 23]. При внутрибольничном инфицировании продолжительность и стоимость госпитализации увеличиваются в 3–4 раза, а показатели смертности — в 5–7 раз[3]. Все более актуальной становится проблема роста и повсеместного распространения микроорганизмов, не чувствительных к антибактериальным препаратам. По данным Европейского центра по контролю заболеваемости (ECDC), около 37 000 пациентов ежегодно умирает от инфекций, вызванных микроорганизмами, устойчивыми к действию антибиотиков. Таким образом, развитие ВБИ является важной проблемой, влияющей на безопасность пациентов и качество оказываемой медицинской помощи[23].
У иммунокомпрометированных пациентов, в том числе со злокачественными заболеваниями крови и солидными опухолями, подавление функций кроветворной и иммунной систем связано как с основным заболеванием, так и c воздействием химио- и иммуносупрессивной терапии.
Особую роль в развитии инфекций, вызванных эндогенной флорой, у данной группы пациентов играют нарушение защитных барьеров кожи и слизистых оболочек, а также развитие органной недостаточности — нередкого осложнения интенсивной химиотерапии. Помимо этого, значимым фактором риска является наличие практически у каждого такого пациента различных устройств и систем жизнеобеспечения, таких как центральные венозные катетеры (ЦВК), шунты, трахео- и гастростомы, зонды и др.
ОСНОВНЫЕ ПРИНЦИПЫ ПРОФИЛАКТИКИ ИНФЕКЦИЙ, СВЯЗАННЫХ С ОКАЗАНИЕМ МЕДИЦИНСКОЙ ПОМОЩИ
При планировании и внедрении программ по предотвращению развития и распространения инфекций в стационарах необходимо учитывать основные механизмы передачи инфекционных агентов. Наиболее частый путь — контактный. Различают прямой контакт (телесный, с биологическими субстанциями), когда инфекционный патоген передается напрямую от инфицированного к иммунокомпрометированному пациенту, и опосредованный — через контаминированные предметы, такие как дверные ручки, стетоскопы, игрушки и т. д. Гемоконтактные инфекции могут распространяться во время инвазивных манипуляций через зараженные иглы и другие острые/режущие предметы, а также при попадании биологического материала на кожу и слизистые оболочки. Респираторные патогены передаются воздушным (Mycobacterium tuberculosis, вирусы кори и ветряной оспы) или капельным путем (Bordetella pertussis, вирусы гриппа, аденовирус)[8].
В различных международных рекомендациях приводится ряд мероприятий, позволяющих выполнять профилактику инфекционных осложнений максимально эффективно[19, 24]. С высокой степенью доказательности рекомендованы наличие в палатах системы приточно-вытяжной вентиляции, осуществляющей высокий воздухообмен; фильтров тонкой очистки воздуха High Efficiency Particulate Absorption (HEPA), удаляющих частицы размером ≥ 0,3 мкм; позитивного давления между палатой пациента и коридором (≥ 2,5 Па), а также хорошей герметизации щелей и стыков в помещениях. Важным фактором в профилактике инфекций, в первую очередь инвазивных микозов, является грамотное проведение ремонта в клинике. Необходимо помнить, что в присутствии пациентов нельзя осуществлять никаких пылеобразующих работ. Сотрудники инженерных и технических служб должны всегда согласовывать проведение необходимых работ с эпидемиологической службой. Место реконструкций обязательно нужно отгораживать специальной пылезащитной рамой, поток пациентов должен перенаправляться, им необходимо использовать защитные аэрозольные респираторы (FFP2-типа). После завершения ремонтных работ должна проводиться многократная комплексная уборка с последующим микробиологическим контролем воздуха.
Дополнительным важным условием, предотвращающим возможность инфицирования, является исключение контакта пациентов с такими высококонтаминированными объектами, как цветы, земля, транспортные картонные коробки, животные и птицы. Для детской клиники еще одним фактором передачи инфекций являются игрушки. Не допускаются мягкие плюшевые игрушки, не поддающиеся санитарной обработке. Тряпичные игрушки могут быть только персональными, их необходимо стирать как минимум раз в неделю. Твердые пластиковые игрушки следует обрабатывать дезинфицирующим средством и/или мыть в зависимости от того, играет ими один пациент или нет.
Иммунокомпрометированным пациентам необходимо соблюдать низкобактериальную диету. В частности, пациенты не должны употреблять в пищу сырые, термически необработанные продукты из рыбы и мяса, сырую зелень, немытые овощи и фрукты, ягоды, кисло-молочные продукты, содержащие живые культуры микроорганизмов, а также мед, соевый соус, сухофрукты, орехи, специи. Разрешены любые продукты, прошедшие термическую обработку, мытые фрукты и овощи с толстой кожурой, хлеб и выпечка (в том числе дрожжевые).
Особое внимание должно уделяться личной гигиене. Учитывая высокую вероятность развития мукозита/стоматита, пациенты должны проводить регулярную обработку полости рта, используя только мягкую или силиконовую зубную щетку.
Требования к внешнему виду медицинского персонала и ухаживающих лиц заключаются в необходимости закрывать участки тела с высоким уровнем микробной колонизации, такие как подмышки и ступни ног (нельзя носить майки, необходимо надевать носки); нужно убирать длинные волосы; запрещены формы пирсинга с переходом на кожу со слизистых оболочек губ и носа; нельзя носить шерстяную одежду.
Необходимо подчеркнуть, что сразу при поступлении пациента в стационар лечащий врач должен в доступной форме объяснить больному и ухаживающему за ним лицу все вышеперечисленные особенности питания и ухода.
Медицинский персонал должен осознавать ответственность и значимость своих действий по предупреждению инфекций: не контактировать с пациентами при наличии признаков острых инфекционных заболеваний; в случае возможного контакта с такими инфекциями, как ветряная оспа, корь, краснуха и др., получать консультацию у инфекционистов; соблюдать рекомендованные схемы иммунизации, в том числе от гриппа, дифтерии, кори, гепатита В.
Реализация мероприятий по профилактике инфекций в стационаре возможна только при наличии разработанных и стандартизированных алгоритмов действий (аналогичных англоязычному SOP — Standard Operating Procedure), позволяющих медицинскому персоналу грамотно и профессионально действовать в соответствии с существующими рисками.
ОПЫТ ОРГАНИЗАЦИИ СЛУЖБЫ ИНФЕКЦИОННОГО КОНТРОЛЯ В ФНКЦ ДЕТСКОЙ ГЕМАТОЛОГИИ, ОНКОЛОГИИ И ИММУНОЛОГИИ ИМ. ДМИТРИЯ РОГАЧЁВА
Еще на этапе проектировки и строительства новой клиники ФКНЦ детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева (далее — Центр) были максимально продуманы и внедрены методы профилактики инфекций. Установлена мощная система приточно-вытяжной вентиляции, производящая 280 тыс. кубометров очищенного воздуха в час с HEPA-фильтрацией; в частности, в отделениях трансплантации гемопоэтических стволовых клеток (ТГСК), реанимации и интенсивной терапии (ОРИТ) и в операционном блоке в течение часа происходит двадцатикратный воздухообмен, в остальных отделениях — восьмикратный. Для уменьшения количества пыли в палатах установлены наружные жалюзи, в отделении ТГСК мониторы телевизоров расположены за стеклом бокса. Стены в палатах покрыты специальным экологически безопасным составом, который может подвергаться обработке дезинфицирующими средствами. Все щели в помещениях тщательно герметизированы медицинским силиконом. В системе водоподготовки предусмотрена противолегионеллезная очистка.
В связи с высоким риском развития инфекций у пациентов Центра было решено создать отдел инфекционного контроля (ОИК), особенностью которого является мультидисциплинарный подход к профилактике и лечению инфекций. В отделе работают клиницисты со знанием детской гематологии и инфекционных болезней и госпитальные эпидемиологи. В структуру отдела включена бактериологическая лаборатория, где проводится весь комплекс диагностических исследований: классический микробиологический анализ с современными возможностями идентификации патогенов, включая масс-спектрометрию, иммуноферментный анализ и молекулярную диагностику. Руководит отделом врач-гематолог, прошедший дополнительную специализацию в области клинической микробиологии.
Основным направлением деятельности группы эпидемиологов является создание надлежащего санитарно-эпидемиологического режима в учреждении. В Центре разработано более 70 алгоритмов и регламентов: «Правильная обработка рук», «Порядок работы в ламинарном шкафу», «Принципы работы с центральными венозными катетерами», «Принципы ухода за трахеостомами и гастростомами» и т. д. С целью контроля их выполнения эпидемиологи проводят систематический внутренний аудит с обязательным микробиологическим анализом. Сотрудники ОИК совместно с главной медицинской сестрой Центра регулярно организуют образовательные семинары и мастер-классы с последующим экзаменационным тестированием медицинского персонала.
Целью работы клиницистов ОИК являются изучение спектра бактериальных инфекций и инвазивных микозову пациентов Центра, анализ резистентности микроорганизмов и эффективности терапии. Совместно с лечащими врачами ими проводятся ежедневные осмотры и обсуждения пациентов с инфекционными осложнениями, разрабатываются лечебно-диагностические планы.
С учетом того что все пациенты Центра относятся к группе риска развития тяжелых инфекций, было принято решение о проведении двух скрининговых программ: одна из них направлена на выявление микроорганизмов, продуцирующих β-лактамазы расширенного спектра (БЛРС), вторая — на обнаружение носительства метициллин-резистентного золотистого стафилококка (MRSA). Согласно принятому плану пациенты проходят первичное обследование при госпитализации и в период проведения интенсивного лечения обследуются с периодичностью в среднем один раз в месяц. Результаты скрининговых исследований в дальнейшем учитываются при принятии решения об эмпирической и целенаправленной антимикробной терапии пациентов, а также, в случае необходимости, позволяют своевременно предпринять изоляционные меры.
Важно подчеркнуть, что выявление у пациентов БЛРС не является абсолютным показанием к проведению пероральной деконтаминации. G. J. Lewis и соавт. продемонстрировали, что сокращение использования фторхинолонов приводит к снижению уровня резистентности синегнойной палочки[12]. На сегодняшний день во многих западных гематологических центрах рутинную пероральную деконтаминацию не проводят именно из-за опасности колонизации организма пациентов мультирезистентными патогенами. В Центре также было решено отказаться от широкого профилактического использования антибиотиков, в первую очередь фторхинолонов, и применять их лишь в исключительных случаях, когда в анамнезе у пациента уже была тяжелая инфекция, вызванная мультирезистентными микроорганизмами.
В случае колонизации MRSA пациенты получают деконтаминацию в условиях изоляции, снятие которой проводится только при достижении отрицательного микробиологического результата. Поскольку наиболее частым локусом колонизации является полость носа, для деконтаминации используются интраназальные аппликации 2%-ной мази мупироцина, слизистые полости рта обрабатываются растворами антисептиков, содержащих хлоргексидин, октенидин или повидон-йод.
Проведение скрининга позволило достичь низкой частоты встречаемости MRSA-инфекций в Центре. За 2014 год колонизация MRSA была зарегистрирована у 55 из 1328 (4,14%) пациентов «на входе» в клинику, последующий скрининг, проводившийся в динамике, выявил лишь 8 (0,6%) пациентов с MRSA. Бактериемия, вызванная MRSA, развилась в трех из этих восьми случаев, что составило 1,28% от общего числа бактериемий (n = 234) и 2,17% от грамположительных бактериемий (n = 138). И лишь у одного пациента, которому не проводилась деконтаминация, развился MRSA-ассоциированный сепсис. Полученные данные подтверждают оправданность и эффективность проводимого скрининга, лекарственной профилактики и изоляции пациентов с MRSA.
Мероприятия, направленные на профилактику инфекций, связанных с оказанием медицинской помощи
Для эффективной реализации профилактики инфекций ОИК Центра были выделены следующие основные направления: гигиена рук как основной путь предотвращения ИСМП, дезинфекция поверхностей, стерилизация оборудования, организация изоляционных мероприятий и внедрение системы контроля использования антибиотиков и противогрибковых препаратов.
Гигиена рук. Доказано, что гигиена рук является наиболее значимым фактором в предупреждении развития ВБИ. Обработка рук эффективна при соблюдении ряда условий: 1) при правильно выбранном антисептике, 2) правильной технике и 3) своевременном исполнении. Доказано, что антисептик должен содержать не менее 70% этилового либо 60% пропилового спирта. Техника выполнения обработки рук представлена европейским стандартом EN 1500. Доказано также, что по сравнению с регулярной обработкой рук кожными антисептиками частое мытье рук водой и мылом приводит к более выраженной сухости и, как следствие, к развитию хронических поражений кожи рук[13].
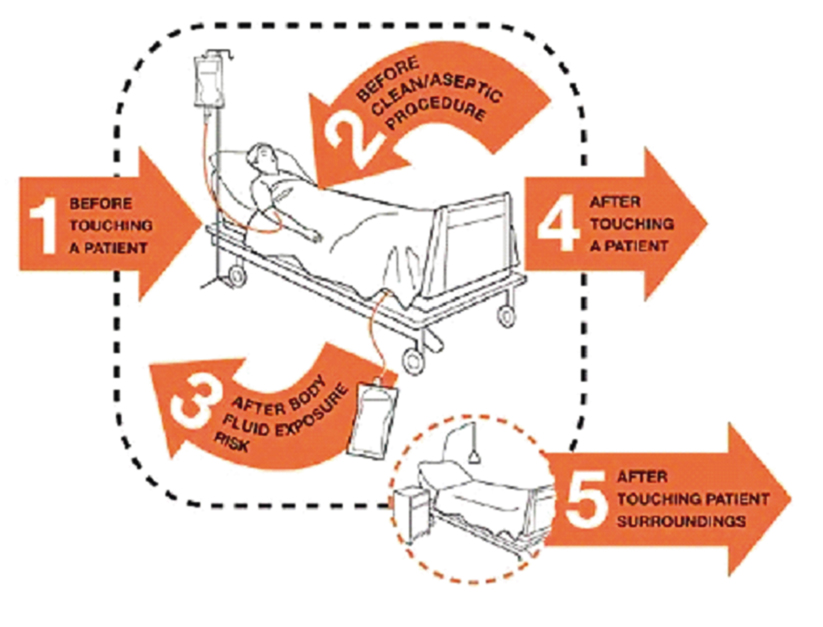
Мытье рук необходимо при видимом загрязнении и в случаях контаминации спорообразующими бактериями, такими как Clostridium difficile. В 2009 г. ВОЗ опубликовала рекомендации по гигиене рук, в которых выделены «пять моментов обработки рук»: 1) перед контактом с пациентом, 2) перед проведением асептических манипуляций, 3) после потенциального контакта с любыми биологическими жидкостями, 4) после контакта с пациентом и 5) после контакта с поверхностями, окружающими пациента (рис. 1)[22].
Рис. 1. Рекомендации Всемирной организации здравоохранения по гигиенической обработке рук[22].
Примечание. 1 — перед контактом с пациентом;
2 — перед выполнением асептических процедур;
3 — после возможного контакта с биологическими жидкостями;
4 — после контакта с пациентом;
5 — после контакта с поверхностями, окружающими пациента
Однако необходимо помнить о том, что существуют факторы, делающие технически грамотную обработку рук неэффективной. В нескольких крупных исследованиях по гигиене рук к таким факторам были отнесены ношение на запястьях часов или браслетов, ношение колец либо накладных ногтей, а также длина свободного края ногтей, превышающая 2 мм[10, 11, 22].
Несмотря на то что гигиеническая обработка рук является краеугольным камнем в предотвращении развития ИСМП, по данным D. Pittet, частота ее выполнения не превышает 50%. В крупных наблюдательных исследованиях выявлены основные факторы, приводящие к низкой выполняемости обработки рук: нехватка времени у персонала, неудобное расположение или малое количество дозаторов кожных антисептиков, боязнь развития поражения кожи рук, уверенность в защитных свойствах перчаток, отсутствие ролевой модели поведения коллег, а также скептицизм и несогласие с рекомендациями[18].
В Центре постоянно ведется обучение медперсонала, пациентов и родителей правильной технике обработки рук, проводятся мастер-классы, созданы методические пособия и видеофильмы. Имеется большое количество мотивирующих плакатов с демонстрацией техники обработки рук. Продумана система расположения дозаторов, в том числе прикроватных, с качественными гипоаллергенными антисептиками. Уделяется внимание не только обработке, но и уходу за кожей рук персонала — имеется достаточное количество специализированных защитных и лечебных кремов. Эта мера является одним из факторов, повышающих выполняемость процедуры.
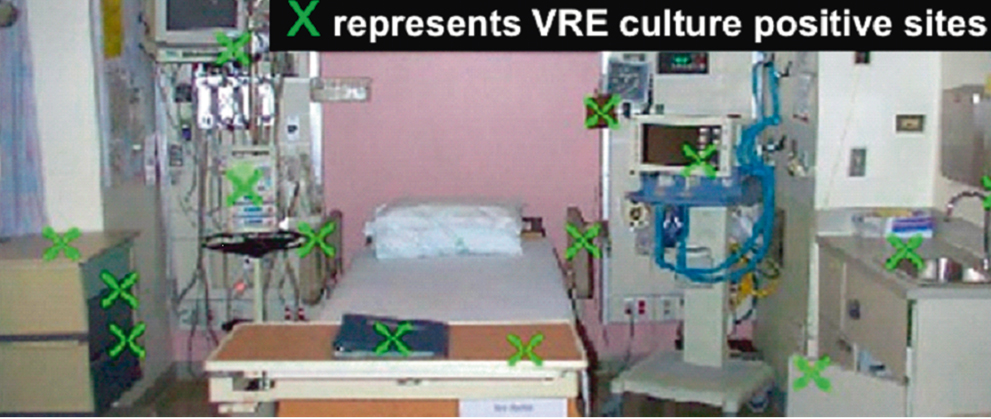
Дезинфекция поверхностей. Очевидно, что обеспечение гигиенической безопасности, а именно удаление патогенной флоры, недопущение ее роста и распространения, требует применения качественных и эффективных дезинфицирующих средств. Наиболее контаминированными объектами являются поверхности, находящиеся в непосредственной близости от пациента, что было показано в исследовании по обнаружению ванкомицинрезистентного энтерококка в палате после выписки пациента (рис. 2)[16]. К объектам большой значимости относятся также предметы, наиболее часто контактирующие с руками: дверные ручки, кнопки и т. д. Поэтому в Центре обработке этих мест уделяется особое внимание.
Рис. 2. Выявление ванкомицинрезистентного энтерококка в палате после выписки пациента[15]
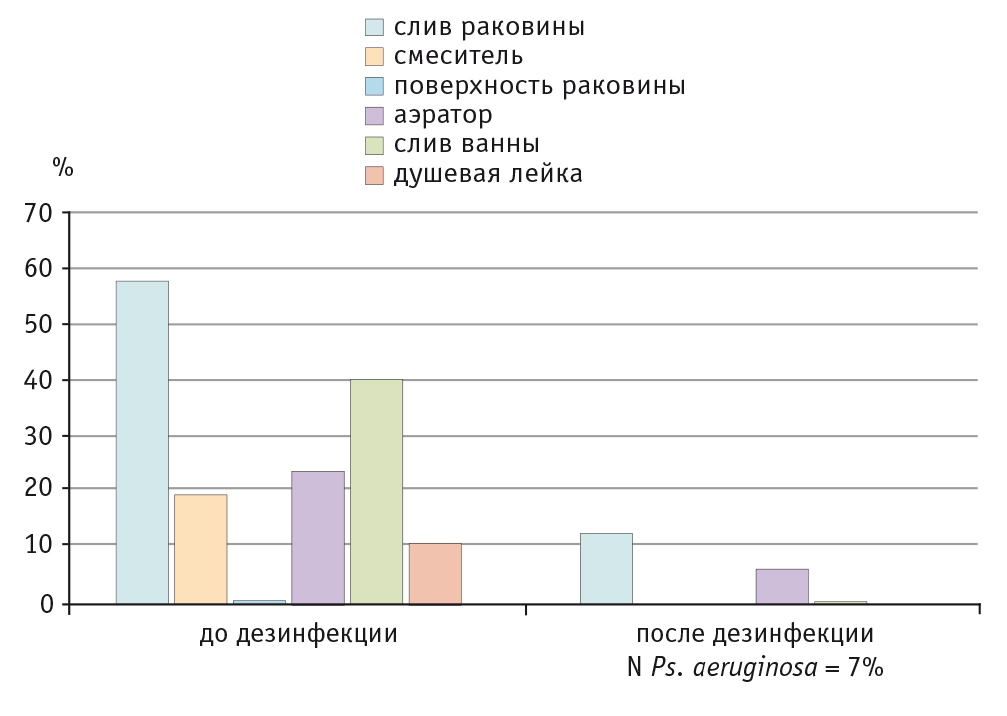
В Центре внедрен наиболее современный метод уборки при помощи систем уборочных тележек и мопов. Применяются двухшаговый метод и метод предварительной подготовки мопов и салфеток с соблюдением принципов цветового кодирования. Сотрудники ОИК разработали все необходимые алгоритмы работы, в том числе касающиеся выбора дезинфектантов и моющих средств, режимов дезинфекции, последовательности проведения уборки, режимов стирки и хранения мопов. В Центре регулярно проводится контроль качества уборки, включающий в себя проверку концентрации рабочих растворов дезинфектантов, использование специальных флюоресцирующих маркеров, микробиологический анализ. Для исследований эпидемиологи делают смывы с различных поверхностей и заборы воздуха аспирационным методом. Микробиологические исследования проводят как в рамках программы производственного контроля Центра, так и по эпидемиологическим показаниям. Такие исследования, в частности, позволили подобрать оптимальные режимы дезинфекции стоков в случае колонизации синегнойной палочкой (рис. 3).
Рис. 3. Снижение контаминации Pseudomonas aeruginosa после проведения дезинфицирующей обработки стоков, % (данные ФНКЦ детской гематологии, онкологии и иммунологии им. Дмитрия Рогачёва)
Стерилизация. В комплексе мер по предотвращению развития ИСМП принципиально важна грамотная организация очистки и стерилизации хирургических инструментов. Для предотвращения риска инфицирования персонала в клинических отделениях Центра проводится только первичная дезинфекция инструментария, вся последующая обработка, включая предстерилизационную очистку, дезинфекцию и стерилизацию, выполняется в центральном стерилизационном отделении (ЦСО).
В целях сохранения стерильности материалов в Центре используют закрытые транспортные тележки, предотвращающие контаминацию. Эпидемиологи Центра проводят тщательный контроль эффективности отмывки специальными тестами — имитаторами загрязненных инструментов. Для стерилизации большей части инструментов используют классический метод паровой стерилизации. Деликатные инструменты (в том числе применяемые в нейрохирургии, офтальмологии), инструменты, не подвергающиеся обычной стерилизации (оптика, дрели, провода и т. д.), обрабатывают методом низкотемпературной плазменной стерилизации. Исключением из принятых правил дезинфекции является обработка эндоскопического оборудования, которая проводится непосредственно в отделении эндоскопии в соответствии с совместимостью тех или иных эндоскопов с различными дезинфектантами.
По виду проводимых манипуляций в Центре установлены три моечных машины: для бронхоскопов, гастроскопов и колоноскопов. Хранение чистых эндоскопов происходит в эндоскопическом шкафу, оборудованном HEPA-фильтрами, что обеспечивает возможность их использования в течение 72 часов. Для транспортировки в другие отделения (ОРИТ, операционный блок) используются специализированные тележки со стерильными одноразовыми пакетами-вкладышами. Применение таких транспортных систем необходимо и для предотвращения обратной контаминации после использования эндоскопа, в отделение эндоскопии его транспортируют для последующей обработки в упакованном виде.
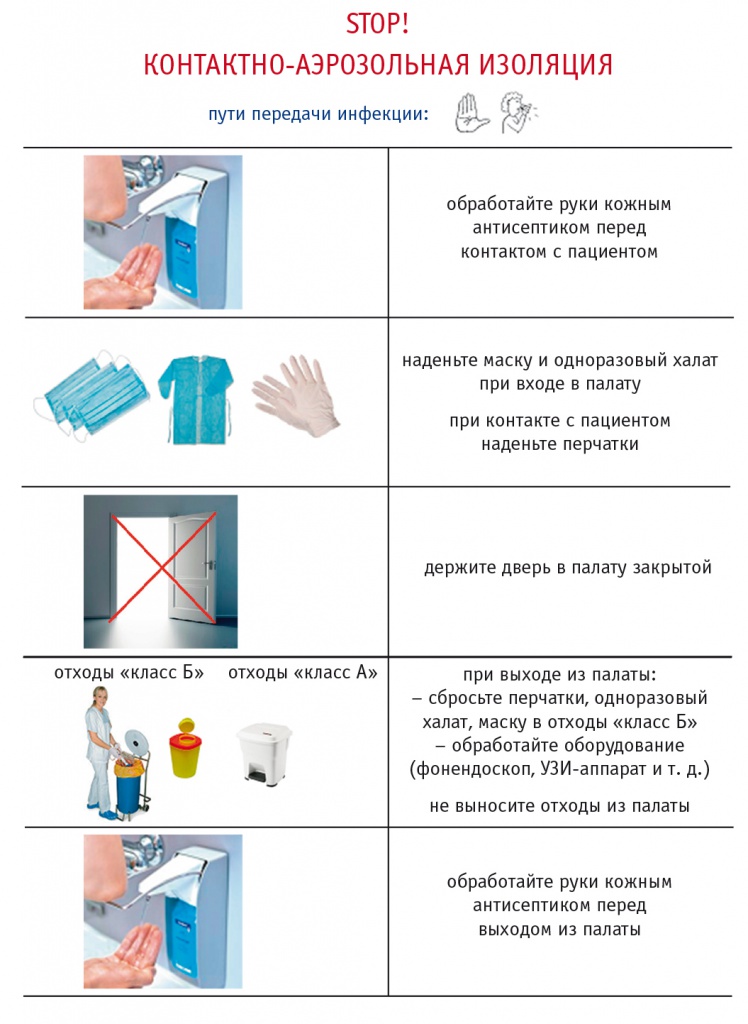
Организация изоляции. Несмотря на весь комплекс эпидемиологических мероприятий, в клинике периодически выявляются пациенты, колонизированные мультирезистентными патогенами. В таких ситуациях помимо стандартных мер предосторожности важно организовать изоляционные мероприятия. В Центре принята изоляция четырех видов: контактная, контактная с необходимостью мытья рук, аэрозольная и контактно-аэрозольная. На дверь палаты изолированного пациента снаружи помещают табличку с указанием требований, предъявляемых к поведению персонала, посетителей и ухаживающих лиц (рис. 4). В тамбур палаты устанавливают столик с необходимым расходным материалом, а также контейнеры для сбора отходов классов А и Б.
Рис. 4. Принципы организации контактно-аэрозольной изоляции (данные ФНКЦ детской гематологии, онкологии и иммунологии им. Дмитрия Рогачёва)
Система оптимизации использования антибиотиков. В последние два десятилетия все более значимой в разных странах становится проблема развития инфекций, вызываемых мульти- и панрезистентными микроорганизмами. ВОЗ определила растущую антибиотикорезистентность как одну из наиболее важных проблем здоровья человечества. В глобальном докладе ВОЗ (2014) отмечено, что весь мир вступает в эру недействительности антибиотиков даже при развитии банальных инфекций[21]. Данная проблема усугубляется крайне ограниченными возможностями фармакологической индустрии в разработке и выпуске новых поколений антибактериальных препаратов[6].
Одна из основных причин формирования резистентности состоит в нерациональном использовании антимикробных препаратов. Международный и национальный опыт свидетельствует о том, что основным мероприятием по сдерживанию антибиотикорезистентности является введение программ по контролю использования антибиотиков[1]. Выполнение этой задачи возможно при осуществлении целого комплекса действий, таких как введение алгоритма эмпирической антибактериальной терапии, внедрение оптимальных схем комбинированной и целенаправленной терапии, контроль своевременной отмены антибактериального лечения, оптимизация интраоперационной антибактериальной терапии. В Центре разработаны алгоритмы эмпирической антибактериальной терапии при развитии фебрильной нейтропении, а также выработаны основные принципы целенаправленной терапии.
В алгоритме эмпирической терапии даны характеристики таких состояний, как нейтропеническая лихорадка, сепсис, различные виды локальной инфекции. Пациенты стратифицированы на группы риска по развитию инфекционных осложнений, принадлежность больного к той или иной группе риска определяет выбор стартовой эмпирической антибактериальной терапии. В алгоритме указаны необходимый объем исследований, условия модификации и своевременной отмены антибактериальной терапии. По прошествии года от момента внедрения алгоритма были изучены результаты его использования. В сравнении с предыдущим годом в Центре отмечено снижение применения таких антибиотиков, как ванкомицин (на 64%), пиперациллин/тазобактам (на 15%), аминогликозиды (на 15%), фторхинолоны (на 7%). В то же время на 25% увеличилось использование цефалоспоринов 3-го и 4-го поколения и на 30% — линезолида.
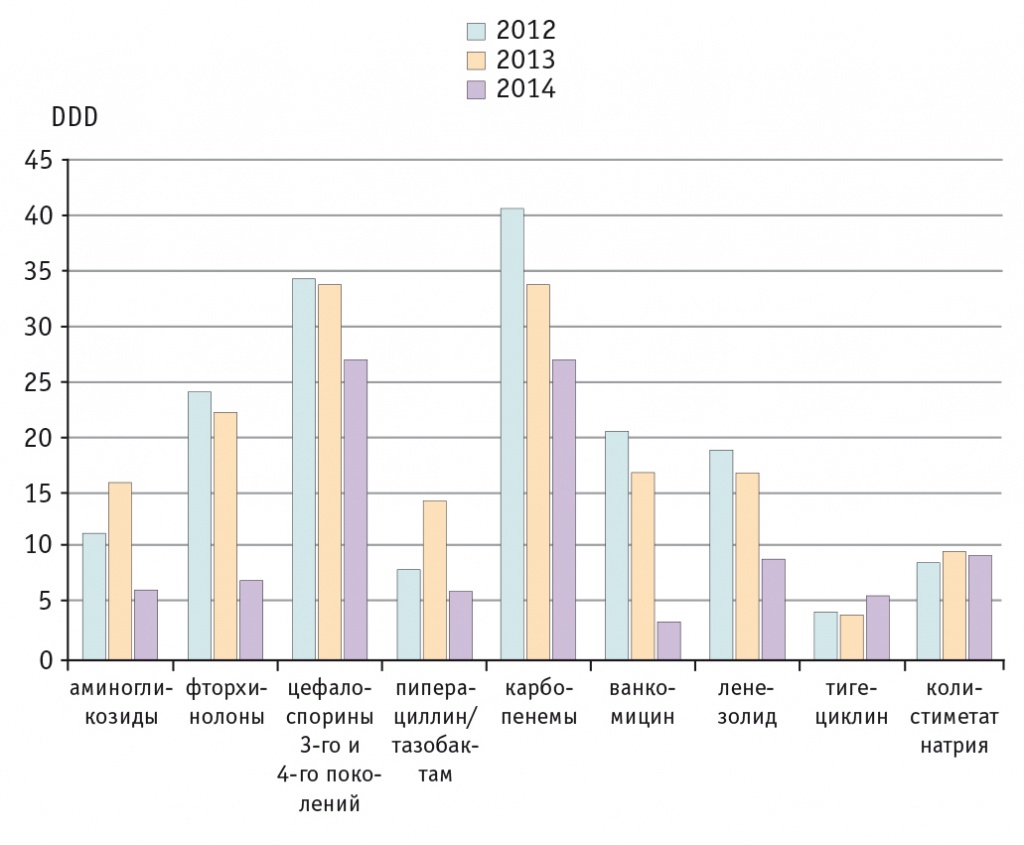
Следует уточнить, что отделения Центра различались по своей приверженности к взаимодействию с ОИК и к применению представленного алгоритма. Наилучшее внедрение системы оптимизации использования антибиотиков продемонстрировало ОРИТ. Несмотря на то что в ОРИТ концентрируются наиболее тяжелые соматические больные как онкогематологического, так и хирургического профиля, в отделении удалось значимо сократить применение антибиотиков всех классов (рис. 5). При этом уровень инфекционной летальности, ассоциированной с развитием грибково-бактериальных осложнений, не повысился.
Рис. 5. Динамика сокращения использования антибиотиков в отделении реанимации и интенсивной терапии, DDD (daily defined dose — установленные суточные дозы) на 100 койко-дней (данные Федерального научно-клинического центра детской гематологии, онкологии и иммунологии им. Дмитрия Рогачёва)
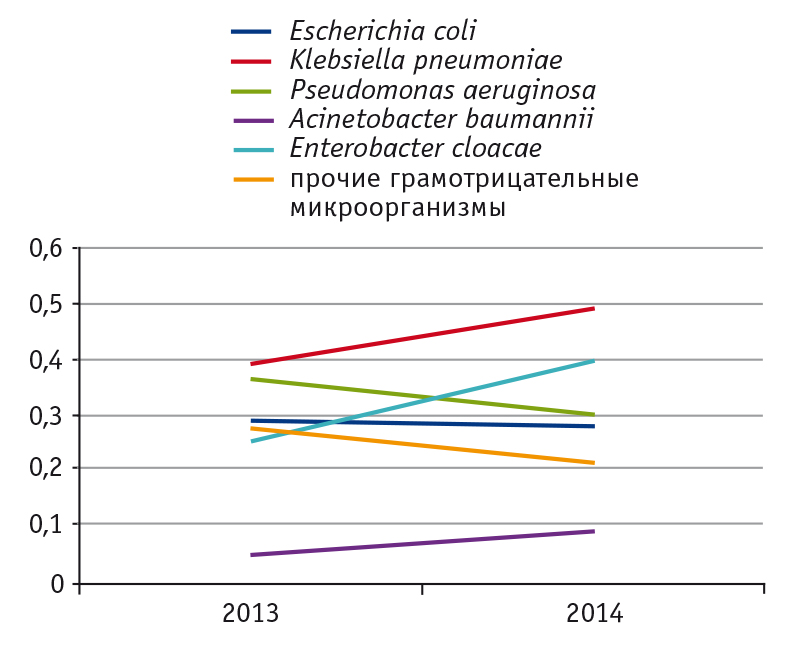
Известно, что показателем, характеризующим эффективность программы контроля использования антибиотиков, является индекс лекарственной устойчивости (ИЛУ), который отображает динамику устойчивости микроорганизмов в зависимости от частоты потребления различных антимикробных препаратов. По истечении года использования алгоритма в Центре был проведен анализ резистентности наиболее значимых грамотрицательных микроорганизмов. Показано снижение ИЛУ таких патогенов, как Pseudomonas aeruginosa, Escherichia coli и ряд других грамотрицательных микроорганизмов (рис. 6). Данные результаты, на наш взгляд, являются достаточно успешными, так как за год до внедрения алгоритма в Центре крайне актуальной была борьба с синегнойной палочкой, единственным препаратом при этом был колистиметат натрия. Однако на графике четко прослеживается рост ИЛУ Klebsiella pneumoniae, Enterobacter cloacae и Acinetobacter baumannii.
Рис. 6. Динамика индекса лекарственной устойчивости (данные ФНКЦ детской гематологии, онкологии и иммунологии им. Дмитрия Рогачёва)
Исходя из вышесказанного, можно сделать следующие выводы:
- сокращение и оптимизация расходов антибиотиков необходимы;
- на примере наиболее тяжелых пациентов Центра, находящихся в ОРИТ, достоверно показано, что это возможно;
- данные мероприятия напрямую влияют на снижение резистентности микроорганизмов и, что немаловажно, позволяют существенно оптимизировать расход финансовых ресурсов.
Перспективные направления работы службы инфекционного контроля
Все вышеперечисленные мероприятия по профилактике и оптимизации лечения инфекционных осложнений являются базовыми и находятся в постоянном развитии и усовершенствовании. В настоящее время запланированы и начинают свою реализацию различные новые протоколы по предотвращению ВБИ.
Эти проекты направлены в первую очередь на катетерассоциированные инфекции кровотока (КАИК), инфекции, связанные с оперативным вмешательством, вентиляторассоциированные пневмонии и инфекции мочевыводящих путей, ассоциированные с наличием мочевых катетеров.
Известно, что наиболее частым видом ВБИ являются КАИК[22, 23]. С целью минимизации частоты их развития в Центре создан алгоритм по уходу за ЦВК, подобраны наиболее эффективные средства дезинфекции и фиксации. Несмотря на очень высокий коэффициент использования ЦВК у пациентов клиники, частота развития КАИК в различных отделениях Центра не отличается от международных данных и на сегодняшний день составляет 1,24–2,51 случая на 1000 катетер-дней[17]. Для дальнейшего снижения частоты КАИК запланирован комплекс дополнительных мероприятий: создание группы сосудистого доступа, проведение тренингов с использованием видеоматериалов и других обучающих программ для врачей и среднего медицинского персонала.
Второй по частоте ИСМП является инфекция области хирургического вмешательства. По данным Центров по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention — CDC), при проведении операций высокого риска частота развития инфекций может достигать 30%, что приводит к увеличению смертности в 2–10 раз[5, 9]. В Центре за 2014 год проведено 1147 оперативных вмешательств, в соответствии с данными CDC, частота постхирургических инфекций могла превысить 300 случаев в год.
Для профилактики инфекций, связанных с хирургическим вмешательством, все операционные клиники Центра оборудованы системой вентиляции с ламинарными потоками воздуха, проходящими через HEPA-фильтры. Перед проходом в операционный блок предусмотрено обязательное переодевание персонала, пациентов и сопровождающих их родителей. Доказанным фактором риска развития инфекции является бритье области оперативного вмешательства, поэтому в Центре применяются специальные атравматичные клипперы с одноразовыми насадками, в том числе для нейрохирургических манипуляций[15]. В связи с тем что, как известно, гипотермия пациента во время операции также является фактором риска развития инфекции, было принято решение при проведении любых оперативных вмешательств использовать системы для интраоперационного обогрева[14].
Особая значимость в Центре придается интраоперационной антибактериальной профилактике. Во внимание принимаются предполагаемая флора с учетом анатомической локализации операции, данные предшествующего скрининга на MRSA и БЛРС и фармакокинетические особенности антибактериальных препаратов. Антибактериальная профилактика может быть успешной только при правильном выборе антибиотика и при его применении в правильной дозе и в правильное время[7].
ЗАКЛЮЧЕНИЕ
Предупреждение развития инфекций, связанных с оказанием медицинской помощи (ИСМП), должно быть приоритетным направлением для любой клиники. Главным мотивирующим фактором, помимо оптимизации расходов клиники, является сохранение здоровья и жизни пациентов. Каждый сотрудник, от директора до представителей младшего медицинского персонала, должен нести индивидуальную ответственность за предотвращение развития ИСМП и являться частью команды инфекционного контроля. При организации грамотного инфекционного контроля нет второстепенных деталей, соблюдая весь комплекс предупредительных мер, можно предотвратить до 50% случаев развития внутрибольничных инфекций.








