В последние годы динамика заболеваемости, ранней инвалидизации и смертности у больных ХОБЛ остается по-прежнему неблагоприятной. Среди причин смертельного исхода ХОБЛ составляет до 85% всех заболеваний органов дыхания [4]. По данным отечественной литературы, в России более 11 млн человек страдают этим заболеванием [10].
Одними из основных причин ранней инвалидизации и смертности при ХОБЛ считаются дыхательная недостаточность и формирование хронического легочного сердца (ХЛС) с последующей декомпенсацией правого желудочка (ПЖ) [2, 11, 15]. Важная роль в развитии гипертрофии, дилатации и декомпенсации ПЖ традиционно отводится легочной гипертензии (ЛГ). ЛГ у больных ХОБЛ возникает в результате структурных изменений сосудистой стенки кровеносного русла легких с пролиферацией медии, миграцией гладкомышечных клеток в интиму, фиброэластозом интимы, утолщением адвентиции [6, 8, 11, 12, 15]. В основе расстройств микроциркуляции легких, способствующих нарушению вентиляционно-перфузионных отношений, формированию и прогрессированию ЛГ лежит нарушение функциональной активности эндотелия, известное как дисфункция эндотелия. Многие авторы указывают на высокую частоту выявления ЛГ у больных ХОБЛ [5, 6, 11, 13]. Однако возможна ли ранняя диагностика ХЛС и ТЭЛА только по уровню ЛГ?
Цель исследования: оценка роли ЛГ в формировании структурных и функциональных нарушений правых камер сердца.
МАТЕРИАЛЫ И МЕТОДЫ
Настоящая работа построена на результатах ретроспективного анализа обследований 981 пациента с заболеваниями легких, проведенных в ГНЦ пульмонологии Минздрава России и в НИИ пульмонологии Первого Санкт-Петербургского государственного медицинского университета им. И. П. Павлова в 2000–2015 гг. Были представлены следующие нозологии: ХОБЛ, диссеминированные поражения легких (ДПЛ), ТЭЛА и первичная ЛГ (ПЛГ). Больных с признаками ИБС, левожелудочковой недостаточности, с сочетанием ХОБЛ и ТЭЛА в анализ не включали. Для статистической обработки использовали программу Statistica 6.0. Различия считали статистически значимыми при р < 0,05.
Для исследования функционального состояния правых камер сердца и параметров легочно-сердечной гемодинамики применяли эходоплеркардиографическое исследование. Систолическое давление в легочной артерии (СДЛА) определяли стандартным косвенным методом по максимальному градиенту потока трикуспидальной регургитации. У некоторых больных, помимо косвенного, осуществлялось прямое измерение давления в сосудах малого круга кровообращения. Регистрировались стандартные эхокардиографические параметры, в том числе толщина миокарда передней стенки ПЖ, конечно-диастолический размер ПЖ, площадь сечения правого предсердия, скорость сокращения миокарда ПЖ, фракция изгнания ПЖ по методу Simpson. Рассчитывали общее легочное сопротивление (ОЛС), фракцию систолического утолщения миокарда передней стенки ПЖ, отношение пиковых скоростей трансмитрального кровотока.
РЕЗУЛЬТАТЫ
В таблице 1 представлены данные о величинах СДЛА у больных ХОБЛ, ДПЛ, ТЭЛА и ПЛГ.
Таблица 1
Распределение больных в зависимости от величины систолического давления в легочной артерии
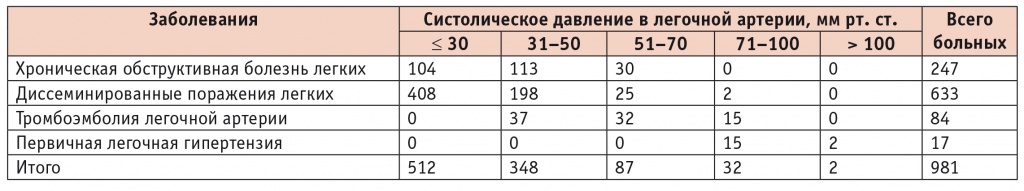
В группе больных ХОБЛ у 42,1% СДЛА в покое не превышало верхнюю границу нормы (30 мм рт. ст.), у 45,7% оказалось в пределах 31–50 мм рт. ст. и лишь у 12,2% превысило 50 мм рт. ст. У 64,5% пациентов с ДПЛ расчетное СДЛА было нормальным, у 31,3 % — в пределах 31–50 мм рт. ст., у 3,9% — от 51 до 70 мм рт. ст. и у 0,3% — более 70 мм рт. ст. Напротив, при ТЭЛА у 44,0% обследованных СДЛА находилось в пределах 31–50 мм рт. ст., у 38,1% — от 51 до 70 мм рт. ст. и у 17,9% — более 70 мм рт. ст., а при ПЛГ у всех пациентов СДЛА превышало 70 мм рт. ст., составив в среднем 89 ± 2,7 мм рт. ст.
Так как для больных с ТЭЛА и ПЛГ была характерна ЛГ высокой степени, при сравнении функционального состояния легочно-сердечной гемодинамики они были объединены в одну группу.
Данные о функциональном состоянии легочно-сердечной гемодинамики у больных ХОБЛ, ДПЛ, ТЭЛА и ПЛГ в зависимости от наличия либо отсутствия ЛГ представлены в таблице 2.
Таблица 2
Показатели легочно-сердечной гемодинамики у пациентов с хронической обструктивной болезнью легких, диссеминированными поражениями легких, тромбоэмболией легочной артерии и первичной легочной гипертензией в зависимости от наличия или отсутствия легочной гипертензии
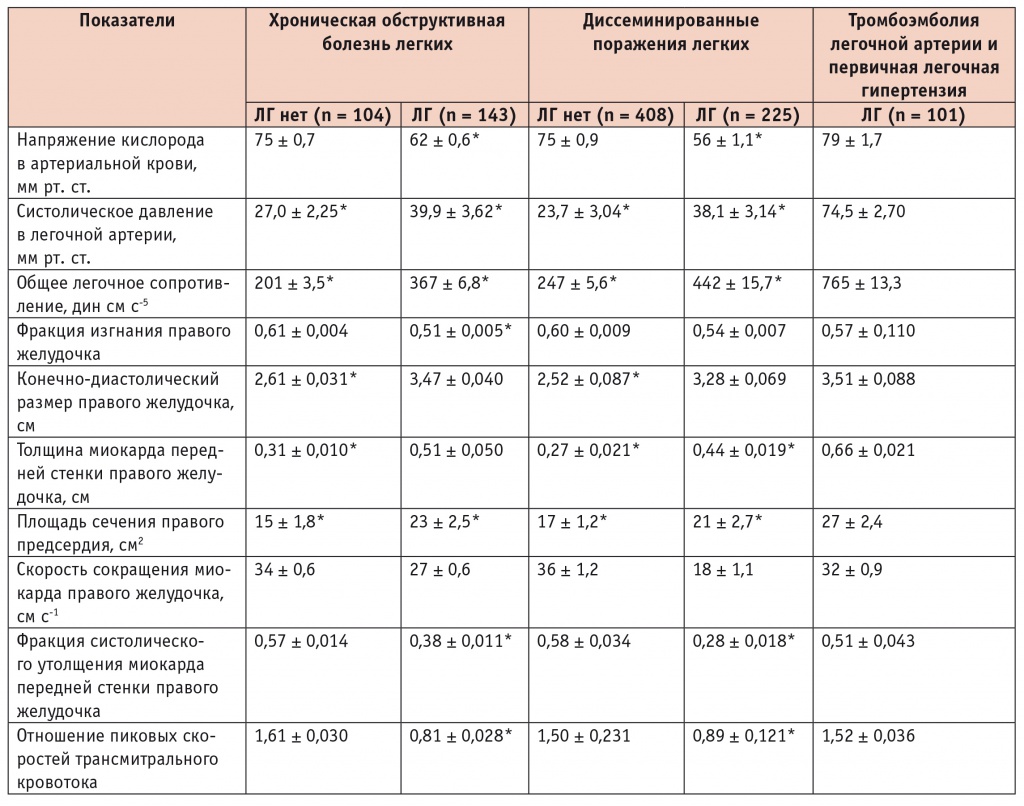
* Отличия от группы тромбоэмболии легочной артерии и первичной легочной гипертензии статистически значимы (p < 0,05).
Полученные результаты позволяют предположить, что характер выявленных гемодинамических изменений зависит не столько от уровня давления в ЛА, сколько от нозологической формы основного заболевания. Так, несмотря на то, что у больных ПЛГ и ТЭЛА отмечались примерно вдвое бóльшие средние величины СДЛА, а гипертрофия миокарда ПЖ была более выраженной, многие показатели функционального состояния правых отделов сердца были статистически значимо выше, чем у больных ХОБЛ. Так, фракция изгнания ПЖ у больных ПЛГ и ТЭЛА статистически значимо не отличалась от таковой в группах ХОБЛ и ДПЛ без признаков ЛГ, в то время как в группе ХОБЛ с ЛГ этот показатель был статистически значимо ниже. Подобная закономерность прослеживалась как для фракционных, так и для скоростных показателей ПЖ, а также для показателей диастолической функции правых отделов сердца. Кроме того, напряжение кислорода в артериальной крови (РаО2) у больных ПЛГ и ТЭЛА было отчетливо выше, чем при ХОБЛ и ДПЛ с ЛГ.
Можно предположить, что значительное ухудшение функционального состояния ПЖ у больных ХОБЛ связано преимущественно с длительностью воспалительного процесса, выраженностью артериальной гипоксемии и гиперкапнии, характером и длительностью инфекционно-токсических и аутоиммунных воздействий на миокард, а не непосредственно с уровнем давления в легочной артерии и ОЛС [3, 4], поскольку известно, что воспалительный процесс играет значительную роль в патогенезе ХОБЛ и основой прогрессирования заболевания является усиление выработки провоспалительных факторов при обострении ХОБЛ [3, 6, 7, 9, 14].
Есть основание предполагать существование, по крайней мере у некоторых больных ХОБЛ, общего фактора, ускоряющего развитие как основного патологического процесса в легочной ткани, так и сопутствующего ему осложнения — поражения сердца. В роли этого фактора может выступать аутоиммунный процесс. Данные о том, что ХОБЛ может быть связана с генетически детерминированным балансом иммунной системы, а профессионально вредные факторы и курение способны усугублять или приводить к проявлению иммунного дисбаланса, дают основание считать, что иммунные нарушения могут способствовать поражению миокарда при ХОБЛ и развитию ХЛС [1, 2, 4, 10].
Нормальной компенсаторной реакцией на возрастание постнагрузки на ПЖ вследствие повышения СДЛА и ОЛС стала тенденция к приросту фракционных и скоростных показателей миокарда ПЖ, что в различной степени отмечалось во всех обследованных группах. Однако, если у больных без существенной гипоксемии (при ТЭЛА, ПЛГ) резервные возможности миокарда ПЖ позволяют достаточно успешно противостоять высокому давлению в малом круге кровообращения, то у лиц с нарушенным газовым составом крови и длительно протекающим, хроническим воспалительным процессом в легких (например, при ХОБЛ) ПЖ может испытывать затруднения при работе даже против значительно меньшего давления. Так, у больных ХОБЛ с ЛГ в условиях резкой гипоксемии (РаО2 = 62 ± 0,6 мм рт. ст.) показатели функционального состояния ПЖ были значительно нарушены при относительно невысоком уровне СДЛА (39 ± 3,62 мм рт. ст.).
Полученные результаты свидетельствуют о том, что развитие гипертрофии и недостаточности ПЖ может наблюдаться при относительно невысоких величинах СДЛА, так, при СДЛА, не превышающем 40–50 мм рт. ст., гипертрофия и дилатация ПЖ нередко отмечались одновременно, а у некоторых больных и вовсе имелась дилатация ПЖ без его гипертрофии.
ЗАКЛЮЧЕНИЕ
Проведенное исследование позволило сделать вывод, что выявленные изменения функционального состояния правого желудочка у больных ХОБЛ и диссеминированными поражениями легких не связаны с высокой легочной гипертензией.
Исследование функциональных параметров только малого круга кровообращения или только правых отделов сердца без их взаимосвязи с системным кровообращением и сердечной деятельностью в целом представляется малоперспективным. Мы полагаем, что одним из важных направлений в изучении хронического легочного сердца в предстоящие годы должны стать исследования повреждающего действия на миокард факторов патологического процесса в легких с широким привлечением биохимических, иммунологических и генетических методов. Целесообразно также всесторонне исследовать у больных ХОБЛ функцию не только правых, но и левых отделов сердца, обратив особое внимание на взаимодействие желудочков, центральной гемодинамики и микроциркуляции в легких, функций малого и большого кругов кровообращения.
Совершенно очевидно, что корригировать тот или иной параметр кровообращения (например, нерезко выраженное повышение давления в легочной артерии) только потому, что он выходит за пределы нормальных значений, у здоровых людей — значит действовать по законам формальной логики. Такие «патологические» изменения могут быть не менее целесообразными для организма, чем физиологические сдвиги у здоровых людей под влиянием стрессов и физических нагрузок. Поиск границ между необходимой защитой организма и повреждающим действием этой защиты до сих пор является сложнейшей задачей.








