Среди самых распространенных заболеваний легких наибольший интерес представляет ХОБЛ. В связи с тем что клинические, функциональные и рентгенологические характеристики ХОБЛ в значительной степени варьируют от одного пациента к другому, даже в случае сопоставимой тяжести вентиляционных нарушений[7, 15, 19, 22], были выделены так называемые фенотипы, определяющие тяжесть течения заболевания. Некоторые авторы предлагают определение фенотипа ХОБЛ как уникальной характеристики или комбинации характеристик, описывающих значимые для клинического исхода различия между пациентами с ХОБЛ[18]. У больных ХОБЛ фенотипа D клинические проявления выражены наиболее ярко.
До сих пор ХОБЛ характеризуется как мультифакторное заболевание, причиной которого могут быть эндо- и экзогенные факторы[4, 16]. Одним из возможных факторов является микробная флора. Ее источником может служить ротовая полость. Микробный зубной налет является причиной возникновения хронического генерализованного пародонтита (ХГП)[3, 21]. Он формируется вследствие недостаточной гигиены полости pта, анатомических особенностей зубочелюстной системы, снижения защитных фактоpов оpганизма и т. д.[9–11]. Основными пародонтопатогенами являются факультативные анаэробы Actinobacillus actinomycetemcomitans, облигатные анаэробы группы Bacteroides рода Prevotella и Porphyromonas, а также грамположительные Peptostreptococcus, Streptococcus[1]. По мере развития тяжелой степени ХГП в суммарной микрофлоре устойчиво увеличивается более чем на два порядка относительное содержание P. gingivalis, Pr. intermedia и Tannerella forsythensis (Bacteroides forsythus)[5, 8, 12].
Изучены и описаны как изменения тканей пародонта при ХОБЛ, так и частое развитие воспалительных изменений в бронхолегочной системе у пациентов с ХГП[1, 6, 14, 20]. Установлено непосредственное влияние степени тяжести ХОБЛ на состояние тканей пародонта: у пациентов с легким течением болезни воспалительные явления в десне менее выражены, чем у пациентов со средним и тяжелым течением[6].
Цель исследования — выявить особенности микрофлоры полости рта у больных ХОБЛ фенотипа D при ХГП легкой и средней степени тяжести.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование были включены 30 больных (26 мужчин и 4 женщины) с ХОБЛ фенотипа D в стадии обострения и ХГП легкой и средней степени тяжести. В группу сравнения вошли 30 пациентов (16 мужчин и 14 женщин) с ХГП легкой и средней степени тяжести без выраженной сопутствующей патологии. Средний возраст исследуемых больных составил 61,2 ± 4,3 года, в контрольной группе — 56,0 ± 6,2 года.
Диагноз ХОБЛ фенотипа D у всех пациентов был верифицирован и подтвержден данными анамнеза, клинической картиной, рентгенологическими и функциональными методами диагностики[17]. Основанием для постановки диагноза служило наличие хронического продуктивного кашля, персистирующей и прогрессирующей одышки при физической нагрузке. Степень тяжести ХОБЛ определяли по GOLD (Global Initiative for Chronic Obstructive Lung Disease) (2011) в соответствии со спирометрическими показателями[17] (ОФВ1 < 80%, ОФВ1/ФЖЕЛ < 70%)[13]. Фенотип определяли при помощи шкал modified Medical Research Council (mMRC) и COPD Assessment Test (CAT) и по анамнезу частоты обострений[2]. Проводили также анализ уровня СРБ и Hb.
Для изучения патологии пародонта применяли клинические методы исследования, включавшие изучение анамнеза, определение общего статуса больного, исследование тканей пародонта. Для уточнения степени костных изменений использовали панорамную рентгенографию челюстей. Регистрировали также степень подвижности зубов по Miller в модификации Flezar, индекс гигиены Федорова — Володкиной и глубину пародонтальных карманов. Для определения микрофлоры полости рта проводили ПЦР-диагностику на основные виды парадонтопатогенов: A. actinomycetemcomitans, P. gingivalis, Pr. intermedia, Treponema denticola, T. forsythensis. Выделение ДНК пародонтопатогенов проводили с помощью набора реагентов МультиДент-5 (ООО НПФ «ГенЛаб», г. Москва).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При сборе анамнеза учитывали показатели длительности течения ХОБЛ и ХГП. Давность появления симптомов ХОБЛ у больных ко времени обследования составляла в среднем 11,7 ± 6,2 года. Длительность проявления ХГП у лиц с сочетанной патологией составляла в среднем 6,1 ± 4,6 года, у пациентов контрольной группы — 7,4 ± 5,9 года.
Одной из основных жалоб у больных ХОБЛ был кашель, который наблюдался в течение всего дня и сопровождался выделением слизистой вязкой, а иногда и гнойной, мокроты. Число обострений в год в среднем составляло 2,2 ± 0,4.
У пациентов с ХОБЛ фенотипа D средний балл по шкале mMRC составил 2,8 ± 0,2, при оценке по шкале CAT — 32 ± 4,9. Существенных различий в уровне Hb у лиц основной и контрольной групп отмечено не было. Концентрация сывороточного СРБ у больных ХОБЛ с ХГП была значительно выше, чем в группе сравнения: 34,5 ± 18,8 мг/л против 12,5 ± 9,7 мг/л соответственно.
Гигиена полости рта у всех исследуемых пациентов была неудовлетворительной. Значения индекса гигиены Федорова — Володкиной в группе ХОБЛ фенотипа D в сочетании с ХГП распределились в пределах 4,7 ± 0,26 мм, у пациентов группы сравнения — в пределах 4,4 ± 0,21 мм. Глубина пародонтальных карманов у всех больных составляла 6,5 ± 0,4 и 6,5 ± 0,4 мм соответственно (табл. 1).
Таблица 1
Параметры состояния пародонта у лиц в исследуемых группах (n = 60)

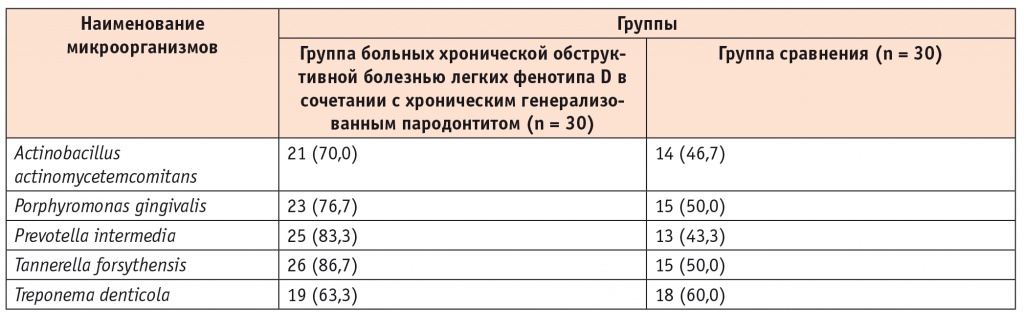
При ПЦР-анализе содержимого пародонтальных карманов у больных обеих групп были обнаружены все исследованные микроорганизмы. У пациентов с сочетанной патологией были наиболее распространены бактерии рода Pr. intermedia, T. forsythensis, тогда как в группе сравнения превалировали Tr. denticola, P. gingivalis. Легкая степень ХГП была выявлена у 40% пациентов, средняя — у 66,7%, в контрольной группе встречаемость ХГП легкой и средней степени тяжести была одинаковой (50%) (табл. 2).
Таблица 2
Частота выявления дезоксирибонуклеиновой кислоты пародонтопатогенов у пациентов исследуемых групп, n (%)
ЗАКЛЮЧЕНИЕ
Учитывая показатели СРБ и Hb, становится очевидным, что в группе с сочетанной патологией были более выражены показатели воспаления, чем в группе сравнения, что может говорить о существенном влиянии ХОБЛ тяжелого течения (фенотипа D) на общее состояние и качество жизни пациентов. В то же время более высокие показатели микрофлоры у больных ХОБЛ в сочетании с хроническим генерализованным пародонтитом (ХГП) демонстрируют возможное негативное влияние микробной флоры на течение ХОБЛ. Механизм патогенеза ХОБЛ и ХГП может быть связан с эндотелиальной дисфункцией и ремоделированием тканей, поэтому в рамках коморбидности развитие ХОБЛ отягощает течение ХГП, и наоборот.








