Термин «ювенильная склеродермия» (ЮСкД), широко использующийся в клинической практике, объединяет два заболевания или, по мнению ряда авторов, две формы одного заболевания неизвестной этиологии с дебютом в возрасте до 16 лет, специфическим проявлением которого является развитие фиброза.
Для ограниченной ЮСкД характерно специфическое фиброзно-склеротическое поражение кожи и подлежащих тканей, при системной ЮСкД, кроме этого, отмечают поражение опорно-двигательного аппарата, внутренних органов и наблюдают вазоспастические нарушения по типу синдрома Рейно, морфологической основой которых является облитерирующий эндартериит, в связи с чем системную ЮСкД считают одним из самых тяжелых ревматических заболеваний у детей[2, 4, 5].
Обе формы ЮСкД относят к редким заболеваниям. В среднем зафиксировано 0,05 случая системной ЮСкД и 1 случай ограниченной ЮСкД на 100 000 населения[9]. ЮСкД часто начинает развиваться в дошкольном и младшем школьном возрасте. Среди больных младше 8 лет количество мальчиков и девочек примерно одинаково, а среди детей старше 8 лет преобладают девочки (соотношение «девочки : мальчики» — 3–4 : 1)[1, 2, 4, 5].
ЮСкД является хроническим заболеванием, которое при отсутствии лечения неуклонно прогрессирует[1, 2, 13, 14]. Наш опыт многолетнего наблюдения свидетельствует о том, что у ряда пациентов с ЮСкД происходит нарушение темпов физического развития, в том числе задержка роста. Эта проблема весьма актуальна, так как дети, имеющие задержку роста, испытывают серьезные психологические и социальные трудности[3]. Можно предположить, что, кроме семейно-конституциональных особенностей, причинами задержки роста больных ЮСкД могут быть тяжесть основного заболевания и проводимая иммуносупрессивная терапия, которая у ряда пациентов с быстропрогрессирующими вариантами заболевания включает глюкокортикоиды (ГК)[6, 7, 8, 11, 12]. Нарушение темпов роста и сроков наступления пубертата хорошо изучены при ювенильном ревматоидном артрите и системной красной волчанке у детей[6]; аналогичные исследования при ЮСкД носят единичный, описательный характер. До настоящего времени вопросы, касающиеся частоты, выраженности и причин нарушений роста при ЮСкД, не решены, что и определило цели нашего исследования.
Цель работы: изучить особенности роста детей с различными формами ЮСкД и оценить значение факторов, влияющих на рост этих пациентов и его темпы.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено проспективное когортное исследование с участием 101 больного ЮСкД в возрасте от 3 до 17 лет (средний возраст участников составил 11,5 ± 3,7 года). Среди участников было 22 мальчика и 79 девочек (девочки : мальчики — 3,5 : 1). Все больные проходили лечение в ревматологическом отделении Университетской детской клинической больницы Первого Московского государственного медицинского университета им. И. М. Сеченова за период с сентября 2012 по апрель 2014 г.
Критерии включения в исследование: верифицированный диагноз системной ЮСкД в соответствии с предварительными диагностическими критериями системной ЮСкД (Pediatric Rheumatology European Society, 2004); верифицированный диагноз ограниченной ЮСкД в соответствии с предварительными классификационными критериями, принятыми на Международной согласительной конференции детских ревматологов в 2004 г.; возраст дебюта заболевания — до 16 лет.
Критерии исключения из исследования: отсутствие сведений о динамике и скорости роста пациентов и о росте их родителей.
Возраст больных на момент дебюта заболевания колебался от года до 15 лет, продолжительность болезни составляла от нескольких месяцев до 15 лет.
По результатам обследования у 77 детей (76,2%) была диагностирована ограниченная ЮСкД, а у 24 (23,8%) — системная.
Анализировали историю заболевания, время установления диагноза, длительность заболевания, его клинические проявления, характер и продолжительность проводимой терапии. Особое внимание уделяли наследственному анамнезу пациентов.
При анализе историй болезни было установлено, что 70 пациентов (69,3%) ранее проходили терапию ГК различной интенсивности и продолжительности, 17 (16,8%) получали метотрексат, 7 (6,9 %) — пеницилламин, а 4 (4,0%) ребенка — только местное лечение.
У всех обследованных пациентов измеряли рост и скорость роста, затем сравнивали полученные значения с нормальными показателями, которые определяли с учетом пола и возраста пациентов по центильным таблицам J. M. Tanner и R. H. Whitehouse. Сравнение значений выражали в виде показателя стандартного отклонения (Standard Deviation Score, SDS), где 0 — среднее, +2 — верхняя граница нормы, –2 — нижняя граница нормы для данного возраста и пола.
Величину целевого конечного роста расcчитывали по формуле: целевой рост = (рост матери + рост отца) / 2 ± 6,5 см (где +6,5 см — для мальчика, –6,5 см — для девочки). Соответствие значений целевого конечного роста норме определяли также с учетом пола и возраста и выражали в виде SDS.
Статистическую обработку данных проводили с использованием пакета программ Microsoft Excel 2010, SPSS 15.0. Количественные переменные представлялись в виде средних значений ± стандартное отклонение, качественные — в виде числа наблюдений и доли от общего числа пациентов в процентах. Статистическую значимость различий показателей определяли с помощью критерия Стьюдента при уровне различия р < 0,05. Рассчитывали ОР.
РЕЗУЛЬТАТЫ
В таблице 1 представлена характеристика клинических вариантов заболевания.
Таблица 1
Клиническая характеристика обследованных больных
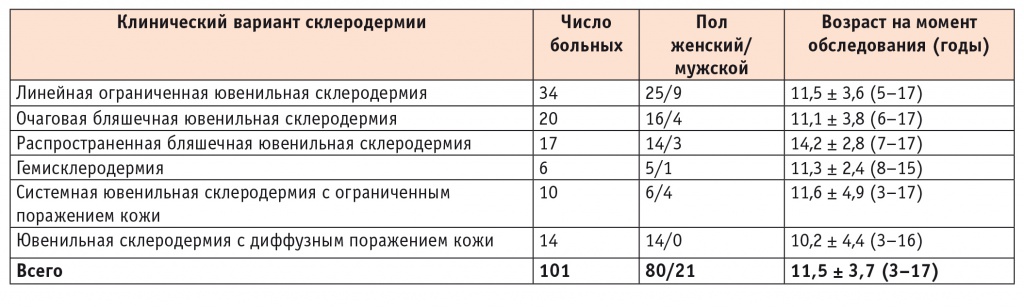
Результаты анализа показали, что среди 101 обследованного ребенка с ЮСкД были пациенты как с нарушениями, так и с нормальными показателями роста и его скорости, на основании чего пациентов распределили по группам (табл. 2).
Таблица 2
Показатели роста и скорости роста у обследованных пациентов
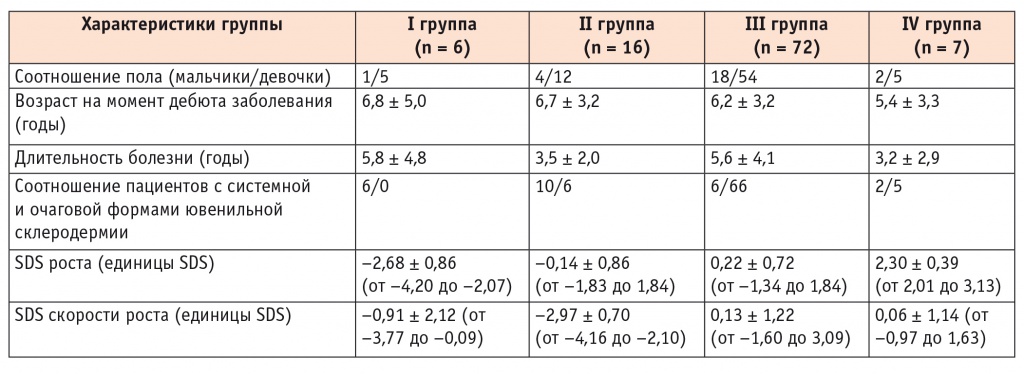
I группу составили 6 детей (5,9%) с задержкой роста (SDS роста < –2); во II группу вошли 16 детей (15,8%) с нормальными показателями роста (–2 < SDS роста < +2), но со снижением его скорости (SDS скорости роста < –2); III группа — 72 ребенка (71,3%) с нормальными показателями роста (–2 < SDS роста < +2) и его скорости (–2 < SDS скорости роста); IV группу составили 7 детей (6,9%) с высокорослостью (SDS роста > +2).
Как следует из таблицы 2, соотношение мальчиков и девочек в I–IV группах составило от 1 : 5 до 1 : 2,5, что соответствует распределению больных по гендерному признаку в когорте. Средний возраст на момент дебюта заболевания ЮСкД в группах статистически значимо не различался.
При анализе соотношения системной и ограниченной форм ЮСкД обращало на себя внимание то, что в группе с задержкой роста все 6 пациентов страдали системной ЮСкД; в группе пациентов со снижением скорости роста системная форма ЮСкД преобладала, ее отмечали у 10 из 16 пациентов (62,5%); в группе пациентов с нормальными показателями роста и его скорости системную ЮСкД диагностировали лишь у 7 из 72 больных (10,6%); в группе высокорослых системная форма имела место лишь у 2 детей из 7 (28,5%). Эти факты свидетельствуют об ассоциации задержки роста с клинически более тяжелой, системной формой ЮСкД.
Средняя длительность заболевания у пациентов разных групп составила от 3,2 ± 2,9 до 5,8 ± 4,8 года. Мы не подтвердили статистической значимости различий длительности заболеваний между группами, что, вероятно, обусловлено небольшой выборкой. Однако у пациентов с высокорослостью длительность заболевания была наименьшей из всех групп, что позволяет предположить наличие влияния длительности заболевания на возможность развития задержки роста.
Мы изучили взаимосвязь показателей роста и его скорости у пациентов с общей длительностью терапии ГК, с длительностью приема терапевтической дозы (доза ≥ 0,5 мг/кг/сут), поддерживающей дозы (доза ≤ 0,3 мг/кг/сут), а также суммарной курсовой дозы ГК. Эти данные подробно представлены в таблице 3.
Таблица 3
Зависимость показателей роста и скорости роста больных ювенильной склеродермией от длительности терапии и величины суммарной дозы глюкокортикоидов
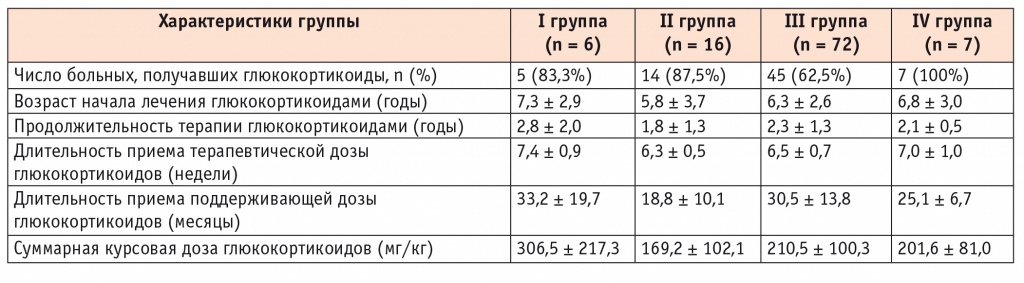
Продолжительность лечения максимальной терапевтической дозой ГК составляла при различных формах ЮСкД в среднем по группам от 6,3 до 7,4 недель, но была наибольшей в группе детей с задержкой роста (7,4 ± 0,9 недели). Продолжительность лечения поддерживающей дозой в этой группе также была максимальной (33,2 ± 19,7 месяца). Соответственно, терапия ГК была наиболее продолжительной (2,8 ± 2,0 года), а суммарная курсовая доза наиболее высокой (306,5 ± 217,3 мг/кг) у пациентов с задержкой роста, у которых отмечали наиболее тяжелые формы болезни. К сожалению, указанные различия не были статистически значимыми.
В целом, в нашей когорте ОР задержки роста был в 2,1 раза выше у пациентов, получавших ГК (95%-ный ДИ: 0,3–19,1). Следует еще раз подчеркнуть, что терапию ГК назначали больным с системной ЮСкД и наиболее тяжелыми формами ограниченной ЮСкД, поэтому не представляется возможным исключить влияние самого заболевания на процесс роста.
С целью оценки влияния наследственности проведено сопоставление роста больных ЮСкД с ростом их родителей (табл. 4).
Таблица 4
Сопоставление показателей стандартного отклонения (Standard Deviation Score, SDS) целевого конечного роста (рассчитывается на основании роста родителей) и SDS фактического роста у пациентов с ювенильной системной склеродермией
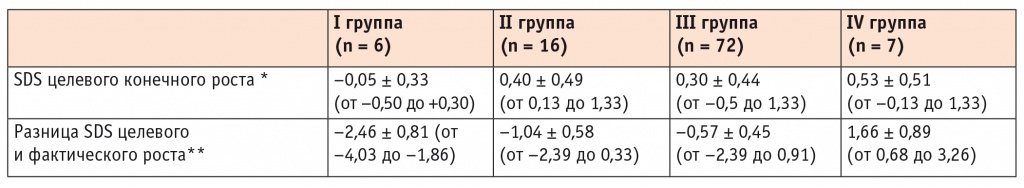
* Целевой рост = (рост матери + рост отца) / 2 ± 6,5 см (где +6,5 см — для мальчика и –6,5 см — для девочки); по центильным таблицам рассчитывался SDS целевого роста (где 0 — среднее, +2 — верхняя граница нормы, –2 — нижняя граница нормы);
** SDS целевого роста — SDS фактического роста на момент осмотра пациента.
При анализе показателей было установлено, что наименьшие значения целевого роста имели дети из группы с задержкой роста, а наибольшие — из группы с высокорослостью, что, безусловно, свидетельствует о роли наследственности. Интересным представляется тот факт, что показатели SDS целевого роста детей и SDS фактического роста на момент осмотра различались. Отмечено, что дети с низкорослостью отставали от целевых показателей (разница SDS целевого роста и SDS фактического роста в этой группе составила –2,46 ± 0,81 SDS), а дети с высокорослостью, напротив, превышали их (в их группе разница целевого и фактического роста составила 1,66 ± 0,89 SDS). Это позволяет утверждать, что наследственность не является единственным фактором, влияющим на рост пациентов с ЮСкД.
Как следует из таблицы 2, наиболее многочисленной была группа, в которой показатели роста и скорости роста пациентов не выходили за пределы нормальных значений (III группа), но существенно варьировали. Для более глубокого анализа мы разделили пациентов III группы на следующие подгруппы (табл. 5): III-a — пациенты, показатели SDS фактического роста которых были ниже показателей целевого роста (SDS фактического роста — SDS целевого роста < –0,5); III-b — пациенты, показатели SDS фактического роста которых соответствовали показателям SDS целевого роста (SDS фактического роста — SDS целевого роста +/–0,5); III-c — пациенты, показатели SDS фактического роста которых превышали SDS целевого роста (SDS фактического роста — SDS целевого роста > +0,5).
Таблица 5
Клиническая характеристика больных ювенильной склеродермией III группы с нормальными показателями роста и скорости роста
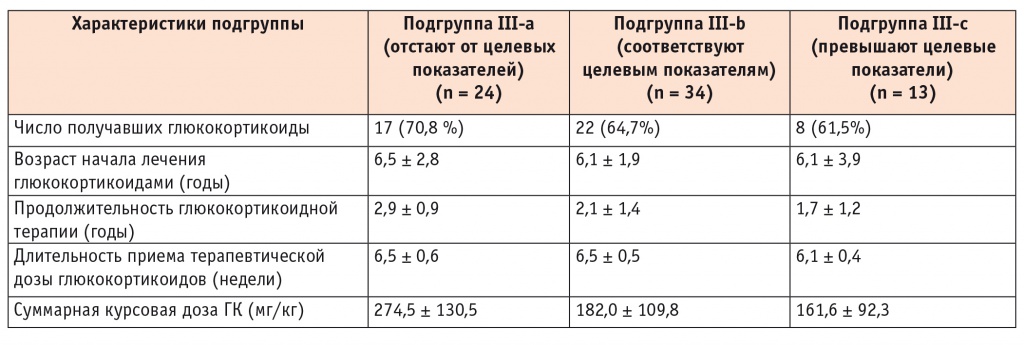
У больных подгруппы III-a, чей рост отставал от целевых показателей, была самая большая продолжительность терапии ГК и самая большая суммарная доза ГК. В то же время у пациентов подгруппы III-c, чей рост превышал показатели целевого роста, продолжительность ГК терапии и суммарная доза этих препаратов были наименьшими.
ОБСУЖДЕНИЕ
По данным литературы, задержка роста у детей и подростков встречается при многих соматических заболеваниях, в том числе хронических воспалительных заболеваниях кишечника, муковисцидозе, онкологических болезнях и ревматических заболеваниях[6, 10]. Причины задержки роста при хронических болезнях объясняются рядом факторов, в том числе патогенетическими особенностями основного заболевания. При ревматических болезнях имеет место гиперпродукция цитокинов различных классов, которые блокируют действие ростовых факторов в органах-мишенях, приводя к задержке роста. Подтверждением этого факта, например, является восстановление темпов роста детей с ювенильным ревматоидным артритом после назначения антицитокиновой терапии[8, 9]. При назначении ГК, с одной стороны, подавляется активность воспаления, что должно производить положительный эффект на процессы роста. С другой стороны, ГК обладают катаболическим действием, снижают секрецию ИФР и соматотропина, что при длительном их применении может оказывать негативное воздействие на линейный рост детей[3].
В нашем исследовании у 88 (87,1%) больных с ЮСкД отмечали нормальные параметры роста, несмотря на то что 66 (75%) из них получали терапию ГК. Лишь у 6 человек (5,9%) из общего числа обследованных пациентов была задержка роста, а у 7 (6,9%), наоборот, отмечали высокорослость. Этот факт представляется нам чрезвычайно значимым, поскольку нами установлено не столь существенное, как принято считать, отрицательное влияние проводимой базисной терапии ГК на рост ребенка. Широкое применение средств базисного лечения, включая ГК, позволяет значительно улучшить прогноз ЮСкД, предотвратить калечащие, инвалидизирующие повреждения кожи, подлежащих тканей, мышц, опорно-двигательного аппарата. Полученные нами данные об отсутствии задержки роста у большинства детей с ЮСкД, получавших лечение ГК, позволяют развеять опасения врача и родителей о неизбежности задержки роста при проведении данного вида лечения.
Рассматривая различные факторы, которые могли бы повлиять на развитие задержки роста, мы не обнаружили ассоциации с полом. В проведенном исследовании соотношение количества мальчиков и девочек во всех группах варьировало от 1 : 5 до 1 : 2,5, что согласуется с литературными данными[1, 2, 5].
Существует мнение, что раннее начало заболевания и, соответственно, ранняя терапия ГК в большей степени ассоциированы с нарушением роста пациента. Однако нами не выявлено связи возраста больного на момент дебюта ЮСкД и начала лечения ГК с риском развития задержки роста.
Известно, что системная ЮСкД характеризуется более тяжелым течением, чем ограниченная ЮСкД, и практически всегда требует длительного лечения ГК. Именно эти два факта в совокупности приводят к развитию задержки роста у пациентов. Действительно, нами установлено, что длительность заболевания, продолжительность терапии и суммарная курсовая доза ГК были наибольшими у пациентов с задержкой роста. Задержку роста отмечали у 5 (7,6%) детей, получавших ГК, и у 1 (3,4%) ребенка среди пациентов, не получавших ГК.
Однако на рост пациентов с ЮСкД влияют не только тяжесть заболевания и терапия ГК. Так, в группе детей с задержкой роста показатель целевого роста детей, рассчитанного на основе роста родителей, был ниже, чем в других группах. На основании этого мы можем предположить, что наследственность вносит свой вклад в формирование задержки роста.
ЗАКЛЮЧЕНИЕ
Проведенное нами исследование свидетельствует, что на развитие задержки роста у пациентов с ювенильной склеродермией (ЮСкД) влияют форма заболевания и его тяжесть, длительность терапии и суммарная курсовая доза глюкокортикоидов (ГК), а также наследственность. Таким образом, терапия адекватными дозами ГК, способствующая снижению активности и предотвращающая прогрессирование тяжелых форм ЮСкД, не должна рассматриваться в качестве негативного фактора, влияющего на ростовой прогноз.








