Увеличение общей продолжительности жизни больных ММ, возможное благодаря непрерывному лечению с применением химиопрепаратов, нередко сопровождается нежелательными явлениями (НЯ), определяющими не только качество жизни пациентов, но и дальнейшую тактику их ведения, прогноз и выживаемость. Кроме того, такие осложнения, как остеодеструкции, полинейропатия и почечная недостаточность, а также сахарный диабет, исходно присутствовавшие у больных ММ, могут прогрессировать в процессе лечения вплоть до необратимости развившихся изменений. Особенности взаимосвязи продолжительности жизни больных ММ и осложнений, наблюдаемых у этой категории пациентов, до конца не изучены [4].
Цель исследования: оценить степень влияния НЯ (остеодеструкции, полинейропатии, почечной недостаточности и сахарного диабета) на продолжительность жизни пациентов с ММ.
МАТЕРИАЛЫ И МЕТОДЫ
Проведен ретроспективный анализ законченных случаев (от момента установления диагноза до летального исхода) 29 больных ММ, лечившихся в гематологическом центре ФГКУ «Главный военный клинический госпиталь им. Н. Н. Бурденко» МО РФ в период с 1988 по 2014 г. В выборку были включены 24 (82,8%) мужчины и 5 (17,2%) женщин, что отражает специфику контингента ведомственного лечебного учреждения. Возраст больных варьировал от 46 до 83 лет (медиана возраста составила 66 лет), причем большинство обследованных (69,0%, n = 20) были пожилого и старческого возраста.
Все больные обследованы по единому протоколу (формализованной истории болезни) включавшему: оценку жалоб, сбор анамнеза; осмотр по органам и системам органов; клинический и биохимический анализы крови; клинический анализ мочи; иммунохимическое исследование белков сыворотки крови и мочи; ЭКГ, рентгенографию органов грудной клетки и костей скелета, КТ и МРТ позвоночника (в случае необходимости); биопсию костного мозга. Стадию заболевания определяли в соответствии с системой ISS (International Staging System, 2005). На первой стадии заболевания наблюдали только 1 пациента (3,5%), на второй стадии — 9 больных (31,0%), на третьей — 19 пациентов (65,5%).
Пациенты получали лечение в соответствии с общепринятыми принципами ведения больных ММ: цитостатическую терапию, глюкокортикоиды, аутологичную трансплантацию гемопоэтических стволовых клеток и сопроводительную терапию, включавшую трансфузии компонентов крови (эритроцитной массы, свежезамороженной плазмы крови, тромбоцитного концентрата), антибиотикотерапию, аналгезию.
При регистрации НЯ оценивали присутствие и выраженность остеодеструкций, полинейропатии, почечной недостаточности и сахарного диабета, различая предшествовавшие состояния и осложнения, возникшие вследствие лечения. Степень выраженности НЯ определяли в соответствии с Common Terminology Criteria for Adverse Events (CTCAE) v. 4.0 и регистрировали в грейдах, где 1 — минимальный, а 5 — максимальный грейд.
Статистическую обработку полученных результатов проводили с помощью пакета программ IBM SPSS Statistics 21 (IBM Corp.). Для оценки статистической значимости различий по каждому патологическому состоянию (остеодеструкции, полинейропатии, нефропатии, сахарному диабету) в разные интервалы наблюдений (дебют, 0–1 год, 1–3 года, 3–5 лет) сравнивали грейды каждого вида нарушений, используя критерий Фридмана. Наблюдения без грейда (0) или с пропущенными значениями (0 или выбывшие больные) исключали из анализа. Для определения различий выраженности НЯ в смежных интервалах наблюдений (дебют и 0–1 год; 0–1 год и 1–3 года; 1–3 года и 3–5 лет) использовали одновыборочный критерий Вилкоксона. Взаимосвязь выраженности НЯ с продолжительностью жизни больных ММ исследовали с помощью коэффициента ранговой корреляции Спирмена [5].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В общей группе больных ММ (n = 29) выделены три подгруппы пациентов в соответствии с продолжительностью жизни после установления диагноза. Первая подгруппа включала проживших не более года (n = 11); пациенты второй подгруппы прожили более года, но не дольше 3 лет (n = 6); больные третьей подгруппы прожили не менее 5 лет после установления диагноза ММ (n = 12). Нарушения (остеодеструкции, полинейропатию, нефропатию, сахарный диабет) регистрировали в дебюте заболевания, в течение первого года, в интервалах лечения от года до 3 лет и от 3 до 5 лет (табл.).
Таблица
Нежелательные явления, зарегистрированные в различные периоды наблюдения больных множественной миеломой
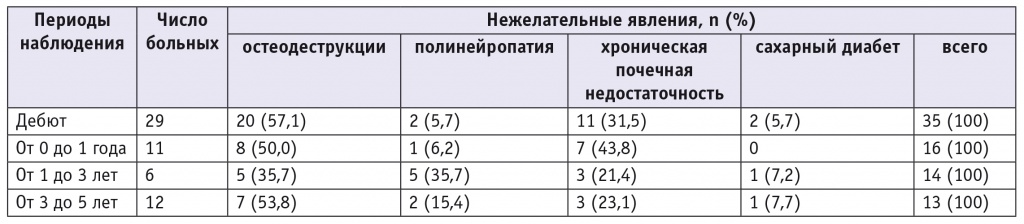
В дебюте заболевания у пациентов (n = 29) зарегистрировано 35 случаев НЯ, включавших как самостоятельные заболевания, так и сочетания патологических процессов.
В течение первого года лечения у больных ММ (n = 11) наблюдались 16 случаев осложнений: остеодеструкции — 8 (50,0%), полинейропатия — 1 (6,2%), почечная недостаточность — 7 (43,8%); случаев сахарного диабета не зарегистрировано.
Среди больных, проживших более года после установления диагноза ММ (n = 6), НЯ распределились следующим образом: остеодеструкции — 5 случаев (35,7%), полинейропатия — 5 (35,7%), почечная недостаточность — 3 (21,4%), сахарный диабет — 1 (7,2%).
В интервале наблюдения 3–5 лет у больных ММ (n = 12) зарегистрировано 13 НЯ: остеодеструкции — 7 (53,8%), полинейропатия — 2 (15,4%), почечная недостаточность — 3 (23,1%), сахарный диабет — 1 (7,7%).
Проанализированы различия выраженности НЯ в разные интервалы времени [3]. Выявление корреляционной взаимосвязи между продолжительностью жизни больных ММ и выраженностью осложнений основывалось на предположении об их обратной взаимозависимости. Для решения этой задачи оценены значение и сила корреляции между продолжительностью жизни больных и грейдом НЯ, выявленных у них, за каждый временной интервал [1, 2].
При оценке выраженности остеодеструкций в разные периоды наблюдения больных (n = 6) различий не выявлено (Fr = 3, df = 3, p < 0,392). Отсутствие различий мы объяснили небольшим количеством больных, проживших более 3 лет, когда каждому значению выраженности остеодеструкций у пациента в дебюте ММ соответствовало значение выраженности этого нарушения в интервалах наблюдения того же пациента. Прочие больные, не имевшие грейда выраженности остеодеструкций (выбывшие в результате смерти или с остеодеструкцией, развившейся не в дебюте заболевания, а позже), исключены из расчетов.
Для сравнения выраженности остеодеструкций в смежных интервалах наблюдения мы сопоставили грейды остеодеструкций в этих интервалах («дебют» и «0–1 год»; «0–1 год» и «1–3 года»; «1–3 года» и «3–5 лет»), как при попарном сравнении двух зависимых выборок, используя одновыборочный критерий Вилкоксона. При этом не понадобилось расчета нового критического уровня статистической значимости. Получены следующие результаты:
-
степень выраженности остеодеструкций в интервале лечения «0–1 год» статистически значимо выше их грейда в дебюте заболевания (n = 20; W = 15, Z = –2,236, p = 0,025);
-
статистически значимых различий грейдов остеодеструкций в интервалах наблюдения «0–1 год» и «1–3 года» (n = 14) не обнаружено (W = 3, Z = –1,414, p = 0,157);
-
различий выраженности остеодеструкций между интервалами наблюдения «1–3 года» и «3–5 лет» (n = 7) не выявлено (W = 1, Z = –1,0, p = 0,317).
Оценить статистическую значимость различий выраженности полинейропатии в разные интервалы наблюдений при помощи критерия Фридмана и критерия Вилкоксона не представлялось возможным из-за ограниченного числа пар пациентов с полинейропатиями. Так, в дебюте заболевания полинейропатию наблюдали только у 2 пациентов (11,8%), на 1-м году лечения — у 5 (29,4%), в интервале наблюдения от года до 3 лет — у 8 (47,0%), с 3 до 5 лет — у 2 больных (11,8%).
Статистически значимых различий по степени выраженности почечной недостаточности у больных ММ (n = 2) в разные периоды наблюдения не обнаружено (Fr = 3, df = 3, p = 0,392). При сравнении грейдов почечной недостаточности в смежные интервалы наблюдения («дебют» и «0–1 год»; «0–1 год» и «1–3 года»; «1–3 года» и «3–5 лет») с помощью одновыборочного критерия Вилкоксона как для попарного сравнения двух зависимых выборок получены следующие результаты:
-
статистически значимых различий выраженности почечной недостаточности (n = 11) между дебютом заболевания и интервалом наблюдения «0–1 год» не выявлено (W = 3, Z = –1,342, p = 0,180);
-
не выявлено различий выраженности почечной недостаточности (n = 5) между интервалами наблюдения «0–1 год» и «1–3 года» (W = 1, Z = –1,0, p = 0,317);
-
исследование значимости различий по грейду почечной недостаточности в парных наблюдениях (n = 3) между интервалами наблюдения «1–3 года» и «3–5 лет» с помощью одновыборочного критерия Вилкоксона ограничено малым числом больных.
Оценить статистическую значимость различий выраженности сахарного диабета в разные интервалы наблюдений при помощи критерия Фридмана и критерия Вилкоксона не представлялось возможным из-за ограниченного числа пациентов с сахарным диабетом. Так, в дебюте заболевания сахарный диабет наблюдали только у 2 пациентов, на 1-м году лечения — у 1, в интервале наблюдения «1–3 года» — у 3, «3–5 лет» — у 1 больного, что показывает отсутствие роста частоты этого сопутствующего заболевания с течением времени.
Таким образом, при сравнении выраженности НЯ в разные интервалы наблюдения больных ММ выявлено значимое увеличение выраженности только остеодеструкций: на первом году лечения выраженность этих осложнений статистически значимо выше их грейда в дебюте заболевания.
Следовательно, остеодеструкции как наиболее важный вид осложнений могут влиять на течение ММ и их можно рассматривать как самостоятельный прогностический признак, определяющий продолжительность жизни таких пациентов. Для проверки этой гипотезы проведен корреляционный анализ между степенью выраженности остеодеструкций больных ММ в интервале наблюдения «0–1 год» и продолжительностью жизни (n = 20). С этой целью применим коэффициент ранговой корреляции Спирмена.
В результате расчетов выявлена обратная, средняя и достоверная связь продолжительности жизни больных ММ со степенью выраженности остеодеструкций (rs = –0,447, p = 0,048, n = 20).
Для исключения влияния возраста больных на выраженность остеодеструкций (например, патологических переломов и деформации костей скелета вследствие остеопороза) мы проверили гипотезу об отсутствии взаимосвязи возраста пациентов со степенью остеодеструкции (Н0), вновь использовав коэффициент ранговой корреляции Спирмена.
В результате корреляционного анализа статистически значимой взаимосвязи возраста пациентов с выраженностью остеодеструкций не обнаружено (rs = –0,117, p = 0,624, n = 20), что подтверждает взаимосвязь выраженности остеодеструкций и продолжительности жизни больных ММ.
ЗАКЛЮЧЕНИЕ
Статистически значимые различия выраженности нежелательных явлений у больных множественной миеломой (ММ), выявленные в нашем исследовании, отражают значительное ухудшение состояния пациентов, «переживших» год с момента установления диагноза. Самым значимым осложнением у таких больных являются остеодеструкции, степень выраженности которых умеренно влияет на продолжительность жизни пациентов, уменьшая ее. При этом выраженность остеодеструкций не зависит от возраста больных ММ, что заставляет рассматривать данный вид осложнений как самостоятельный фактор, снижающий продолжительность жизни таких пациентов.
Возможно, при анализе большего числа наблюдений подобная закономерность проявится более четко. Однако патогенетический смысл влияния возрастающей выраженности остеодеструкций на продолжительность жизни больных ММ (что наиболее значимо проявляется на первом году лечения) скорее всего останется неизменным, так как эта взаимосвязь отражает растущий объем миеломы, несмотря на лечение.
Результаты исследования заставляют продолжить работу по изучению выраженности остеодеструкций как самостоятельного прогностического фактора в анализе продолжительности жизни больных ММ.








