По данным ВОЗ, ХОБЛ занимает 3-е место в структуре смертности. Ведущей причиной смерти при этом заболевании являются сердечно-сосудистые осложнения. Известно, что хроническое системное воспаление при ХОБЛ — важный фактор риска развития поражения сердечно-сосудистой системы, поэтому данная нозология сопровождается АГ, ИБС, сердечной недостаточностью, аритмиями. Наиболее неблагоприятные осложнения, несмотря на относительно редкую встречаемость у больных ХОБЛ (10%), влечет за собой фибрилляция предсердий (ФП)[5]. Больные ХОБЛ часто не подозревают о наличии у них ФП и не получают антикоагулянтную терапию, имея при этом высокий риск возникновения тромбоэмболических осложнений. Поэтому поиск предикторов развития ФП у больных ХОБЛ является актуальной проблемой.
Исследования, посвященные данному вопросу, не дают исчерпывающей информации о том, какие изменения сердечно-сосудистой и бронхолегочной систем влияют на возникновение и протекание этого вида аритмии у пациентов с ХОБЛ. Имеются данные о том, что повышение давления в легочной артерии и увеличение диаметра ПЖ связаны с развитием ФП у больных ХОБЛ[6, 7, 8].
Есть сведения, что диастолическая дисфункция ЛЖ коррелирует с выраженностью бронхообструкции. Предполагают, что хроническое легочное сердце при вторичной легочной гипертензии может изменять геометрию ЛЖ[9, 5]. Однако не установлено, насколько диастолическая функция ЛЖ может влиять на возникновение и течение ФП у больных ХОБЛ.
Н. А. Кароли и соавт.[2] выявили корреляционную связь между жесткостью сосудистой стенки и тяжестью течения ХОБЛ. Авторы другого исследования отмечают, что у больных с сочетанием ХОБЛ и АГ жесткость сосудистой стенки, как и пульсовое давление в аорте, статистически значимо выше, чем у больных с изолированными патологиями. Однако влияние параметров ригидности и центральной гемодинамики на возникновение ФП у больных ХОБЛ не изучено[1].
Известно, что высокочувствительный СРБ (ВчСРБ) связан как с возникновением, так и с частотой рецидивирования ФП в общей популяции[4]. Однако степень влияния системного воспаления на возникновение ФП у больных ХОБЛ не изучена.
Цель исследования: изучение состояния сердечно-сосудистой системы и системного воспаления у больных ХОБЛ с ФП и выявление параметров, влияющих на возникновение данного вида аритмии.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводили на базе кардиологического и пульмонологического отделений филиала № 1 Городской клинической больницы № 24 Департамента здравоохранения г. Москвы в период с февраля 2014 по январь 2015 г. В исследование включали пациентов с ХОБЛ, наличие которой подтверждалось спирометрией. Изучали также данные оценочного теста по ХОБЛ (COPD Assessment Test) и модифицированной шкалы одышки Modified Medical Research Council. Критериями исключения являлись ИБС, пороки сердца, сахарный диабет, нарушения функции щитовидной железы, бронхиальная астма, синдром Вольфа — Паркинсона — Уайта, синдром слабости синусового узла, постоянная форма ФП.
Распределение пациентов по группам проводили на основании подтвержденного медицинскими документами анамнеза пароксизмальной формы ФП и результатов суточного мониторирования ЭКГ по Холтеру (ХМ-ЭКГ).
Исследуемую группу составили 45 больных с неклапанной пароксизмальной ФП и ХОБЛ II–IV стадий (по критериям Global Initiative for Chronic Obstructive Lung Disease, 2011) вне обострения. Из них 22 человека имели ФП в анамнезе, у 23 данный вид аритмии был зарегистрирован впервые при включении в исследование. Группу контроля составили 40 пациентов с ХОБЛ II–IV стадий вне обострения без ФП.
Средний возраст больных в группе ХОБЛ и ФП (Me [25k%; 75k%]) составил 68 [62; 74] лет, в контрольной группе — 65 [61; 69] лет (р = 0,032). Длительность течения ХОБЛ у пациентов с коморбидной патологией составила 10,0 [6,0; 12,0] года, в группе больных ХОБЛ — 8,5 [6,3; 11,0] года (р = 0,137). Индекс курения (пачка/лет) статистически значимых различий не имел. В обеих группах преобладали лица мужского пола (табл. 1). С учетом возможного влияния терапии ХОБЛ на возникновение и частоту пароксизмов ФП проводили ее сравнительную оценку, при этом статистически значимых различий между группами выявлено не было. По результатам ХМ-ЭКГ оценивали наличие и количество эпизодов ФП за сутки.
Таблица 1
Характеристика групп
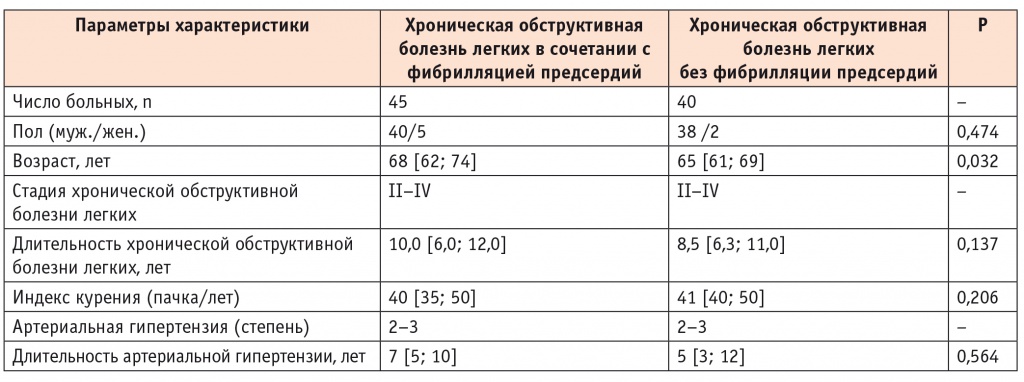
Примечание. Данные представлены в виде медианы, первого и третьего квартилей. Для расчета статистической значимости различий между группами использовали двухсторонний U-критерий Манна — Уитни.
Пациентам обеих групп проводили СМАД с определением центрального давления в аорте и параметров жесткости сосудистой стенки: средней скорости распространения пульсовой волны в аорте (PWao), времени распространения отраженной пульсовой волны (RWTT), амбулаторного индекса ригидности артерий (AASI), а также максимальной скорости нарастания АД (dP/dt) с помощью суточного монитора АД BPLab МнСДП-2 (ООО «Петр Телегин», г. Нижний Новогород).
Всем пациентам выполняли ЭхоКГ с использованием эхокардиографа Vivid 7 Expert (General Electric Medical Systems, Германия) с определением диастолической функции миокарда ЛЖ: пиковых скоростей раннего наполнения (vE, м/с) и позднего наполнения (vA, м/с), времени замедления раннего диастолического наполнения (DT), времени изоволюметрического расслабления (IVRT). В качестве маркера выраженности системного воспаления оценивали ВчСРБ.
Статистическую обработку данных осуществляли в программе IBM SPSS Statistics 20.0 (IBM, США). Межгрупповое сравнение производили с использованием U-критерия Манна — Уитни. Для анализа взаимосвязи признаков применяли коэффициент ранговой корреляции Спирмена (R). Данные описательной статистики представлены в виде медианы, 1-го и 3-го квартилей. Для оценки качественных признаков использовали критерий χ2. Статистически значимыми считали различия при р ≤ 0,05. Проводился линейный регрессионный анализ.
РЕЗУЛЬТАТЫ
Пациенты обеих групп имели АГ, преимущественно 3-й степени, и патологические суточные профили АД без статистически значимых различий. По длительности течения АГ статистически значимых различий выявлено не было (р = 0,564) (см. табл. 1). При этом у больных ХОБЛ в сочетании с ФП было отмечено статистически значимое повышение систолического АД в дневное время (р = 0,024) в сравнении с контрольной группой, что, вероятно, связано с наибольшей активацией у них симпатоадреналовой системы на фоне ХОБЛ (табл. 2).
Таблица 2
Сравнительный и корреляционный анализы в группах
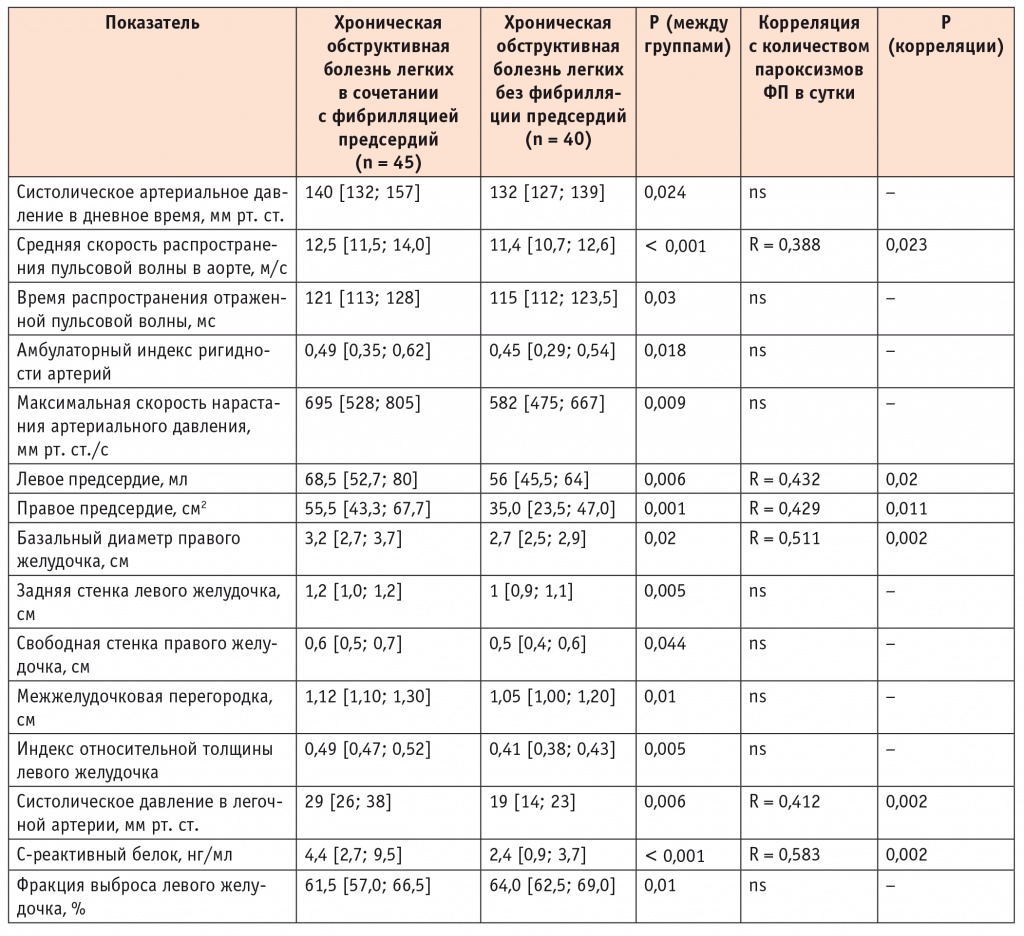
Примечание. Данные представлены в виде медианы и первого и третьего квартилей. Для расчета статистической значимости различий между группами использовали двухсторонний U-критерий Манна — Уитни, для определения взаимосвязи признаков — коэффициент ранговой корреляции Спирмена.
При изучении параметров жесткости сосудистой стенки PWao была статистически значимо выше у больных с ФП (р ˂ 0,001) и коррелировала с количеством пароксизмов (R = 0,388, р = 0,023).
RWTT (р = 0,03), AASI (р = 0,018) и (dP/dt)max (р = 0,009) также оказались выше в группе больных с коморбидной патологией и не коррелировали с количеством пароксизмов ФП. При оценке центрального давления в аорте статистически значимых различий выявлено не было.
Уровень СРБ был выше в группе ХОБЛ и ФП (р = 0,001) и коррелировал с частотой пароксизмов ФП за сутки (R = 0,583; p = 0,002), а также с PWao (R = 0,374, р = 0,04). Повышение жесткости сосудистой стенки и бо,льшая выраженность системного воспаления в группе с ФП, вероятно, обусловлены более тяжелым течением ХОБЛ.
По данным ЭхоКГ, группы статистически значимо различались объемом левого предсердия (р = 0,006) и площадью правого предсердия (р = 0,001), которые коррелировали с частотой пароксизмов ФП (R = 0,432; p = 0,02 и R = 0,429; р = 0,011 соответственно) (см. табл. 2).
Конечный систолический и диастолический размеры и объемы ЛЖ у пациентов обеих групп находились в пределах нормы и статистически значимо не различались. Фракция выброса ЛЖ была ниже у пациентов с ФП (вне пароксизма) (р = 0,01), что говорит о влиянии ФП на сократительную способность миокарда ЛЖ.
Базальный диаметр ПЖ (БДПЖ) был выше у пациентов группы ХОБЛ и ФП (р = 0,02) и коррелировал с частотой пароксизмов (R = 0,511; р = 0,002).
Задняя стенка ЛЖ, свободная стенка ПЖ и межжелудочковая перегородка оказались более утолщенными у больных с ФП (р = 0,005; р = 0,044; р = 0,01 соответственно), однако корреляционной связи этих параметров с частотой пароксизмов ФП выявлено не было. Индекс массы миокарда ЛЖ был выше нормы в обеих группах: у пациентов с ФП (Me [25k%; 75k%]) он составил 138 [128; 154] г/м2, в контрольной группе — 134 [126; 138] г/м2, но без статистически значимых различий. При этом индекс относительной толщины ЛЖ был выше нормальных значений у больных с коморбидной патологией и в норме в группе без ФП (р = 0,005). Таким образом, у пациентов с ФП наблюдался прогностически наиболее неблагоприятный концентрический тип гипертрофии ЛЖ, тогда как у больных ХОБЛ без ФП — эксцентрический.
При оценке диастолической функции выявлено, что соотношение vE/vA ЛЖ было менее 1 в обеих группах, что свидетельствует о наличии диастолической дисфункции I типа, связанной с гемодинамическими изменениями на фоне АГ. DT и IVRT ЛЖ были выше нормы в обеих группах без статистически значимых различий. Систолическое давление в легочной артерии (СисДЛА) было выше в группе ХОБЛ и ФП (р = 0,006) и имело взаимосвязь с количеством пароксизмов (R = 0,412; р = 0,002). Зависимость количества пароксизмов ФП от PWao, БДПЖ, СисДЛА и размеров предсердий была подтверждена в линейном регрессионном анализе.
ОБСУЖДЕНИЕ
Системное воспаление влияет на жесткость сосудистой стенки, о чем свидетельствует прямая корреляционная связь между PWao и уровнем СРБ. Взаимосвязь между PWao, СРБ и количеством пароксизмов ФП позволяет рассматривать эти показатели в качестве предикторов возникновения аритмии.
Более выраженное системное воспаление, бо,льшая жест-кость сосудистой стенки и повышенное систолическое АД днем, характерные для больных с ФП, могут являться механизмами ремоделирования миокарда и способствовать развитию аритмии.
Учитывая статистически значимую корреляционную связь между количеством пароксизмов ФП и СисДЛА, правым предсердием, БДПЖ, можно сделать вывод о влиянии тяжести течения ХОБЛ на возникновение аритмии. Поэтому особенности течения ХОБЛ в качестве предикторов развития ФП должны стать предметом дальнейшего изучения.
Отметим, что у 22 (49%) больных основной группы ФП была выявлена впервые, по результатам ХМ-ЭКГ, и протекала практически бессимптомно, остальные 23 (51%) пациента имели ФП в анамнезе, при этом из всех больных антикоагулянтную терапию получали только 8 (17,8%) человек.
ЗАКЛЮЧЕНИЕ
Параметры, коррелирующие с количеством пароксизмов фибрилляции пердсердий (ФП), могут быть рассмотрены в качестве предикторов развития данного вида аритмии у больных ХОБЛ. К ним относятся средняя скорость распространения пульсовой волны в аорте, СРБ, площадь правого предсердия и объем левого предсердия, базальный диаметр ПЖ и систолическое давление в легочной артерии.
Параметры, имеющие статистически значимые различия между группами, но не коррелирующие с количеством пароксизмов ФП, вероятно, могут рассматриваться как факторы риска развития ФП. Среди них возраст, увеличение времени распространения отраженной пульсовой волны, амбулаторного индекса ригидности артерий и максимальной скорости нарастания АД, а также утолщение задней стенки ЛЖ, межжелудочковой перегородки, свободной стенки ПЖ и повышение индекса относительной толщины ЛЖ.
Частое бессимптомное течение ФП у пациентов с ХОБЛ говорит о необходимости проведения суточного мониторирования ЭКГ по Холтеру для исключения данного вида аритмии.








