Вместе с тем, несмотря на значительно меньшее периоперационное агрессивное воздействие по сравнению с открытыми оперативными вмешательствами, малоинвазивные манипуляции сопряжены с определенным риском развития осложнений. Существуют и риски, связанные с анестезией.
Особенности клинических проявлений гематологических заболеваний, характеризующиеся значимыми изменениями системы гемостаза и патологической деформацией иммунного ответа, диктуют необходимость использования дифференцированных протоколов лечения и, следовательно, исключают возможность полного унифицирования методов анестезиологической протекции. Вероятность периоперационных осложнений для рассматриваемого контингента больных необходимо прогнозировать с учетом возможности развития кровотечения или, напротив, тромбозов, а также ургентных ситуаций, обусловленных манифестацией острой сердечно-сосудистой недостаточности вследствие исходно сниженных резервов адаптации [10–12, 16, 17].
Анестезиологическое сопровождение малоинвазивных диагностических и хирургических вмешательств в детской гематологии осуществляется в соответствии с положениями Федерального закона от 21.11.2011 № 323-ФЗ (редакция от 13.07.2015, с изменениями от 30.09.2015) «Об основах охраны здоровья граждан в Российской Федерации» (с изменениями и дополнениями, вступившими в силу с 24.07.2015), приказа Министерства здравоохранения Российской Федерации от 15.11.2012 № 919н «Об утверждении Порядка оказания медицинской помощи взрослому населению по профилю “анестезиология и реаниматология”», а также приказа Министерства здравоохранения Российской Федерации от 12.11.2012 № 909н «Об утверждении Порядка оказания медицинской помощи детям по профилю “анестезиология и реаниматология”».
Показаниями для анестезиологического обеспечения малоинвазивных вмешательств в детской гематологии служат следующие клинические ситуации [7, 8]:
-
обеспечение центрального сосудистого доступа;
-
пункции костного мозга и поясничные пункции;
-
лучевая и радиоизотопная диагностика;
-
лучевая терапия;
-
эндоскопические исследования;
-
стоматологические манипуляции;
-
отоларингологические операции.
Требования к препаратам для общей анестезии в детской гематологии: быстрота действия, безопасность, контролируемость анестетического эффекта, возможность использования в условиях гиповолемии [1–6, 9, 13–15]. Среди препаратов для индукции в общую анестезию у детей наиболее распространен севофлуран [3–5, 8, 13–15]. Препарат обладает относительно приятным запахом и не раздражает слизистые оболочки дыхательных путей, что позволяет обеспечить комфортное проведение аппаратно-масочной индукции у детей без рутинной предварительной премедикации.
В ФГБУ «ФНКЦ детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» Минздрава России используют анестезиологические протоколы, в соответствии с которыми близкие люди находятся с ребенком на начальных этапах анестезии. Присутствие родителей в момент засыпания ребенка успокаивает его. Родителям ребенка тщательно объясняют, каковы возможные риски развития побочных реакций на ингаляцию анестетика, на что они должны обращать внимание, а также действия медицинского персонала в указанных ситуациях. Проведение комфортной для ребенка индукции севофлураном возможно со скоростью, сопоставимой с действием внутривенных анестетиков. При использовании не более 2 минимальных альвеолярных концентраций (МАК) изменения частоты дыхания и дыхательного объема не превышают 30% исходных значений.
Индукция осуществляется на спонтанном дыхании во избежание нарушений механики дыхания, а также выраженных изменений давления в дыхательных путях. Выполнение индукции севофлураном возможно методом «пошаговой» индукции или методом «болюсной» индукции [3]. Окончанием индукции считают достижение концентрации севофлурана в выдыхаемом воздухе, равном MAKEI.
Под МАКEI принято понимать концентрацию анестетика в конце выдоха, достаточную для выполнения мягкой интубации трахеи при отсутствии в 50% случаев двигательной реакции на раздувание манжеты без использования дополнительных средств для анестезии. Достижение MAKEI позволяет обеспечить надежную проходимость дыхательных путей посредством интубации трахеи при необходимости избежать применения миорелаксантов (например, в случае прогнозируемых «трудных дыхательных путей»). МАКEI у детей от года до 9 лет составляет 2,69–2,83 об%, а у пациентов старше 16 лет — 4,52 об%.
Поддержание анестезии при моноанестезии севофлураном отличается некоторыми особенностями. На этапе поддержания анестезии концентрацию препарата уменьшают до 2,5 об%, а поток свежего газа снижают до 1–2 л/мин. Однако в целом анестетик характеризуется высокой степенью управляемости анестезии как на этапе ее поддержания, так и на этапе пробуждения.
У детей с обеспеченным сосудистым доступом в случае экстренной операции и при высоком риске регургитации предпочтительна внутривенная индукция в анестезию, в прочих случаях обеспечение венозного доступа возможно после ингаляционной индукции. Кроме того, иногда родители ребенка или сам пациент, достигший 15 лет, настаивают именно на внутривенной анестезии, мотивируя отказ от ингаляционной анестезии севофлураном риском развития возбуждения или рвоты. Принимая во внимание необходимость поддержания устойчивого продуктивного контакта анестезиолога с больным и его родственниками, действия анестезиологической службы должны быть направлены на достижение компромиссного решения между предпочтениями больного и объективными показаниями к применению того или иного метода анестезии. Выбор внутривенного метода анестезии может быть обусловлен «технологическими» факторами, например отсутствием в малой операционной наркозно-дыхательной аппаратуры с современными испарителями; столь же значимо и отсутствие принудительного отвода газов от аппарата, в связи с чем происходит загрязнение воздуха операционной парами севофлурана.
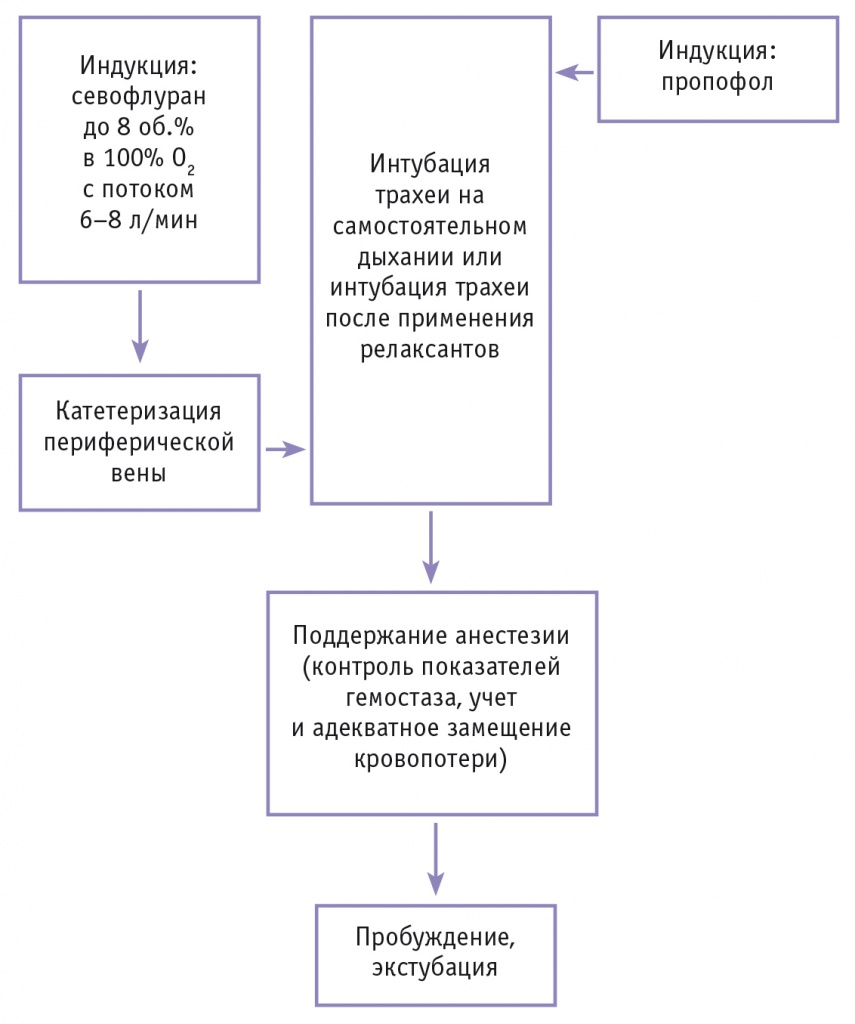
Стандартная схема анестезии при выполнении малоинвазивной операции в области носоглотки представлена на рисунке [8]. Если пациенту ранее установлен внутривенный катетер, то схема анестезии отличается внутривенной индукцией с обязательным применением миорелаксантов для интубации [8].
Рис. Схема анестезии при выполнении операции в области носоглотки
Ниже приведен клинический пример предоперационного обследования и анестезиологического обеспечения ребенка с геморрагической тромбоцитопатией: сочетанным дефицитом плотных и α-гранул тромбоцитов.
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ
Девочка А. А., 5 лет, наблюдалась гематологом консультативного отделения Центра в связи с жалобами на повторные носовые кровотечения попеременно из правой и левой ноздри и однократно — из обеих. В возрасте 3 лет интенсивность носовых кровотечений увеличилась. Описанные эпизоды максимальной длительностью до 30 минут наблюдались практически ежедневно, вне зависимости от времени суток, чаще купировались самостоятельно, однократно был необходим вызов бригады скорой помощи. Других проявлений геморрагического синдрома у ребенка не наблюдалось, травм, операций, экстракции зубов не было. Кроме того, в феврале 2014 г. у пациентки обнаружена шейная лимфоаденопатия шейно-подчелюстной области неясного генеза (периодически — примерно раз в 3 месяца — получает курсы антибактериальной терапии с хорошим эффектом). Максимальный размер лимфатического узла (в шейной группе) — 24 мм, в динамике без увеличения. Как известно из семейного анамнеза, у старшей сестры также отмечали рецидивирующие носовые кровотечения, легкое появление экхимозов, обструктивный бронхит; у матери — обильные менструации, в детстве были рецидивирующие носовые кровотечения. По результатам обследования, у девочки не обнаружено признаков геморрагической коагулопатии и/или болезни Виллебранда, исследование функциональной активности тромбоцитов выявило сочетанный дефицит плотных и α-гранул. Ребенок осмотрен оториноларингологом консультативного отделения Центра. Учитывая основное заболевание, рекомендована плановая госпитализация для проведения оперативного вмешательства в объеме отсепаровки слизистой оболочки перегородки носа и биопсии подчелюстного лимфатического узла.
При поступлении состояние ребенка удовлетворительное. Кожный покров и видимые слизистые оболочки обычной окраски, кожный геморрагический синдром представлен единичными посттравматическими экхимозами. Периферические лимфатические узлы — единичные мелкие мягкие, безболезненные, пальпируются по задней шейной, передней шейной, подмышечной и паховой группам. При пальпации мягких тканей поднижнечелюстного треугольника слева выявлено смещаемое безболезненное образование плотноэластической консистенции до 2,5–3,0 см в диаметре. Кожа над образованием не изменена. В легких дыхание пуэрильное, проводится во все отделы, хрипов нет. Сердечные тоны ясные, ритмичные. Живот мягкий, безболезненный при пальпации. Пальпируется край печени, селезенка не пальпируется. Физиологические отправления — без особенностей. В рамках предоперационного обследования у ребенка подтвержден сочетанный дефицит плотных и α-гранул тромбоцитов. Данных за геморрагическую коагулопатию не получено.
На основании клинических данных анестезиологическое обеспечение предполагалось выполнить в условиях комбинированной анестезии с искусственной вентиляцией легких через эндотрахеальную трубку. Тест Маллампати I. ASA III. Статус операции: II (операции умеренной степени риска).
Учитывая высокий риск развития интраоперационного жизнеугрожающего кровотечения, принято решение о плановой катетеризации центральной вены в предоперационном периоде. Во избежание непреднамеренной травматизации центральных сосудов при «слепой» методике постановки центрального венозного катетера, а также повышенного риска кровоточивости из места пункции за сутки до оперативного вмешательства пациентке установлен катетер типа PICC-line диаметром 3 Fr. Установка катетера выполнена в медиальную подкожную вену левого плеча (v. basilica) под контролем ультразвуковой навигации в динамической методике и под R-графическим контролем положения, без технических сложностей.
Принимая во внимание риск жизнеугрожающего кровотечения, на интраоперационный период в отделе трансфузиологии, заготовки и процессинга гемопоэтических стволовых клеток зарезервирован тромбоцитный концентрат, а также заготовлен концентрат активированного рекомбинантного человеческого фактора свертывания крови VII (рVIIa).
Согласно рекомендациям гематолога, в рамках антигеморрагической профилактики за сутки до хирургического вмешательства начата терапия этамзилатом по 100 мг через каждые 8 часов в/в струйно. Непосредственно за час до вмешательства дополнительно введено 200 мг этамзилата. На фоне адекватного местного гемостаза проведены эндоскопическая подслизистая отслойка зоны Киссельбаха слева, биопсия подчелюстного лимфатического узла слева. Во время операции план хирургического вмешательства выполнен. С целью защиты дыхательных путей в течение анестезии пациентка после внутривенной индукции интубирована оротрахеально, затем проводили эндотрахеальную анестезию на основе десфлурана для более быстрого восстановления сознания и глоточных рефлексов в послеоперационном периоде. Течение анестезии без особенностей, кровотечение минимальное. После окончания оперативного вмешательства надманжеточное пространство осмотрено эндоскопически, санировано. Пациентка экстубирована по восстановлении триады Гейла. В послеоперационном периоде повышения кровоточивости не наблюдали.
Через час после вмешательства повторно введен раствор этамзилата в дозе 200 мг в/в струйно. В течение первых послеоперационных суток проводили профилактику этамзилатом по 200 мг через каждые 8 часов, затем дозу препарата снизили до 100 мг через каждые 8 часов в/в струйно. Ребенок повторно осмотрен гематологом на 1-е и 3-и сутки после операции. Ввиду отсутствия кровотечения антигеморрагическая профилактика прекращена на 4-е сутки. Введения тромбоцитного концентрата или рVIIa не потребовалось.
ЗАКЛЮЧЕНИЕ
Малоинвазивные процедуры у детей с гематологическими заболеваниями выполняют в соответствии с принятыми протоколами и регламентами анестезиологического обеспечения. Предоперационная подготовка предусматривает расширенное обследование, включающее лабораторную и инструментальную диагностику, в условиях взаимодействия реанимационно-анестезиологической и гематологической служб стационара.








